- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Свободные аминокислоты. значение и пути синтеза белковых и небелковых аминокислот. (Лекция 4) презентация
Содержание
- 1. Свободные аминокислоты. значение и пути синтеза белковых и небелковых аминокислот. (Лекция 4)
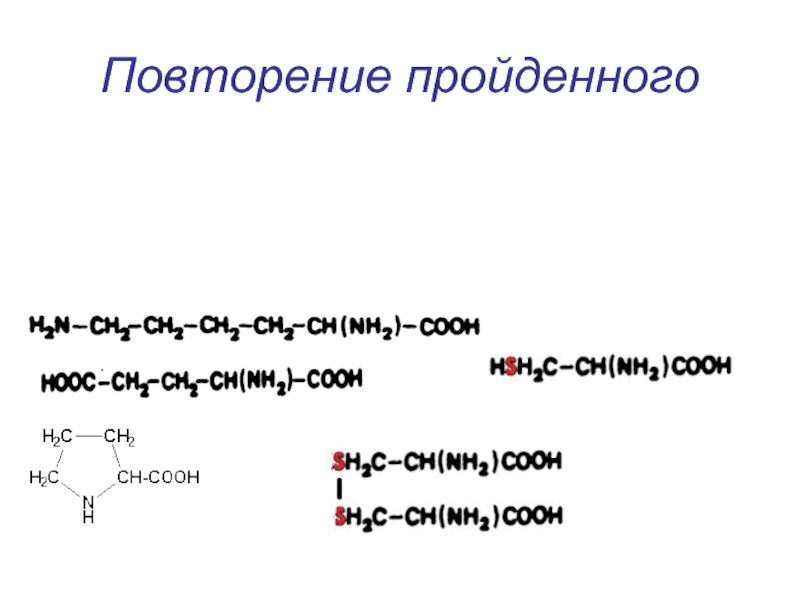
- 2. Повторение пройденного
- 3. Незаменимые аминокислоты (человек, min в сут) НО: для птиц незаменим глицин…
- 4. Аминокислоты Протеиногенные (белковые) – именно они
- 5. Формулы к контрольной работе 1) 3,4-дигидроксифен 2)
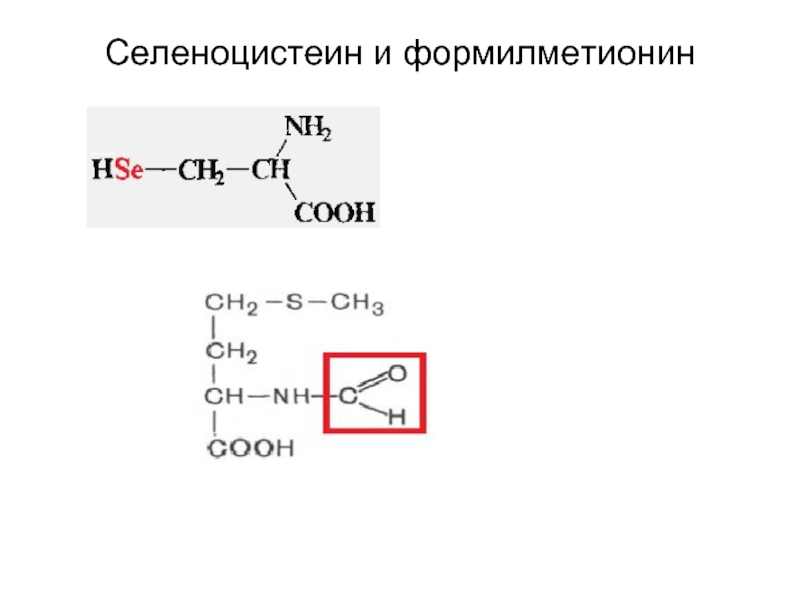
- 6. Селеноцистеин и формилметионин
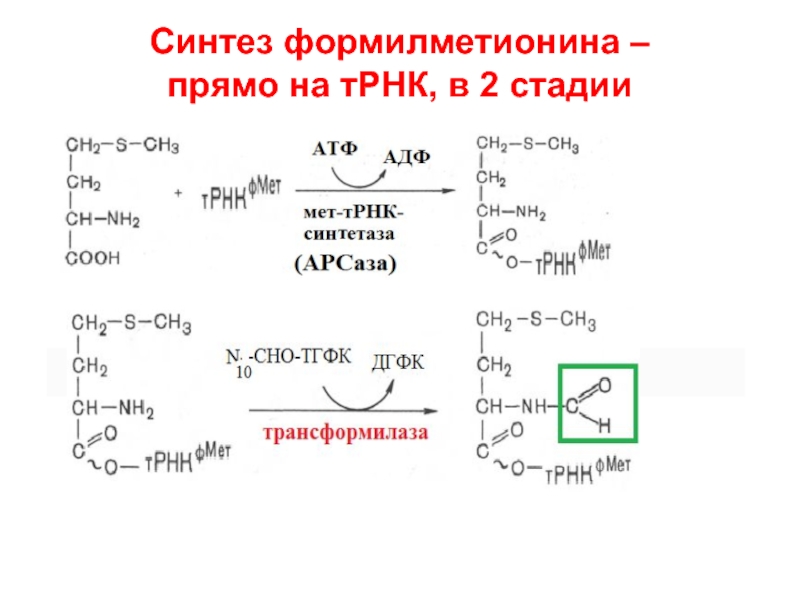
- 7. Синтез формилметионина – прямо на тРНК, в 2 стадии
- 8. Протеиногенные аминокислоты именно они кодируются в ДНК. Это всегда α, L-аминокислоты Как они синтезируются?
- 9. Какие пути синтеза аминокислот вам известны? 1)
- 10. Гистидин – особый путь
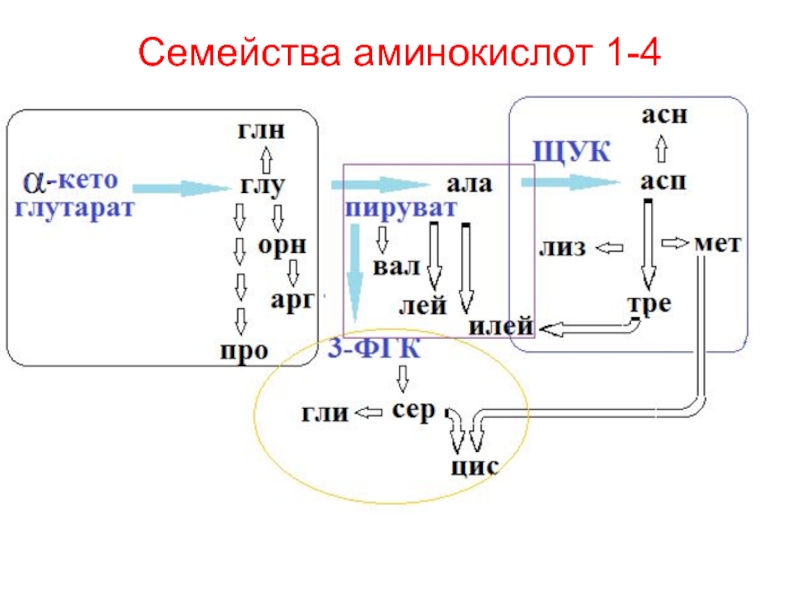
- 11. Семейства аминокислот 1-4
- 12. Семейство 5 (ароматические) – по шикиматному пути
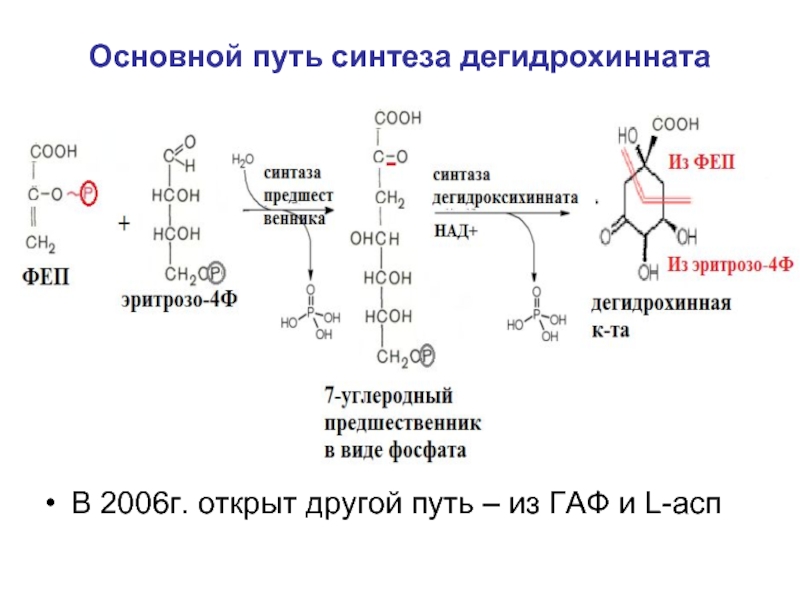
- 13. Основной путь синтеза дегидрохинната В 2006г. открыт другой путь – из ГАФ и L-асп
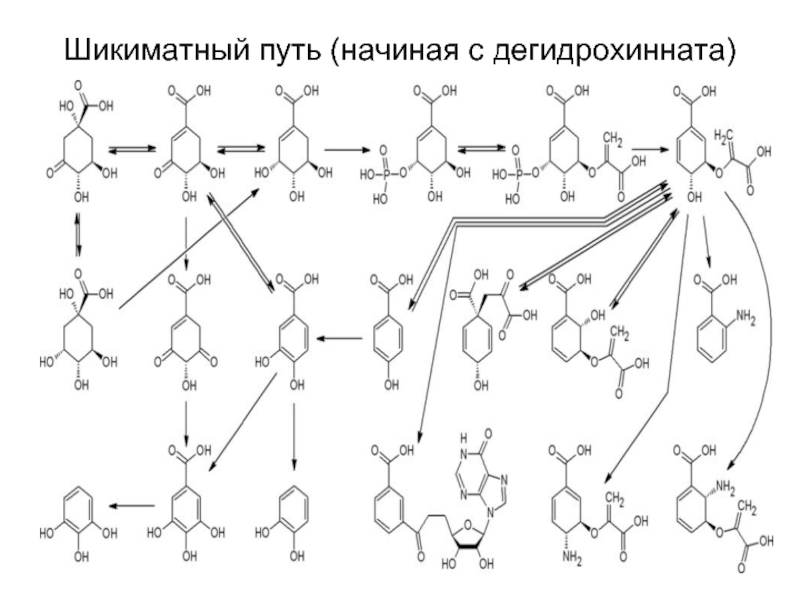
- 14. Шикиматный путь (начиная с дегидрохинната)
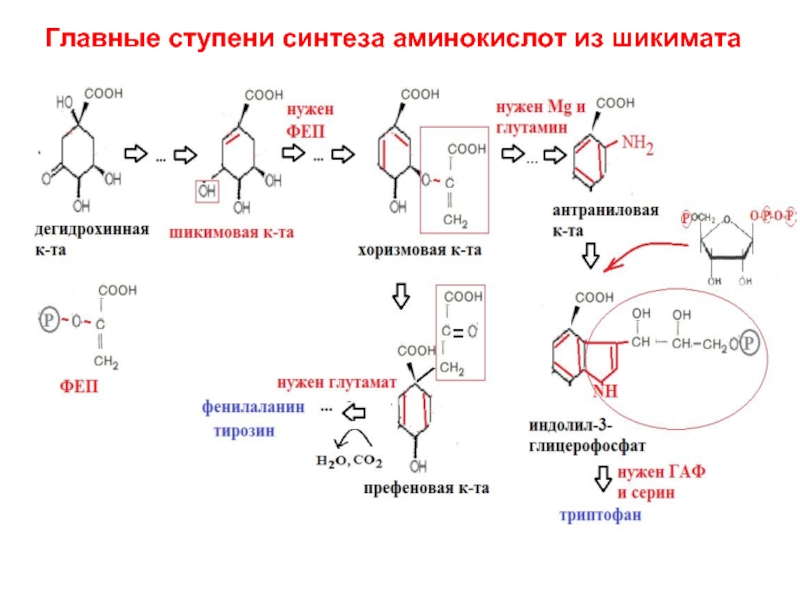
- 15. Главные ступени синтеза аминокислот из шикимата
- 16. Небелковые аминокислоты Небелковые аминокислоты синтезируются, если у
- 17. Функции аминокислот в экологических взаимодействиях 1) Средообразующая
- 18. Mucuna (сем. Бобовые) – зудящие бобы Гриффония
- 19. Аланин и его вариации (более 30 в
- 20. Небелковые аминокислоты синтезируются имеющимися в клетке ферментами.
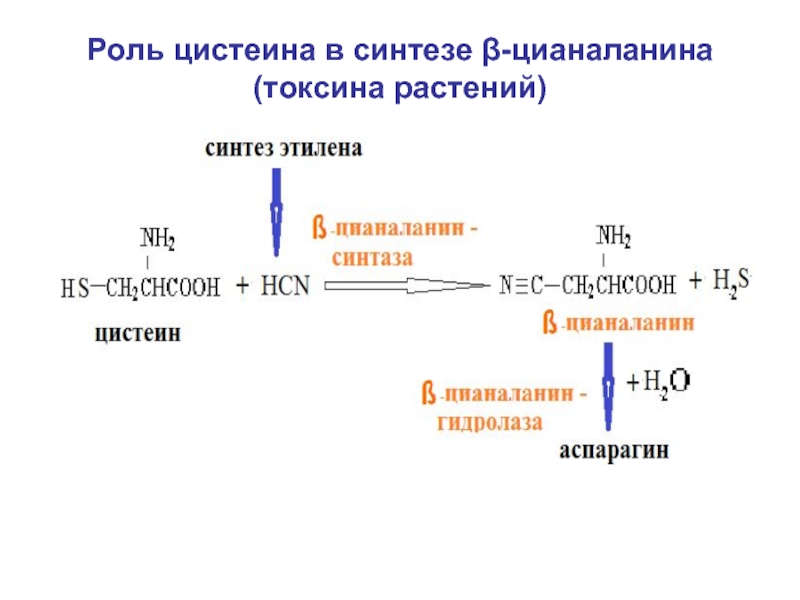
- 21. Роль цистеина в синтезе β-цианаланина (токсина растений)
- 22. Пример 3. Синтез 3,4-дигидроксифенилаланина Mucuna – зудящие
- 23. Пример 4. Синтез 5-гидрокситриптофана у животных и
- 24. Пример 5. Синтез азетидин-2-карбоновой кислоты Convallaria majalis
- 25. Антибиотики бацитрацин и грамицидин S содержат небелковые
- 26. Глутамат нужен для синтеза хлорофилла на этапе 1 пути “зеленого растения”
- 27. Синтез нетипичных аминокислот после построения белка
- 28. Приложение
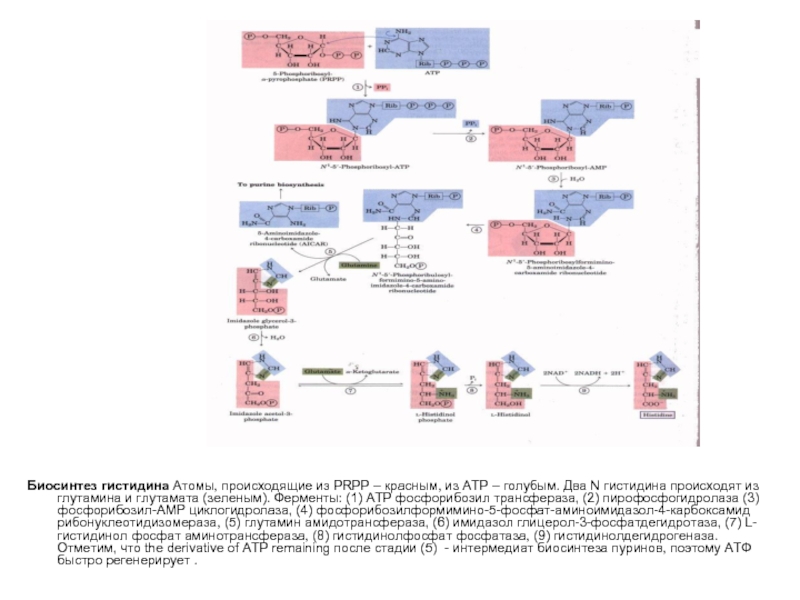
- 29. Биосинтез гистидина Атомы, происходящие из PRPP – красным,
- 30. Путь синтеза дегидрохинната у ряда архей, не имеющих ДАГФ-синтазы
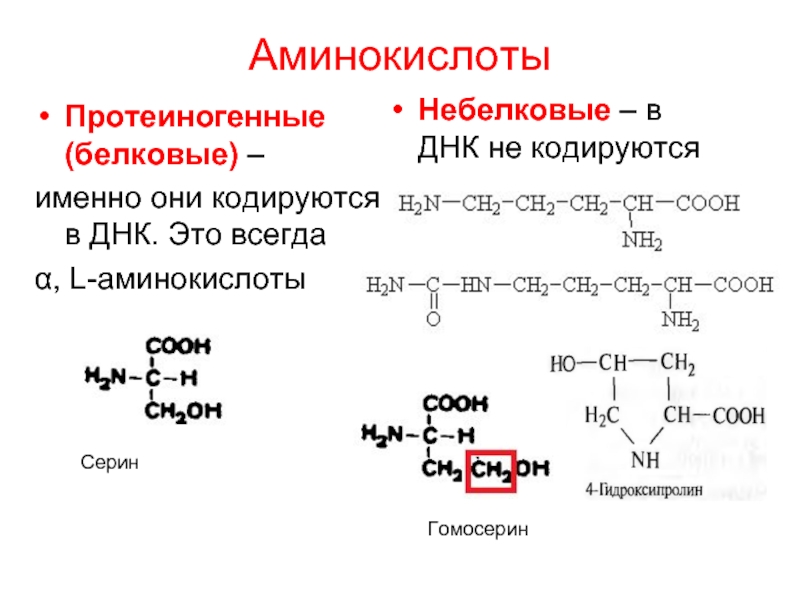
Слайд 4Аминокислоты
Протеиногенные (белковые) –
именно они кодируются в ДНК. Это всегда
α,
Небелковые – в ДНК не кодируются
Серин
Гомосерин
Слайд 5Формулы к контрольной работе
1) 3,4-дигидроксифен
2) 5-гидрокситри
3) азетидин-2-карбоновая к-та
4) цианаланин
5) гомосерин
6) ацилгомосеринлактон
7)
8) селеноцистеин
Слайд 8Протеиногенные аминокислоты
именно они кодируются в ДНК. Это всегда α, L-аминокислоты
Как они
Слайд 9Какие пути синтеза аминокислот вам известны?
1) прямое восстановительное аминирование
1а) –
2) переаминирование
3) ферментативные превращения
Слайд 12Семейство 5 (ароматические) – по шикиматному пути
1) синтез дегидрохинной кислоты (дегидрохинната),
2) синтез шикимовой кислоты из дегидрохинната
3) синтез фенилаланина, тирозина, триптофана
Слайд 16Небелковые аминокислоты
Небелковые аминокислоты синтезируются, если у организма имеются особые ферменты для
Слайд 17Функции аминокислот в экологических взаимодействиях
1) Средообразующая функция -нет
2) Химические предшест-венники для
3) Защита
4) Функция нападения - нет
5) Сигнальная -?
-
Нужны при синтезе сигналов QS, токсинов, антибиотиков, пигментов и др.
От конкурентов (аллелопати-ческие агенты), от поедания (токсины, детерренты), при осмопротекции
-
Вкусовые аттрактанты (приманки для рыб).
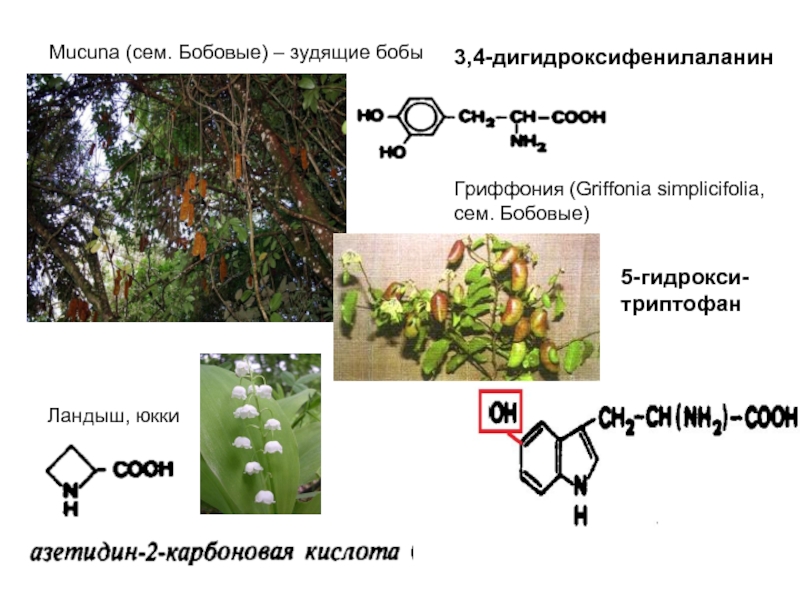
Слайд 18Mucuna (сем. Бобовые) – зудящие бобы
Гриффония (Griffonia simplicifolia, сем. Бобовые)
3,4-дигидроксифенилаланин
5-гидрокси-триптофан
Ландыш,
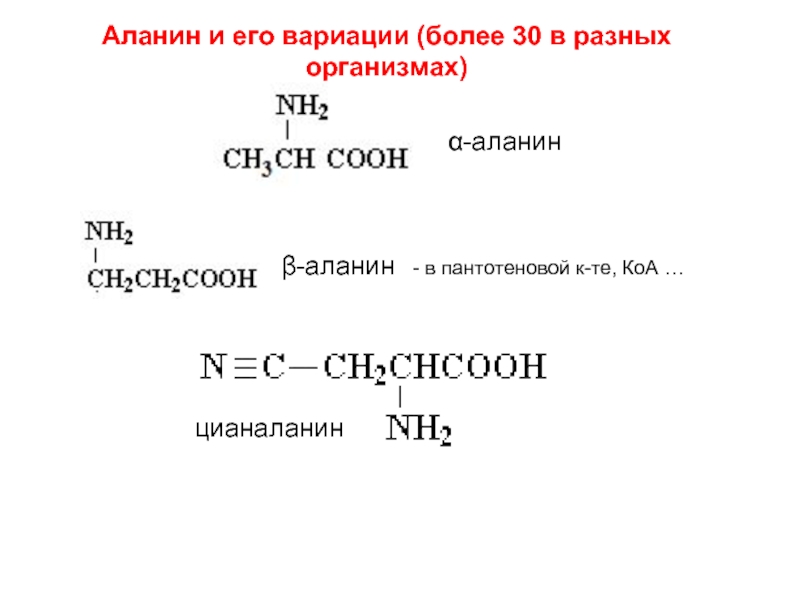
Слайд 19Аланин и его вариации (более 30 в разных организмах)
α-аланин
β-аланин
цианаланин
Слайд 20Небелковые аминокислоты синтезируются имеющимися в клетке ферментами.
Пример 1. Синтез β-аланина
β-аланин затем может пойти на синтез КоА:
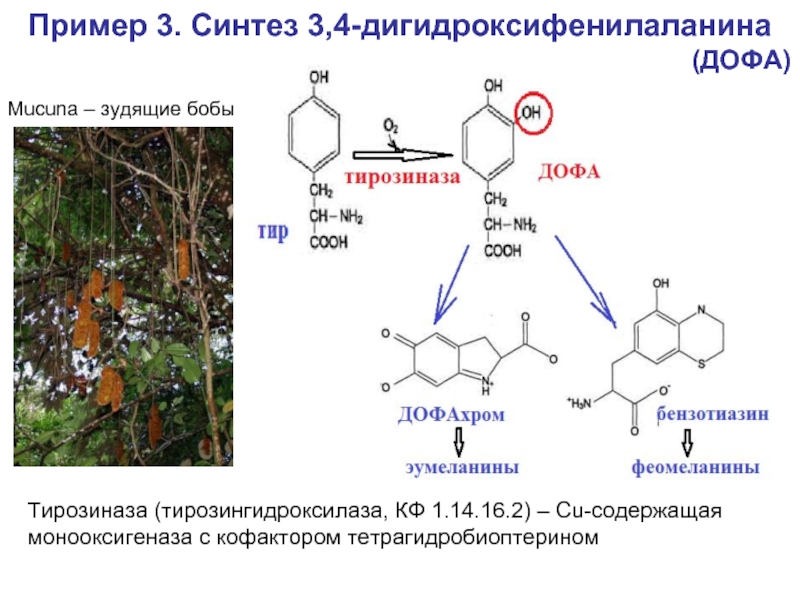
Слайд 22Пример 3. Синтез 3,4-дигидроксифенилаланина
Mucuna – зудящие бобы
(ДОФА)
Тирозиназа (тирозингидроксилаза, КФ 1.14.16.2) –
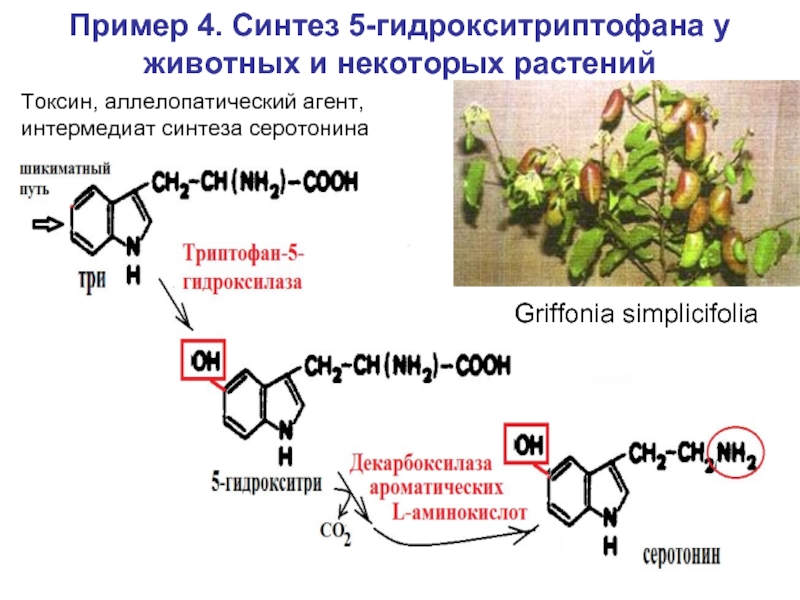
Слайд 23Пример 4. Синтез 5-гидрокситриптофана у животных и некоторых растений
Griffonia simplicifolia
Токсин,
Слайд 24Пример 5. Синтез азетидин-2-карбоновой кислоты
Convallaria majalis (до 7% сухого веса листьев).
У ряда Streptomyces - антибиотик и сильный токсин для человека.
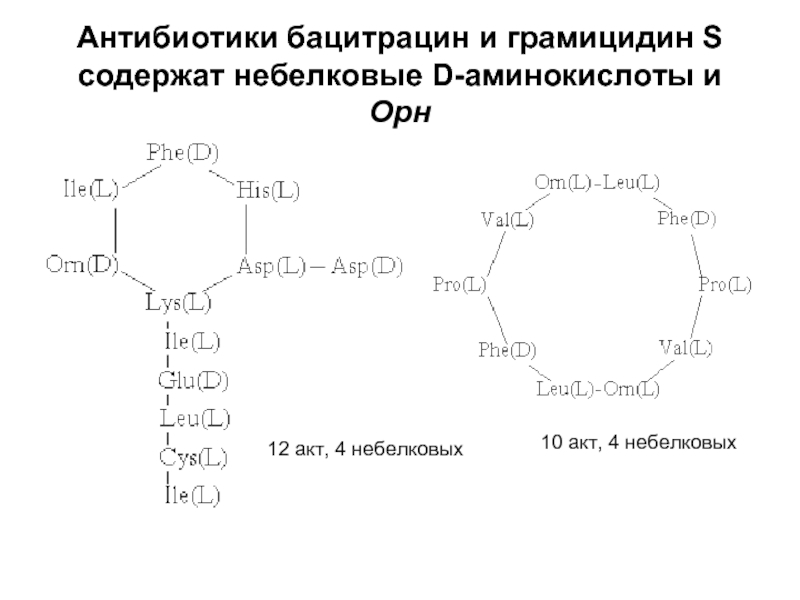
Слайд 25Антибиотики бацитрацин и грамицидин S
содержат небелковые D-аминокислоты и Орн
12 акт, 4
10 акт, 4 небелковых
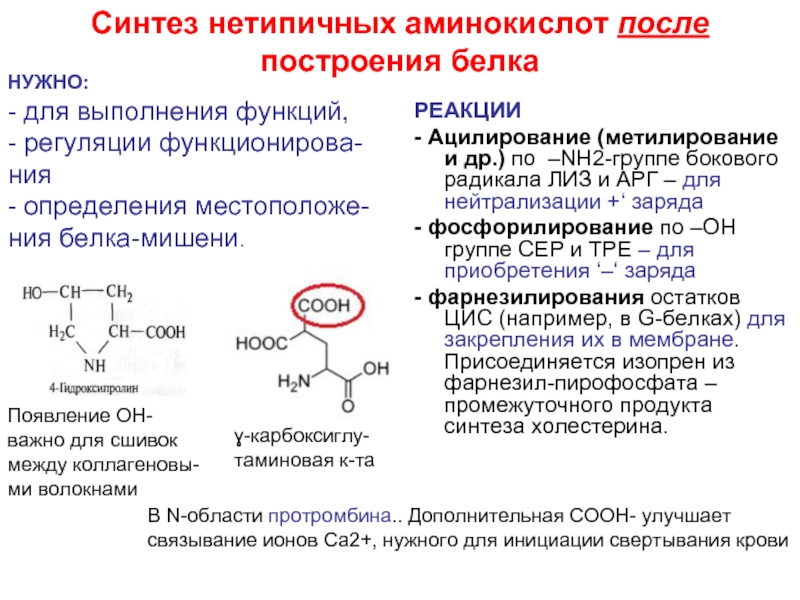
Слайд 27Синтез нетипичных аминокислот после построения белка
РЕАКЦИИ
- Ацилирование (метилирование и др.) по
- фосфорилирование по –OH группе СЕР и ТРЕ – для приобретения ‘–‘ заряда
- фарнезилирования остатков ЦИС (например, в G-белках) для закрепления их в мембране. Присоединяется изопрен из фарнезил-пирофосфата – промежуточного продукта синтеза холестерина.
НУЖНО:
- для выполнения функций,
- регуляции функционирова-ния
- определения местоположе-ния белка-мишени.
Появление ОН- важно для сшивок между коллагеновы-ми волокнами
ɣ-карбоксиглу-таминовая к-та
В N-области протромбина.. Дополнительная СООН- улучшает связывание ионов Са2+, нужного для инициации свертывания крови