- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Современные методы ДНК-диагностики наследственных болезней презентация
Содержание
- 1. Современные методы ДНК-диагностики наследственных болезней
- 2. План Введение Молекулярно-генетические метод ДНК-диагностика
- 3. Введение Нынешний мир это место, где
- 4. Молекулярно-генетические метод Это большая и разнообразная группа
- 5. ДНК-диагностика ДНК-диагностика — это один из наиболее
- 6. Типы ДНК-диагностики Прямая Определение мутации, являющейся непосредственной
- 7. Методы ДНК-диагностики Во время диагностики цепи ДНК
- 8. Цитогенетический метод С помощью данного метода
- 11. Методы идентификации мутаций генов наследственных болезней К
- 12. Диагностика с использованием метода Fluorescence in situ
- 13. Метод FISH-диагностики FISH анализ осуществляется в несколько
- 14. Полимеразная цепная реакция Полимеразная цепная реакция
- 15. Стадии ПЦР Денатурация – переход ДНК из
- 17. ДНК-секвенирование Вплоть до настоящего времени «золотым
- 18. ДНК-секвенирование Производится ПЦР-амплификация фрагмента ДНК К полученному
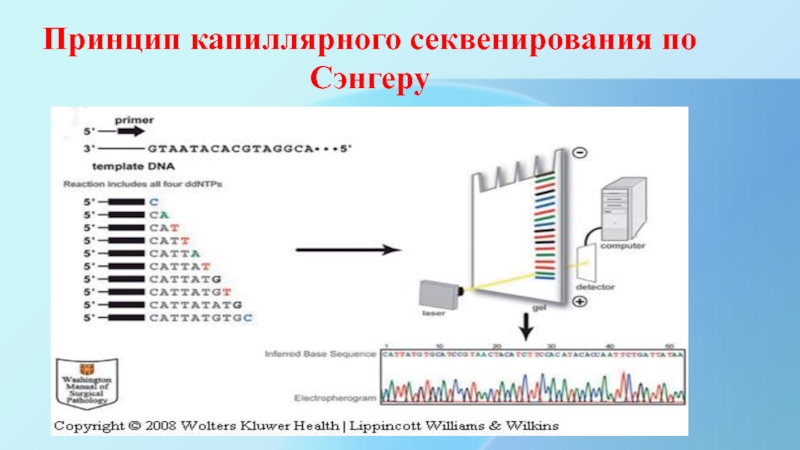
- 19. Принцип капиллярного секвенирования по Сэнгеру
- 20. Секвенирование нового поколения (NGS) Новые технологии секвенирования
- 21. Секвенирование нового поколения (NGS) Несмотря на свою
- 22. Заключение На сегодняшний день, технологии уже
- 23. Список использованной литературы «Медицинская биология и генетика»
Слайд 1Современные методы ДНК-диагностики наследственных болезней
Выполнил: студент 1 курса,
факультета ОМ
Группы 028-2
Нишанбаев
Слайд 2План
Введение
Молекулярно-генетические метод
ДНК-диагностика
Типы ДНК-диагностики
Методы ДНК-диагностики
Диагностика с использованием метода Fluorescence
Метод FISH-диагностики
Полимеразная цепная реакция
Стадии ПЦР
ДНК-секвенирование
Заключение
Список использованной литературы
Слайд 3Введение
Нынешний мир это место, где день ото дня люди открывают
Слайд 4Молекулярно-генетические метод
Это большая и разнообразная группа методов, позволяющих выявить различные вариации
Слайд 5ДНК-диагностика
ДНК-диагностика — это один из наиболее современных высокотехнологичных методов исследования. ДНК-анализы
Слайд 6Типы ДНК-диагностики
Прямая
Определение мутации, являющейся непосредственной причиной заболевания
При прямой диагностике обнаруживают
Прямые методы отличаются точностью, достигающей почти 100 %
Показаны для таких заболеваний, как фенилкетонурия, муковисцидоз, хорея Гентингтона и другие
Косвенная
Определение хромосомы, несущей поврежденный ген при семейном анализе
Косвенные методы ДНК-диагностики применяются в тех случаях, когда при наследственных заболеваниях ген не клонирован или заболевания сопровождается повреждением различных генов, либо молекулярная организация гена не позволяет использовать прямые методы.
Точность косвенной диагностики значительно меньше, чем прямой диагностики
Слайд 7Методы ДНК-диагностики
Во время диагностики цепи ДНК могут выявляться различные нарушения и
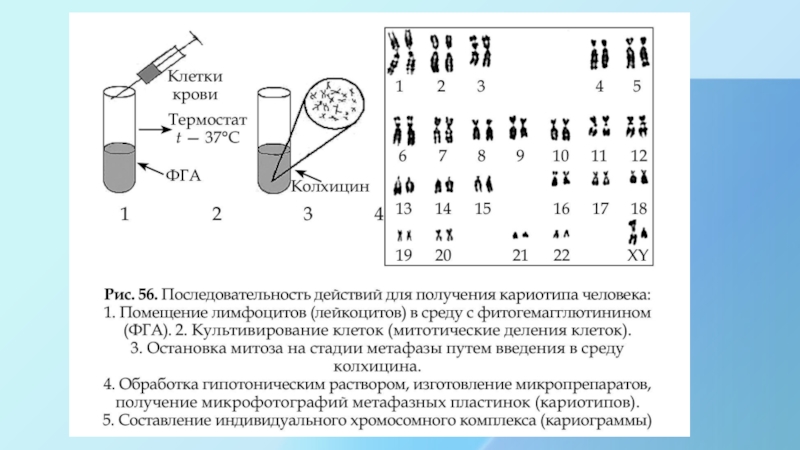
Слайд 8Цитогенетический метод
С помощью данного метода можно изучать наследственный материал клетки:
Слайд 11Методы идентификации мутаций генов наследственных болезней
К методам идентификации мутаций генов наследственных
-идентификация известных мутаций,
-идентификация невыявленных мутаций,
-идентификация мутаций и генетических полиморфизмов.
Слайд 12Диагностика с использованием метода Fluorescence in situ Hybridization (FISH)
Классический метод FISH-анализа
Слайд 13Метод FISH-диагностики
FISH анализ осуществляется в несколько этапов:
получение препаратов и их
мечение ДНК-пробы;
-гибридизация с ДНК-пробой, то есть собственно технология FISH:
-денатурация препаратов;
-денатурация ДНК-проб;
-процедура гибридизации;
-окраска препаратов;
детекция ДНК-зонда при микроскопическом анализе
Слайд 14Полимеразная цепная реакция
Полимеразная цепная реакция (ПЦР) – экспериментальный метод молекулярной
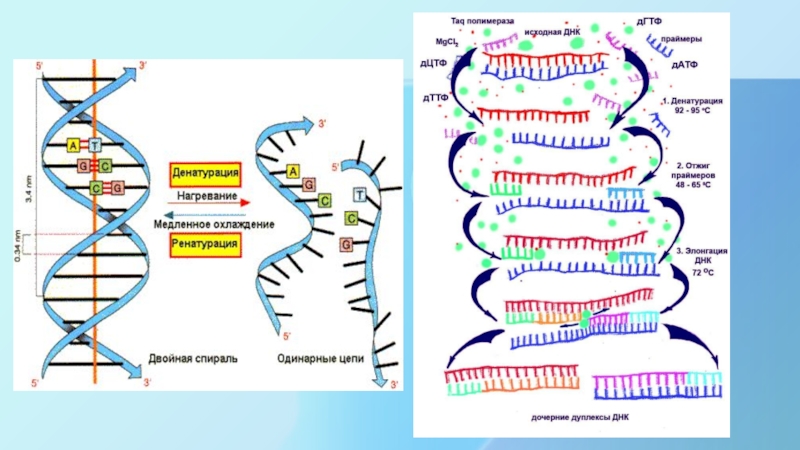
Слайд 15Стадии ПЦР
Денатурация – переход ДНК из двухнитевой формы в однонитевую при
Отжиг - присоединение праймеров к одноцепочечной ДНК-мишени. Праймеры подбирают так, что они ограничивают искомый фрагмент и комплементарны противоположным цепям ДНК. Отжиг происходит в соответствии с правилом комплементарности Чаргаффа.
Элонгация (синтез) - после отжига праймеров Taq-полимераза начинает достраивание второй цепи ДНК с 3'-конца праймера
Слайд 17ДНК-секвенирование
Вплоть до настоящего времени «золотым стандартом» ДНК-диагностики остается традиционное секвенирование.
Фредерик Сэнгер
Слайд 18ДНК-секвенирование
Производится ПЦР-амплификация фрагмента ДНК
К полученному продукту добавляют прямой или обратный праймер
В ходе реакции ДНК-полимераза встраивает в растущую цепь ДНК терминирующий нуклеотид, который прекращает синтез после соответствующего нуклеотида.
Образуется большое число фрагментов ДНК, отличающихся по длине на один нуклеотид
Фрагменты ДНК движутся в тонком капилляре, заполненном полиакриламидным гелем, и разделяются в соответствии с их длиной.
Флуоресцентный сигнал от каждого терминирующего нуклеотида детектируется с помощью лазера и преобразуется в хроматограмму, где каждый нуклеотид представлен в виде пика соответствующего цвета (красный, синий, зеленый, черный).
Слайд 20Секвенирование нового поколения (NGS)
Новые технологии секвенирования позволяют избавиться от главного недостатка
Слайд 21Секвенирование нового поколения (NGS)
Несмотря на свою недолгую историю, секвенирование нового поколения
Прибор для полногеномного секвенирования HiSeq2000 фирмы Illumina
Слайд 22Заключение
На сегодняшний день, технологии уже позволяют выявлять множество болезней при
Слайд 23Список использованной литературы
«Медицинская биология и генетика» Учебное пособие для студентов медицинских
«Традиционные методы ДНК-диагностики генных мутаций» В.В.Стрельников, Н.И. Пирогова, 2016г. http://genschool.ru/wa-data/public/site/1.5_Tradits_metody_StrelnikovVV.pdf
«Применение молекулярних технологий нового поколения в медицинской генетике», Е.Н.Суспицын, А.П.Соколенко, 2013г https://gpma.ru/structure/chair/med_gen/prim_moltech.pdf
Методы молекулярно-генетической диагностики сегодня. Никоненко Т.А., 2008г.http://www.ramld.ru/articles/files/nikonenkoLM9.pdf
Fluorescence in situ hybridisation (FISH). Unique, 2013г. http://www.rarechromo.org/information/Other/FISH%20FTNW.pdf
http://yamedik.org/?p=61&c=biologiya/bio_gen_myt