- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Обмін ліпідів презентация
Содержание
- 1. Обмін ліпідів
- 3. План лекції 1.Травлення ліпідів у кишково-шлунковому тракті
- 5. Запас енергетичних ресурсів у організмі людини Energy
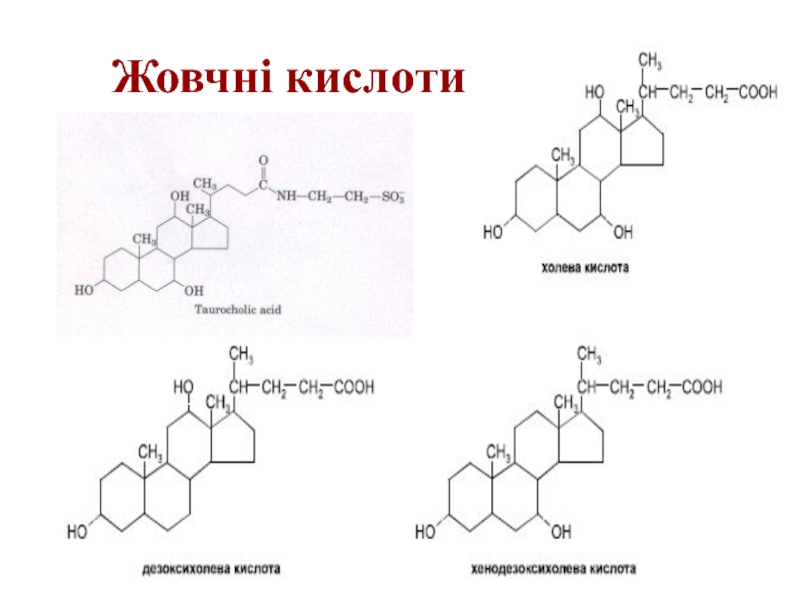
- 6. Жовчні кислоти
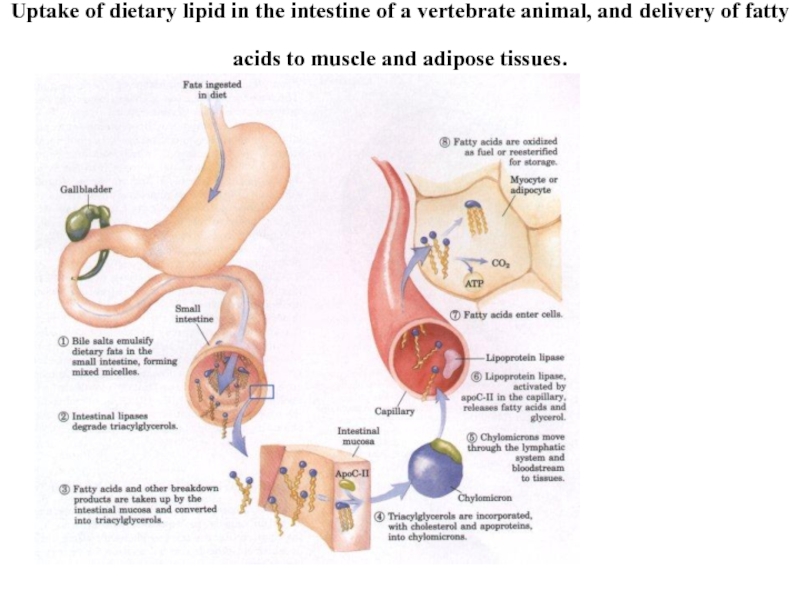
- 7. Uptake of dietary lipid in the intestine
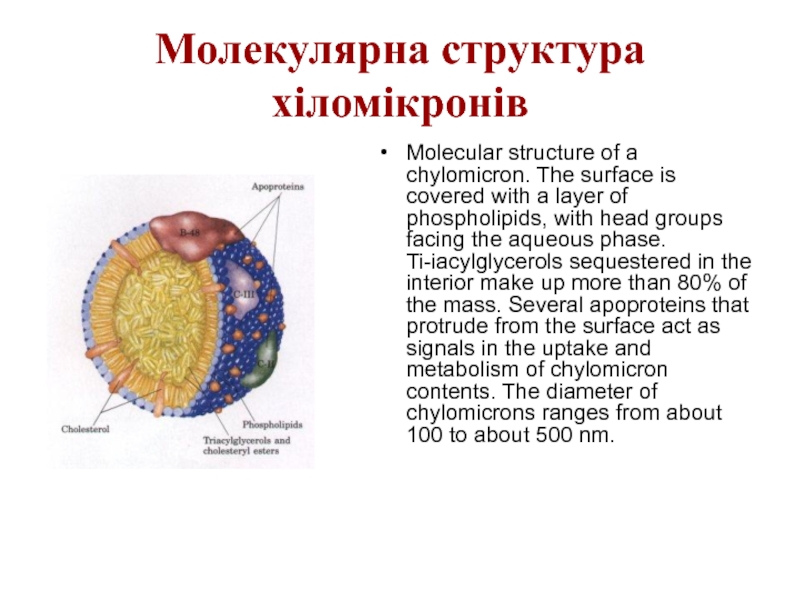
- 8. Молекулярна структура хіломікронів Molecular structure of a
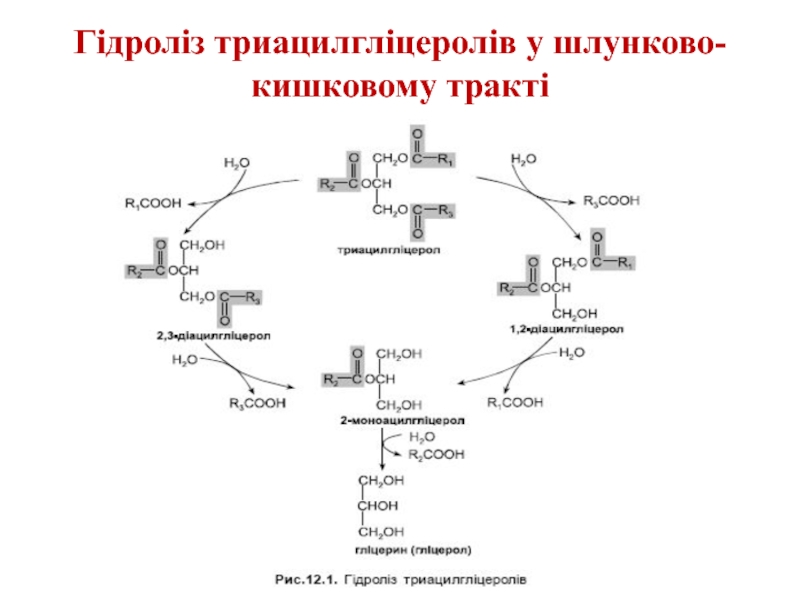
- 9. Гідроліз триацилгліцеролів у шлунково- кишковому тракті
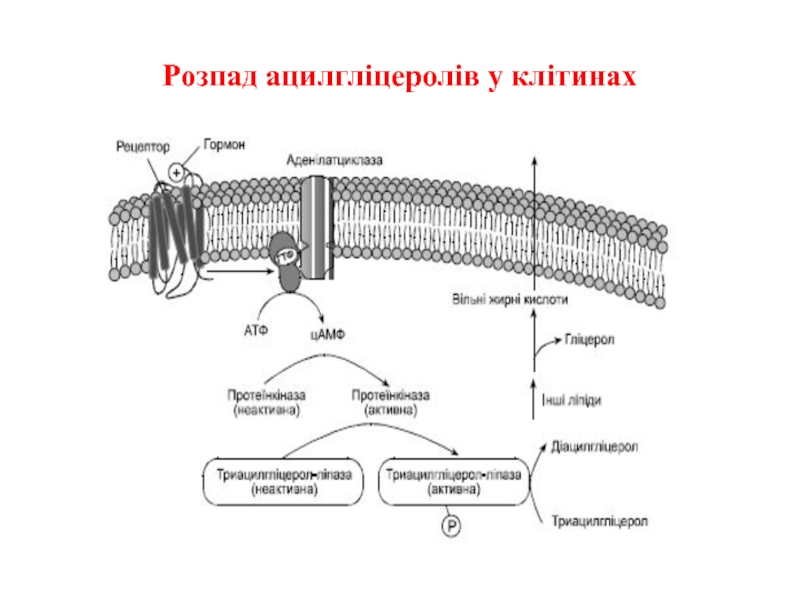
- 11. Розпад ацилгліцеролів у клітинах
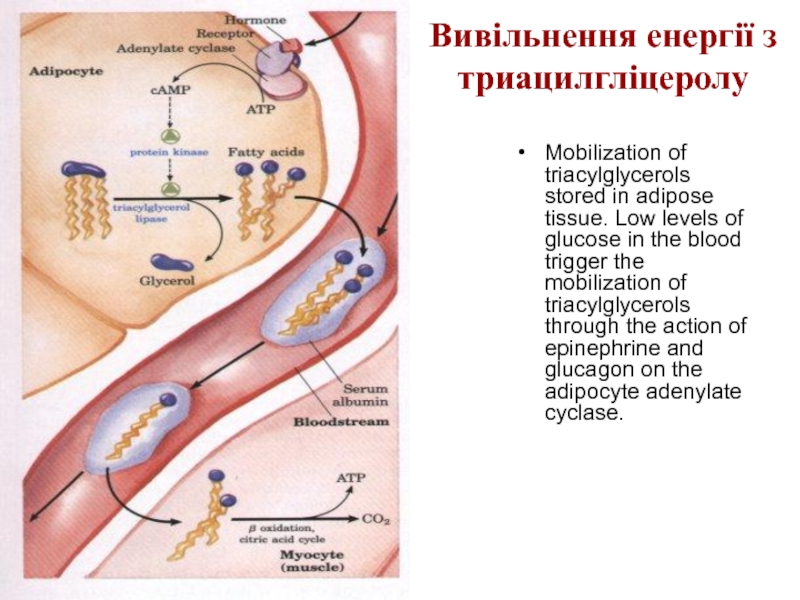
- 12. Вивільнення енергії з триацилгліцеролу Mobilization of triacylglycerols
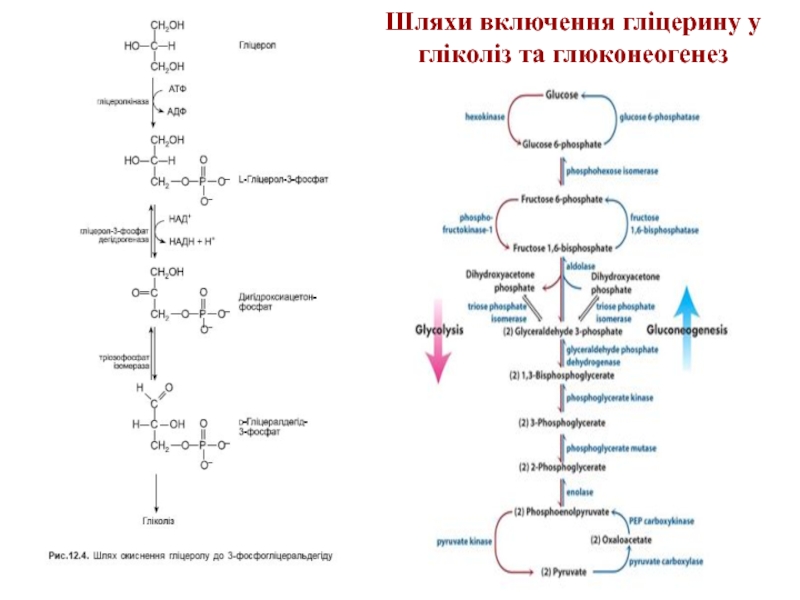
- 13. Шляхи включення гліцерину у гліколіз та глюконеогенез
- 14. β-окиснення жирних кислот
- 15. Stages of fatty acid oxidation. Stage 1:
- 16. β-окиснення жирних кислот
- 17. Активація жирних кислот Fatty acid activation by
- 18. Проникнення жирних кислот через мембрану мітохондрії
- 19. Проникнення жирних кислот через мембрану мітохондрії
- 20. Транспорт жирних кислот через внутрішню мембрану мітохондрій
- 21. Карнітин
- 22. Проникнення жирних кислот через мембрану мітохондрії
- 23. Стадія дегідрування
- 24. Стадія гідратації
- 25. Друга стадія дегідрування
- 26. Тіолазна реакція
- 27. β-окислення The fatty acid oxidation (β-oxidation) pathway.
- 28. Енергетичний баланс
- 29. Енергетичний баланс
- 32. Окислення ненасичених жирних
- 33. Окислення ненасичених жирних кислот Oxidation of polyunsaturated
- 34. Кетонові тіла
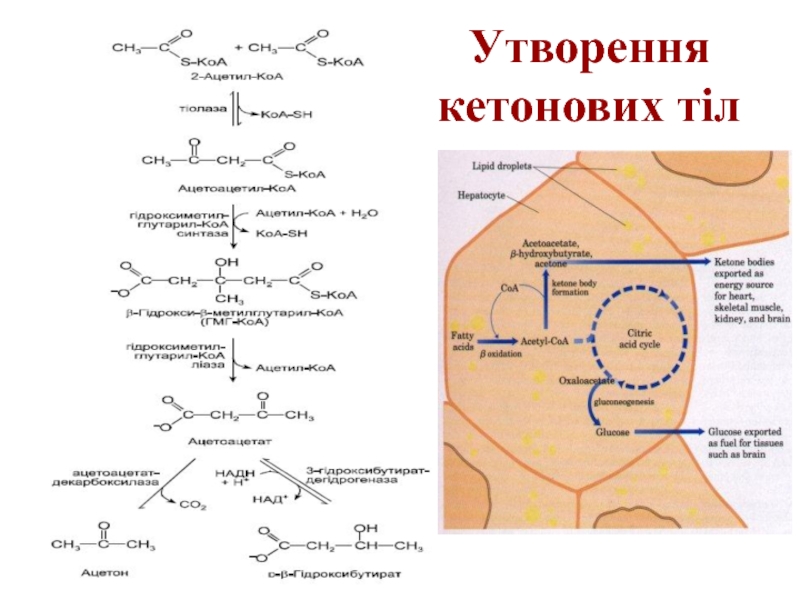
- 35. Утворення кетонових тіл
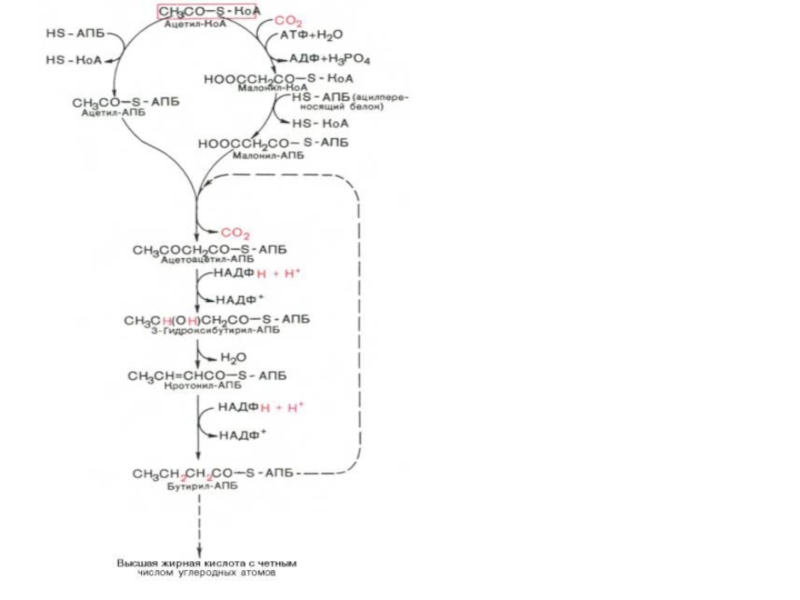
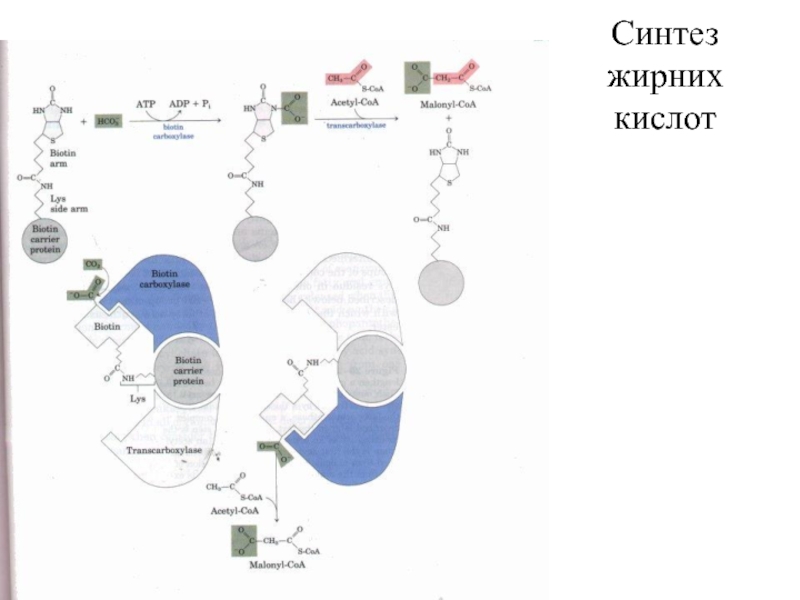
- 36. Синтез жирних кислот
- 37. Синтез жирних кислот
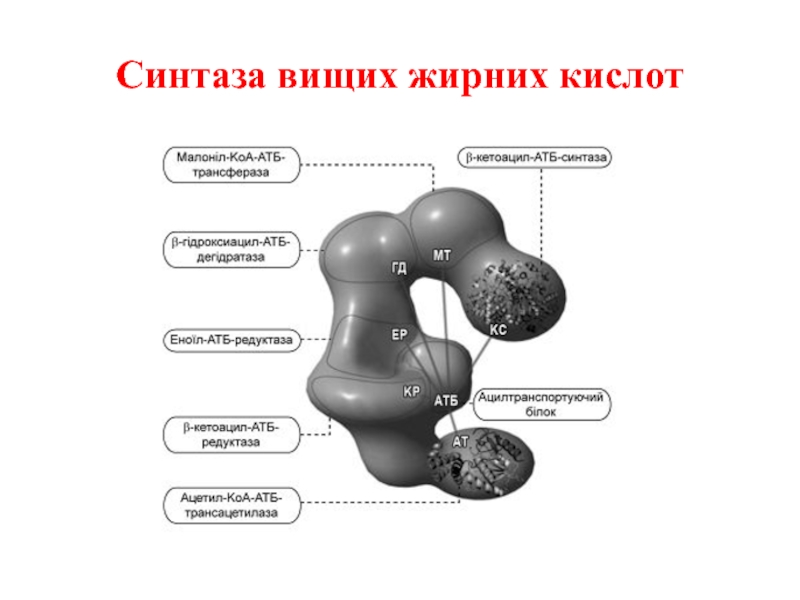
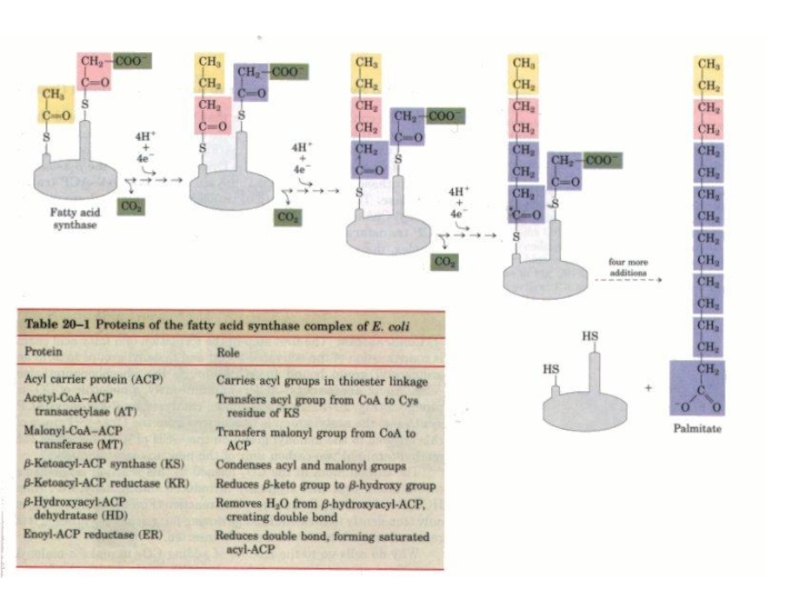
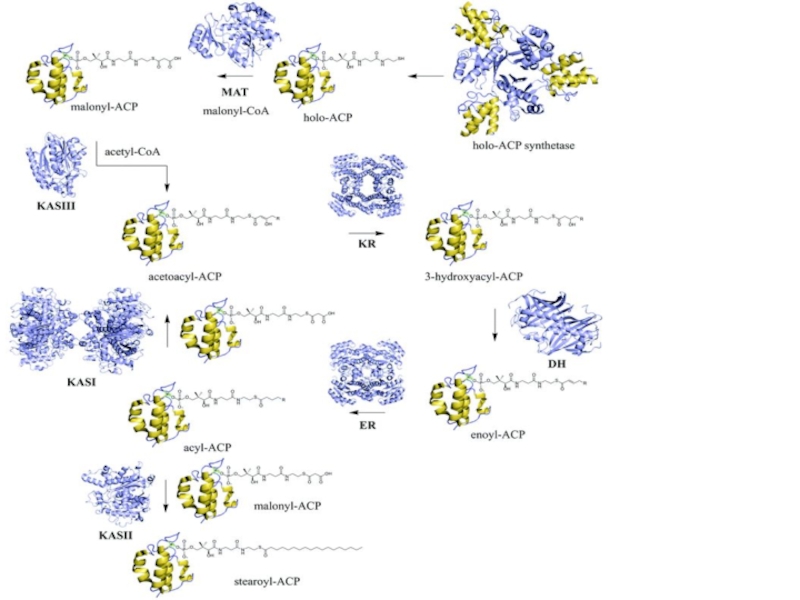
- 38. Синтаза вищих жирних кислот
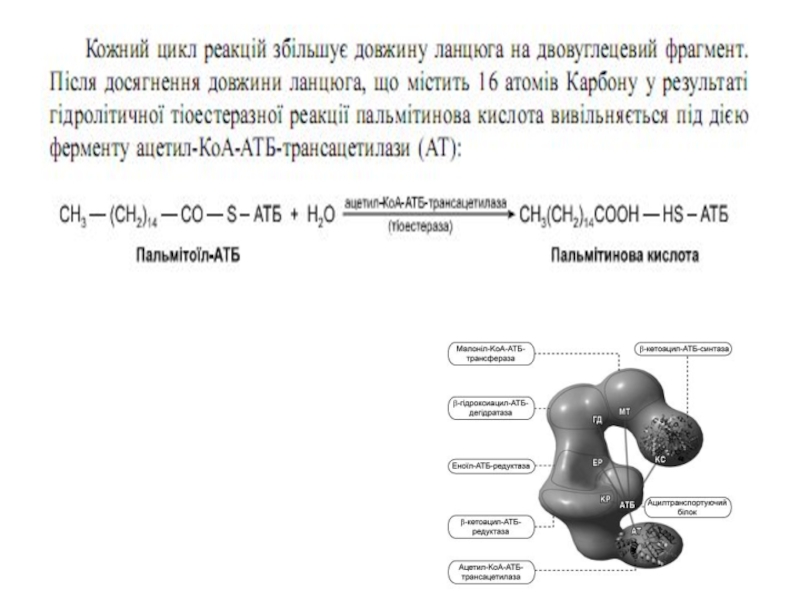
- 47. Сумарне рівняння синтезу жирних кислот Із пальмітинової
- 48. Синтез жирних кислот Утворений
- 51. Позамітохондріальна система біосинтезу жирних кислот
- 52. Утворення ненасичених жирних кислот
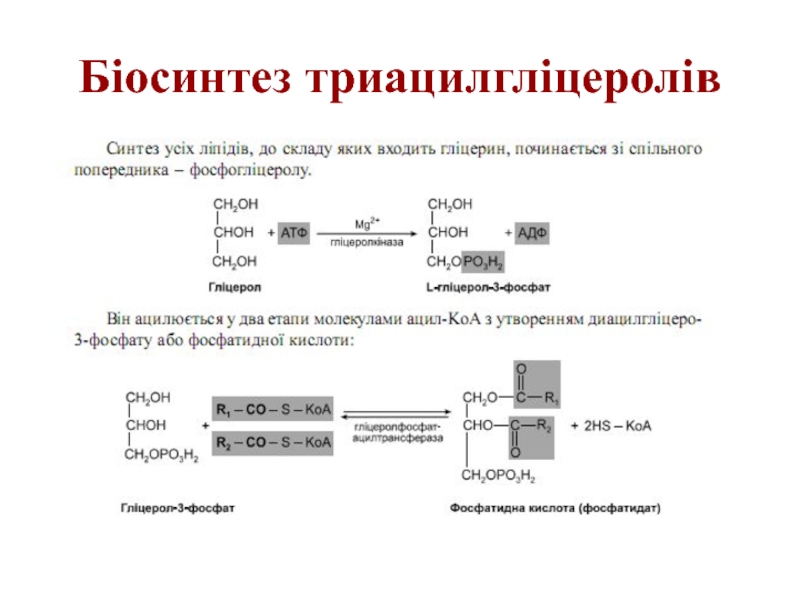
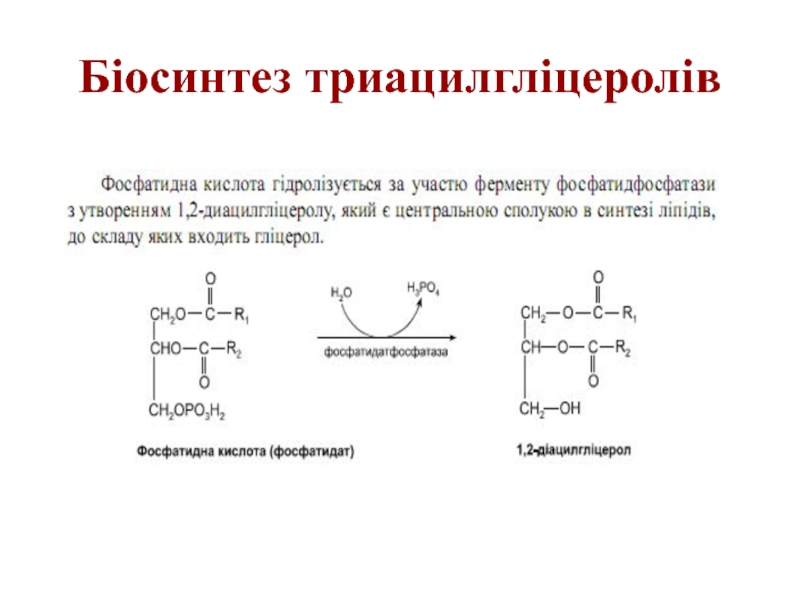
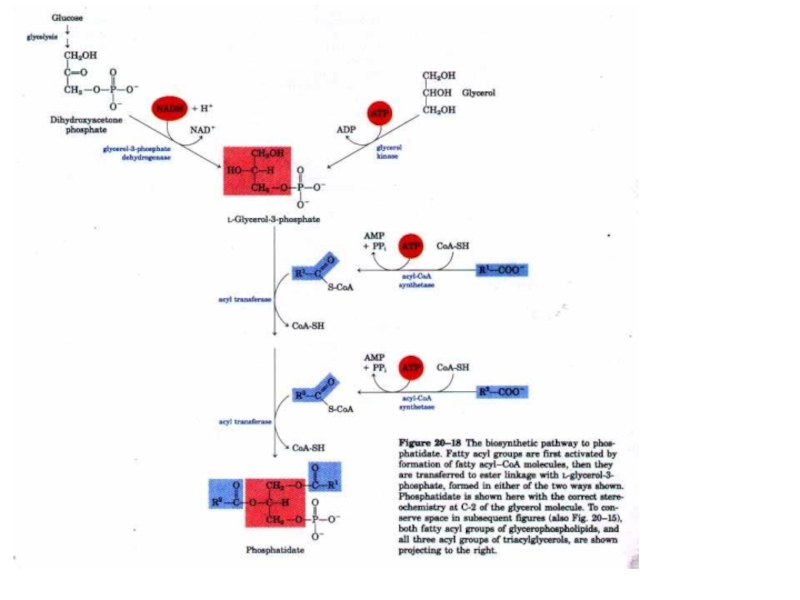
- 53. Біосинтез триацилгліцеролів
- 54. Біосинтез триацилгліцеролів
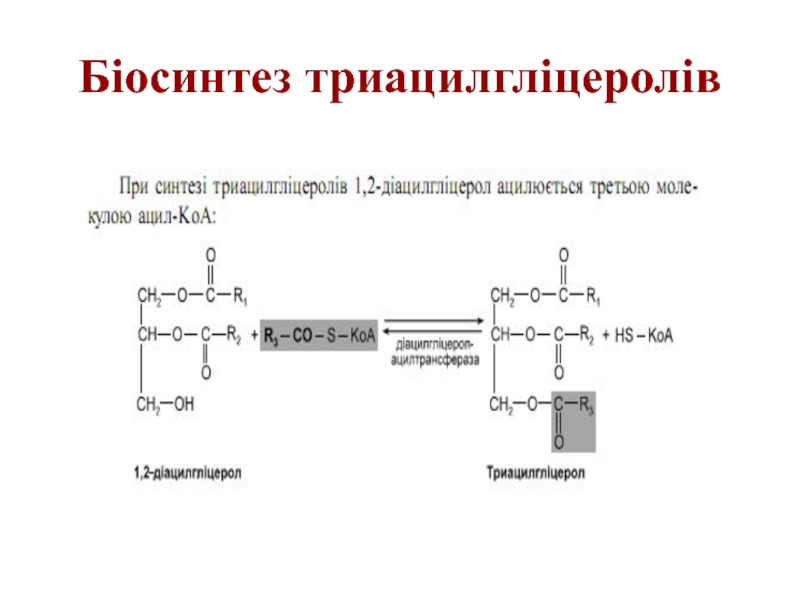
- 55. Біосинтез триацилгліцеролів
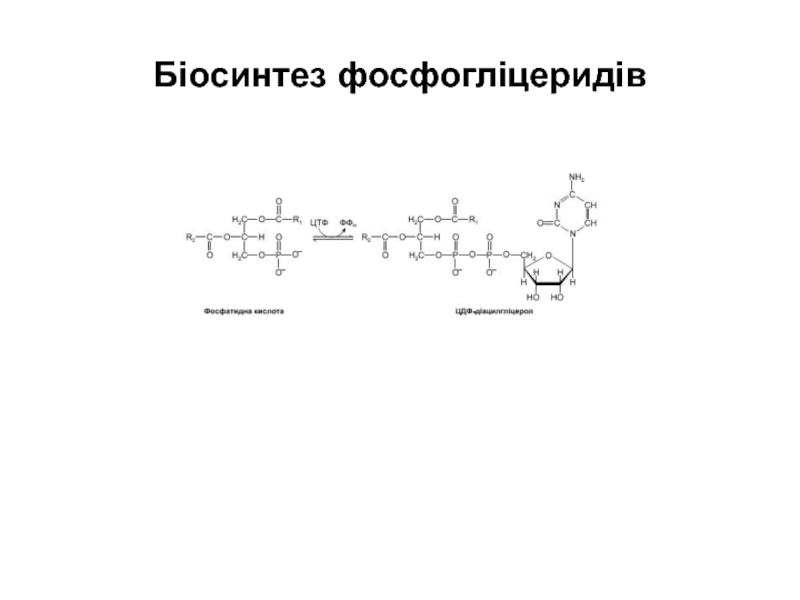
- 56. Біосинтез фосфогліцеридів
- 57. Біосинтез фосфогліцеридів
- 58. Біосинтез фосфогліцеридів
- 59. Біосинтез фосфогліцеридів
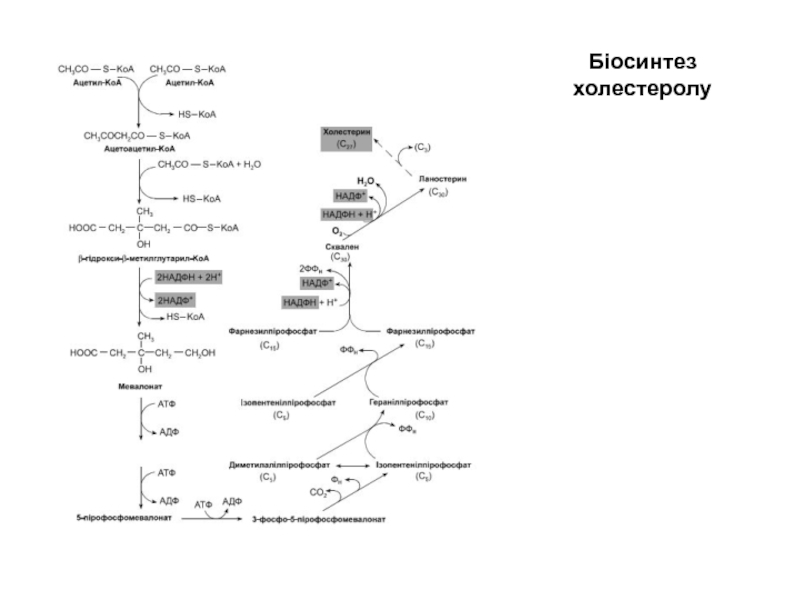
- 60. Біосинтез холестеролу
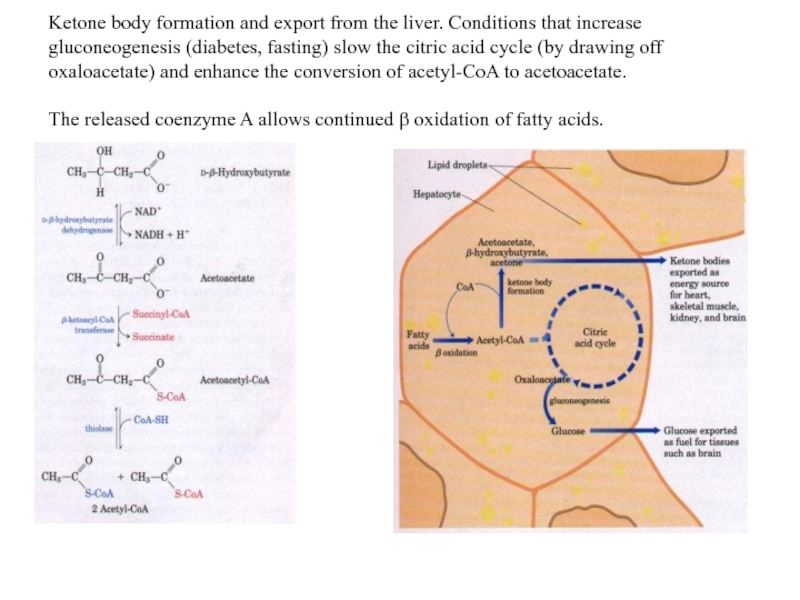
- 63. Ketone body formation and export from the
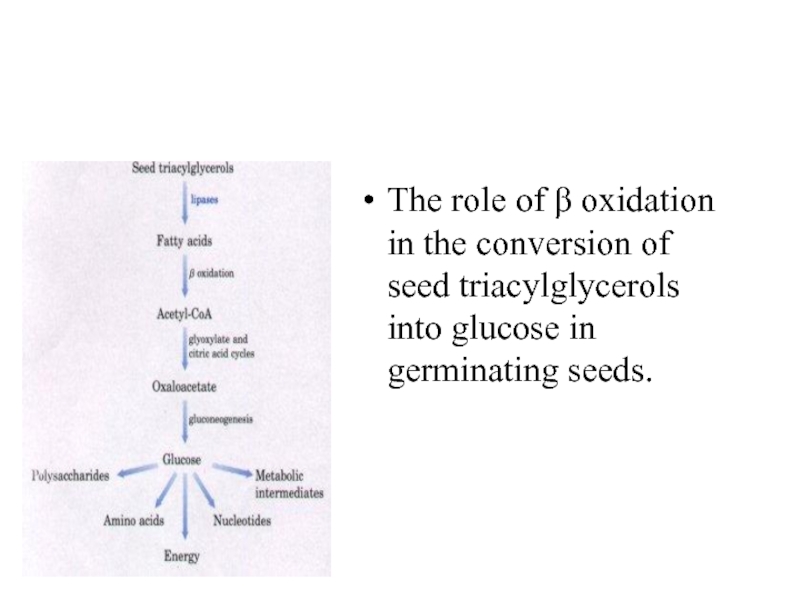
- 64. The role of β oxidation in
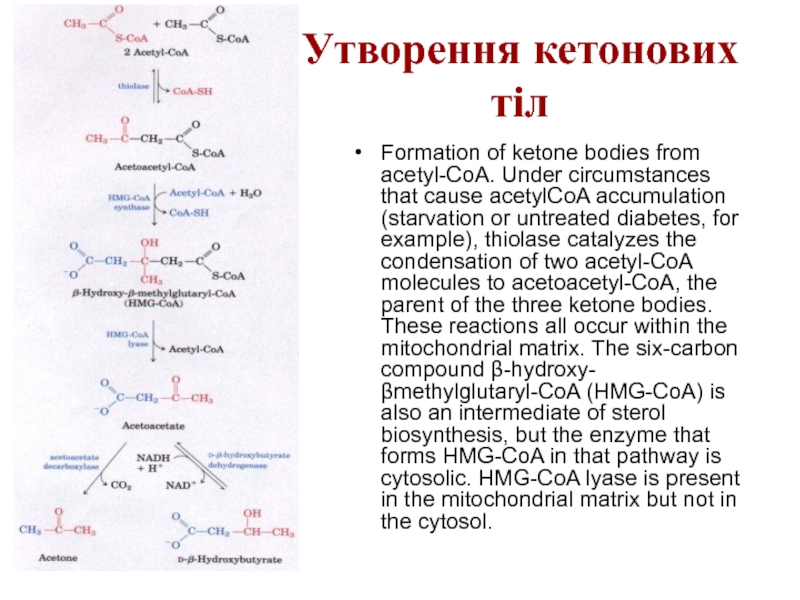
- 65. Утворення кетонових тіл Formation of ketone bodies
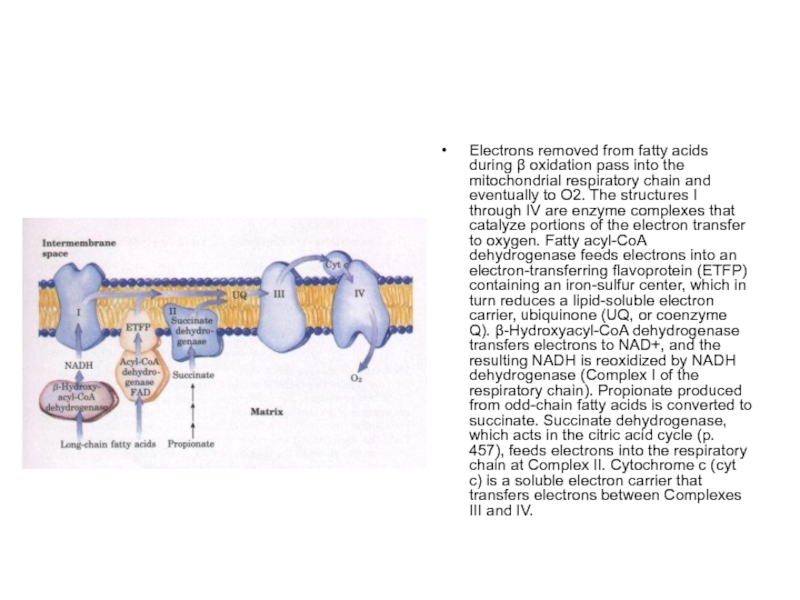
- 66. Electrons removed from fatty acids during
- 68. Синтез жирних кислот
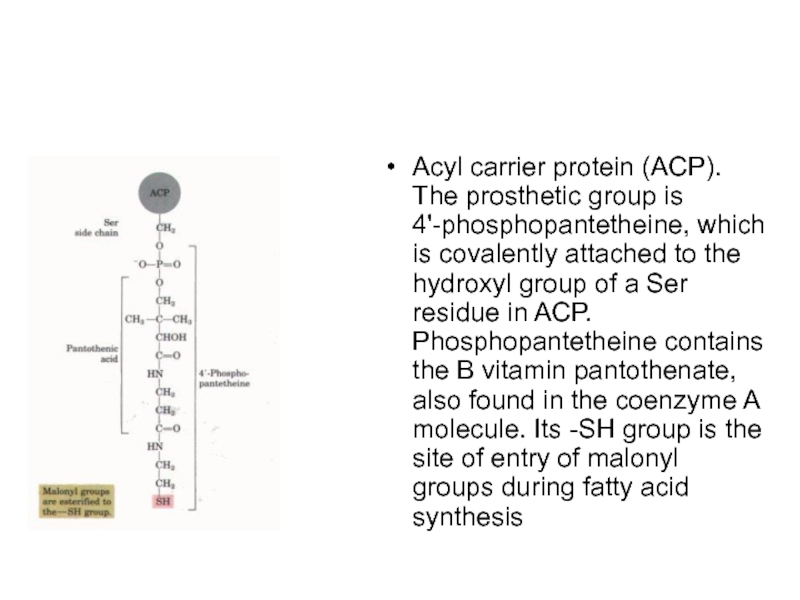
- 69. Acyl carrier protein (ACP). The prosthetic
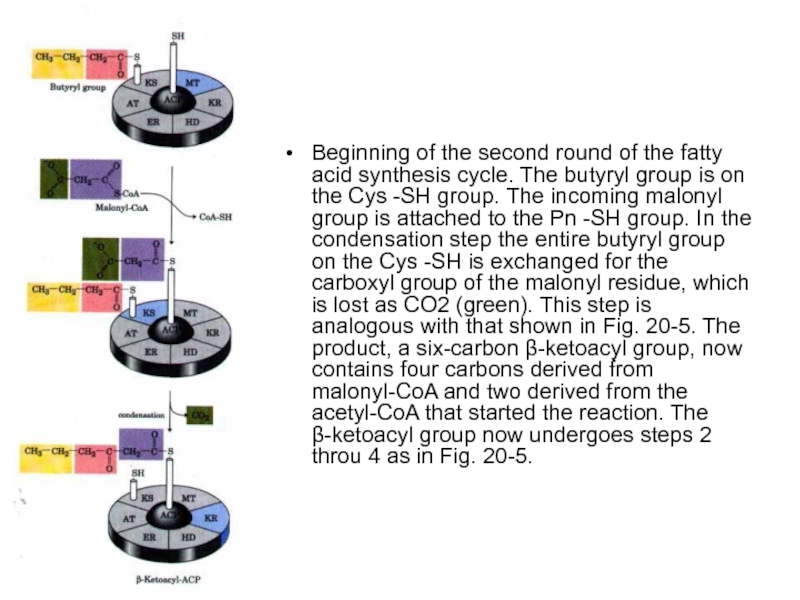
- 71. Beginning of the second round of
- 72. The acetyl group shuttle for transfer
- 73. Regulation of fatty acid synthesis. (a)
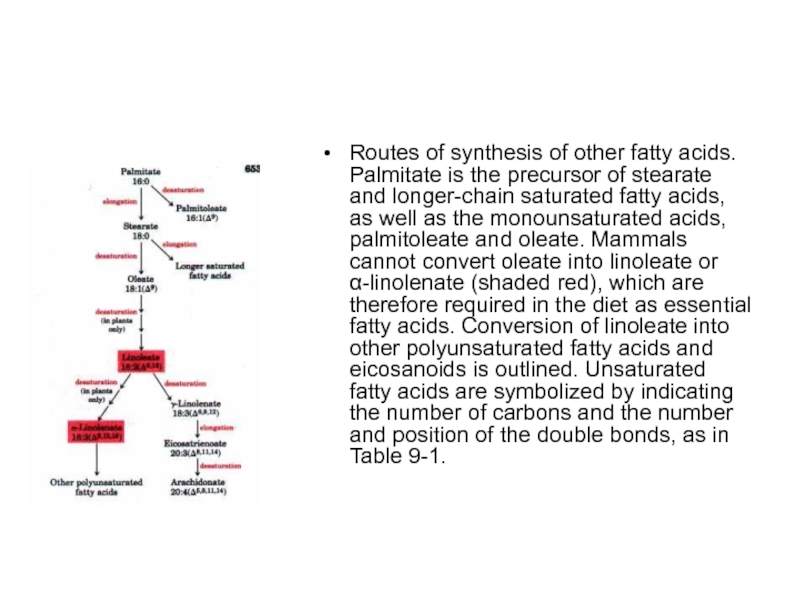
- 74. Routes of synthesis of other fatty
- 77. Schematic
Слайд 3План лекції
1.Травлення ліпідів у кишково-шлунковому тракті
2.Розпад ліпідів у клітинах організму.
3.Окиснення жирних
4.Утворення кетонових тіл.
5.Біосинтез жирних кислот.
6.Біосинтез триацилгліцеролів.
Слайд 5Запас енергетичних ресурсів у організмі людини
Energy is stored in the body
Слайд 7Uptake of dietary lipid in the intestine of a vertebrate animal,
Слайд 8Молекулярна структура хіломікронів
Molecular structure of a chylomicron. The surface is covered
Слайд 12Вивільнення енергії з триацилгліцеролу
Mobilization of triacylglycerols stored in adipose tissue. Low
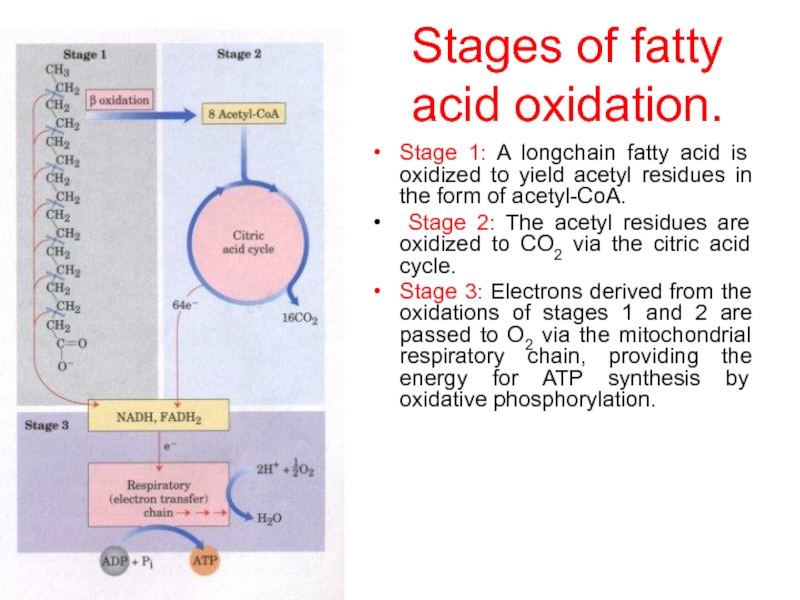
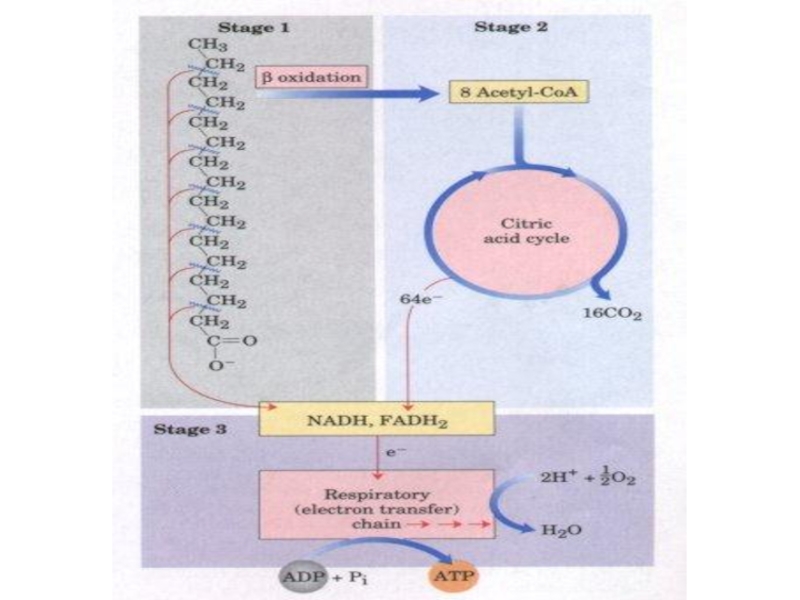
Слайд 15Stages of fatty acid oxidation.
Stage 1: A longchain fatty acid is
Stage 2: The acetyl residues are oxidized to CO2 via the citric acid cycle.
Stage 3: Electrons derived from the oxidations of stages 1 and 2 are passed to O2 via the mitochondrial respiratory chain, providing the energy for ATP synthesis by oxidative phosphorylation.
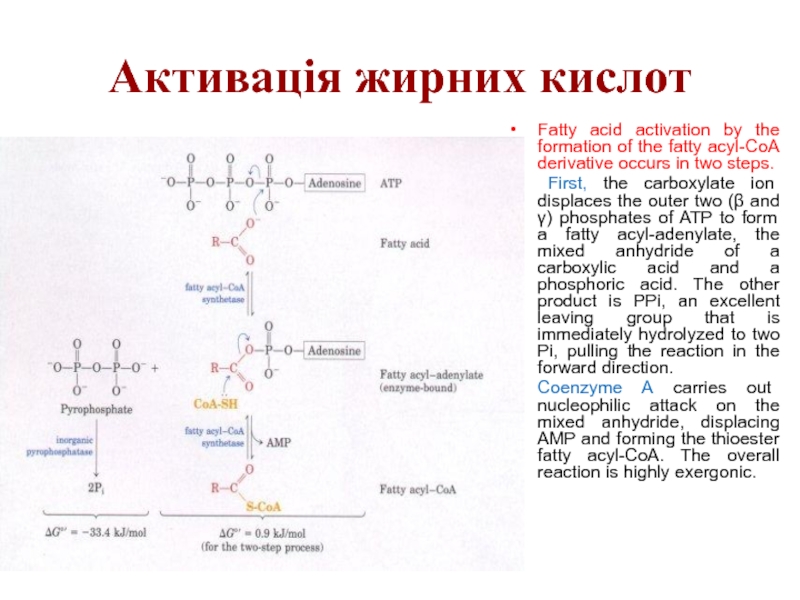
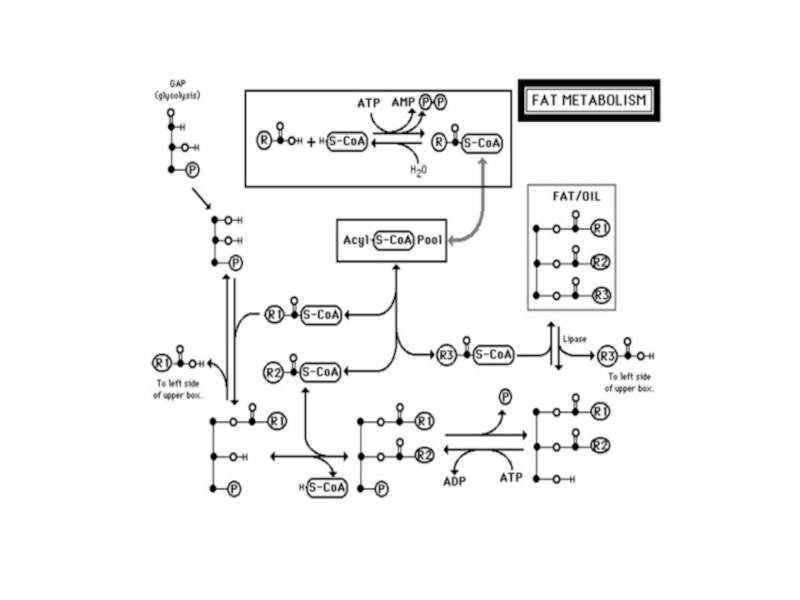
Слайд 17Активація жирних кислот
Fatty acid activation by the formation of the fatty
First, the carboxylate ion displaces the outer two (β and γ) phosphates of ATP to form a fatty acyl-adenylate, the mixed anhydride of a carboxylic acid and a phosphoric acid. The other product is PPi, an excellent leaving group that is immediately hydrolyzed to two Pi, pulling the reaction in the forward direction.
Coenzyme A carries out nucleophilic attack on the mixed anhydride, displacing AMP and forming the thioester fatty acyl-CoA. The overall reaction is highly exergonic.
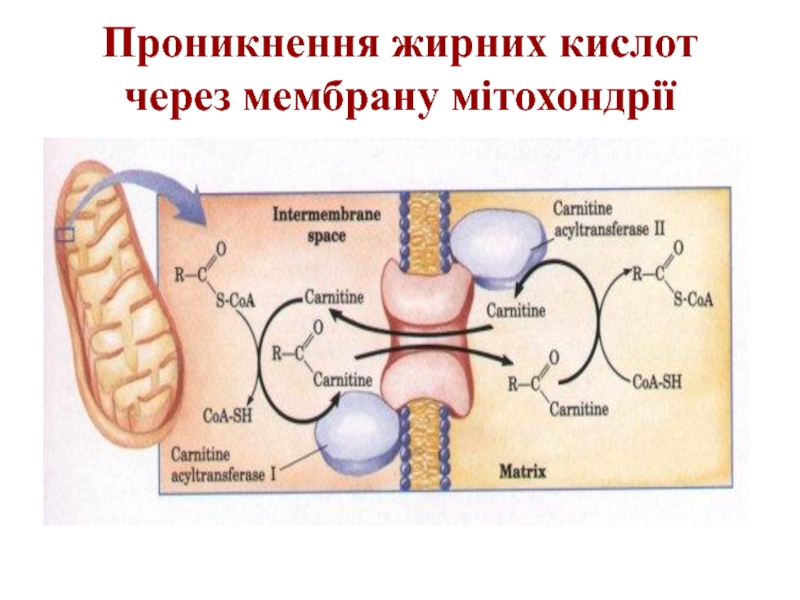
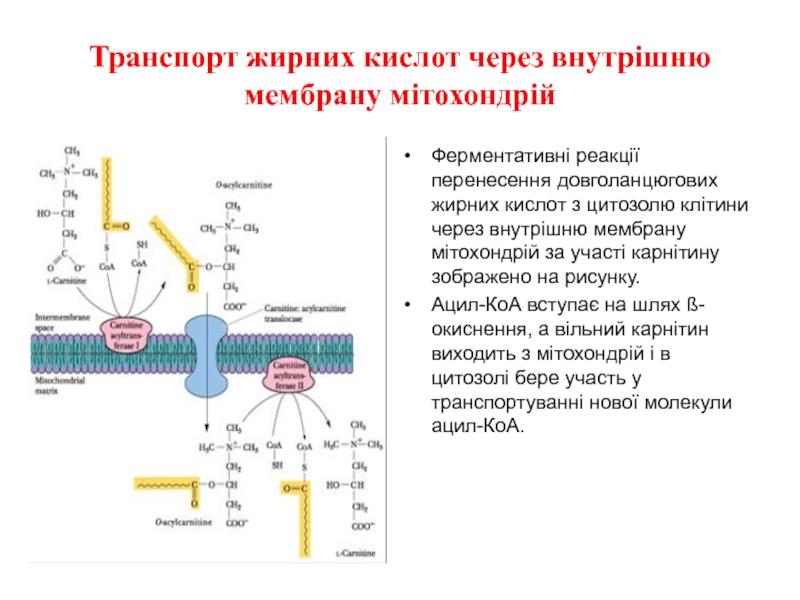
Слайд 20Транспорт жирних кислот через внутрішню мембрану мітохондрій
Ферментативні реакції перенесення довголанцюгових жирних
Ацил-КоА вступає на шлях ß-окиснення, а вільний карнітин виходить з мітохондрій і в цитозолі бере участь у транспортуванні нової молекули ацил-КоА.
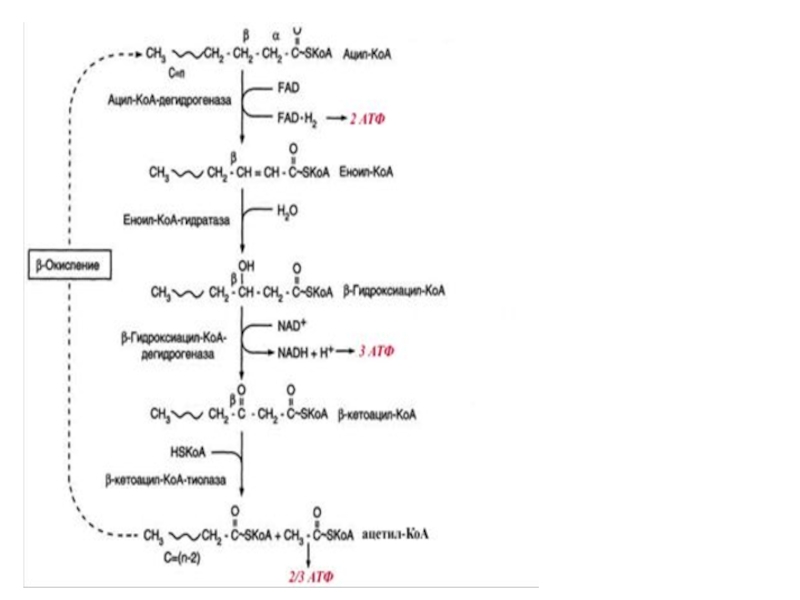
Слайд 27β-окислення
The fatty acid oxidation (β-oxidation) pathway.
(a) In each pass through
(b) Six more passes through the pathway yield seven more molecules of acetyl-CoA, the seventh arising from the last two carbon atoms of the 16-carbon chain. Eight molecules of acetyl-CoA are formed in all.
Слайд 28Енергетичний баланс
Якщо жирна кислота містить n атомів карбону, то за повного її окиснення утворюється (n : 2 ) молекул ацетил-KоА ( кожний ацетил містить два атоми карбону ) та (n : 2 ) – 1 молекул ФАДН2 і НАДH(Н+), оскільки за останнього циклу окиснення утворюються дві молекули ацетил-KоА, але по одній молекулі ФАДH2 і НАДH (Н+).
Отже продуктами окиснення жирної кислоти з парним числом атомів карбону є: ацетил-КоА, ФАДH2 і НАДH(Н+). В подальшому ацетил-KоА вступає в ЦТК, а ФАДH2 і НАДH (Н+) – безпосередньо в дихальний ланцюг.
За кожного циклу β-окиснення утворюється : 1 молекула ФАДH2 і 1 молекула НАДH(Н+). Останні у процесі окиснення в дихальному ланцюзі та спряженого з ним фосфорилювання дають: ФАДH2 (через KoQ) – 2 молекули АТФ, а НАДH(Н+) – 3 молекули АТФ,
тобто сумарно за один цикл утворюються 5 молекул АТФ.
Слайд 29Енергетичний баланс
У випадку пальмітинової кислоти (С 16) відбувається 7 циклів β-окиснення:
пальмітоїл-KоА + 7ФАД + 7НАД+ + 7Н2O + 7HS-KoA = 8ацетил-KоА + 7ФАДН2 + 7НАДН + 7Н+
Оскільки за окиснення жирної кислоти, яка містить n(16) атомів карбону, відбувається (n : 2) – 1 = (16:2)-1= 7 циклів β-окиснення, це призводить до утворення: 5 × 7 = 35 молекул АТФ.
У процесі β-окиснення пальмітинової кислоти утворюються 8 молекул ацетил-КоА (n:2)=(16:2)=8, кожна з яких, згораючи в циклі трикарбонових кислот, дає 12 молекул АТФ. Отже 12 × 8=96 молекул АТФ. Таким чином усього за повного β-окиснення пальмітинової кислоти утворюється:
35 + 96 = 131 молекула АТФ.
Одна молекула АТФ витрачається на активацію жирної кислоти, тому баланс АТФ при повному окисненні пальмітинової кислоти складає 131 – 1= 130 молекул АТФ.
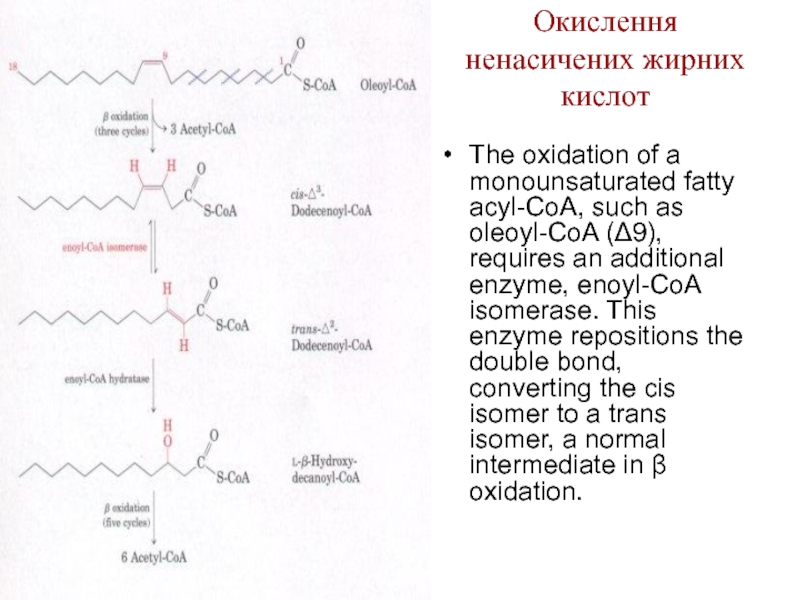
Слайд 32Окислення ненасичених жирних
The oxidation of a monounsaturated fatty acyl-CoA, such as oleoyl-CoA (Δ9), requires an additional enzyme, enoyl-CoA isomerase. This enzyme repositions the double bond, converting the cis isomer to a trans isomer, a normal intermediate in β oxidation.
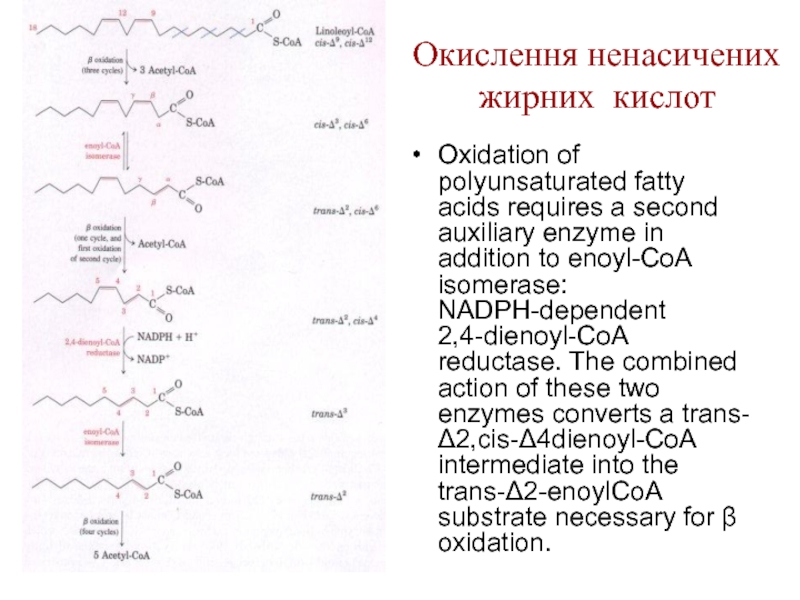
Слайд 33Окислення ненасичених жирних кислот
Oxidation of polyunsaturated fatty acids requires a second
Слайд 47Сумарне рівняння синтезу жирних кислот
Із пальмітинової кислоти синтезується стеаринова і інші
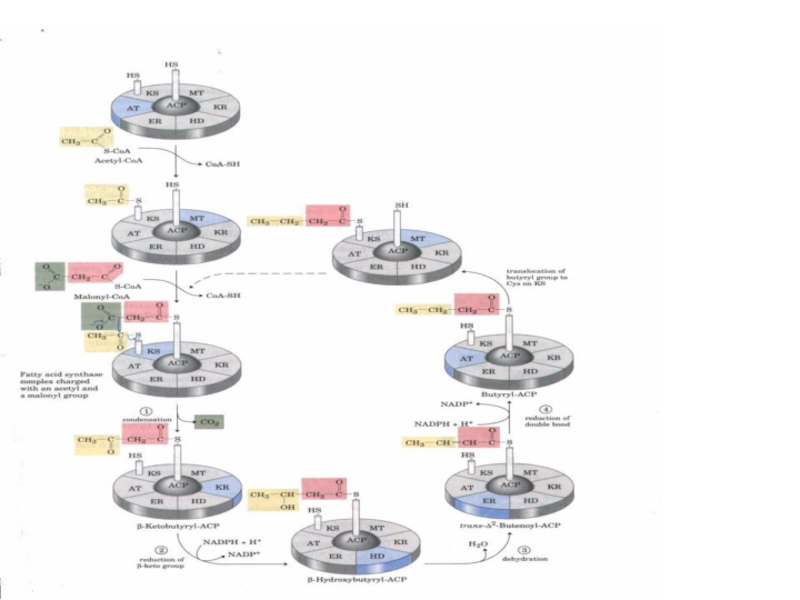
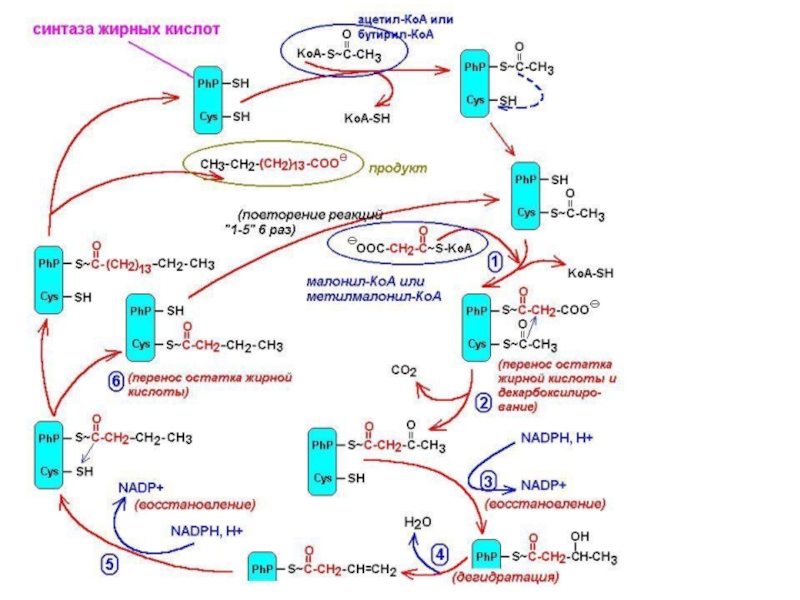
Слайд 48Синтез жирних кислот
Утворений малоніл~KоА взаємодіє з АТБ-SH під
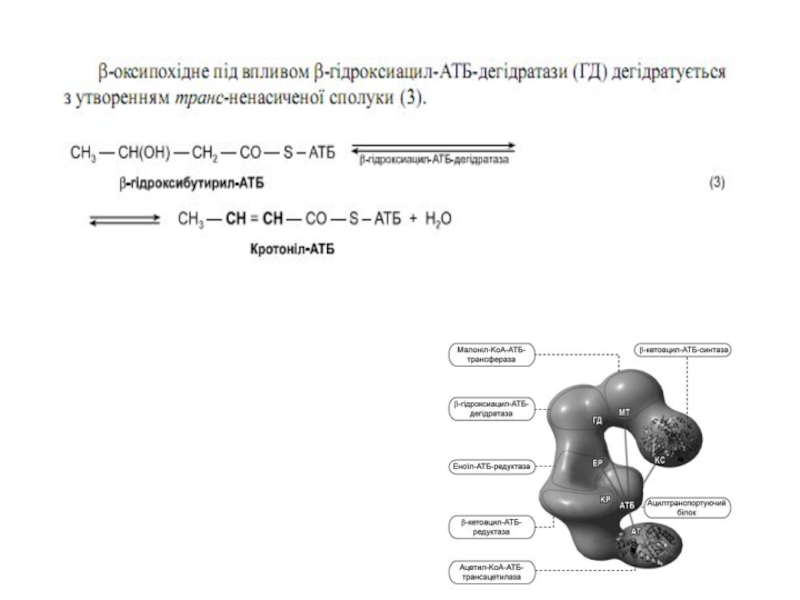
хідного під впливом 3-кетоацил-АТБ-редуктази. Донором гідрогену для цієї реакці є НАДФH(Н+). β-оксипохідне під впливом β -гідроксиацил-АТБ-дегідратази дегідра-
тується з утворенням транс-ненасиченої сполуки , яка, у свою чергу, відновлюється за рахунок НАДФH(Н+) під впливом ферменту еноїл-АТБ-редуктази. Таким чином з двох окиснених двовуглецевих фрагментів синтезується відновний чотиривуглецевий-бутирил-АТБ. Він переноситься з АТБ на залишок цистеїну ферменту.
Слайд 51
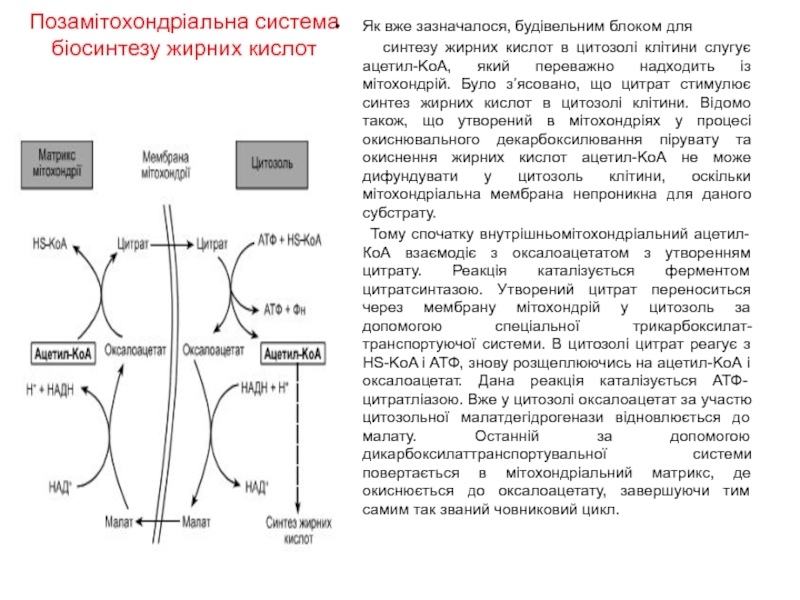
Позамітохондріальна система
біосинтезу жирних кислот
Як вже зазначалося, будівельним блоком для
Тому спочатку внутрішньомітохондріальний ацетил-КоА взаємодіє з оксалоацетатом з утворенням цитрату. Реакція каталізується ферментом цитратсинтазою. Утворений цитрат переноситься через мембрану мітохондрій у цитозоль за допомогою спеціальної трикарбоксилат-транспортуючої системи. В цитозолі цитрат реагує з HS-KoA і АТФ, знову розщеплюючись на ацетил-KоА і оксалоацетат. Дана реакція каталізується АТФ-цитратліазою. Вже у цитозолі оксалоацетат за участю цитозольної малатдегідрогенази відновлюється до малату. Останній за допомогою дикарбоксилаттранспортувальної системи повертається в мітохондріальний матрикс, де окиснюється до оксалоацетату, завершуючи тим самим так званий човниковий цикл.
Слайд 63Ketone body formation and export from the liver. Conditions that increase
Слайд 64
The role of β oxidation in the conversion of seed triacylglycerols
Слайд 65Утворення кетонових тіл
Formation of ketone bodies from acetyl-CoA. Under circumstances that
Слайд 66
Electrons removed from fatty acids during β oxidation pass into the
Слайд 69
Acyl carrier protein (ACP). The prosthetic group is 4'-phosphopantetheine, which is
Слайд 71
Beginning of the second round of the fatty acid synthesis cycle.
Слайд 72
The acetyl group shuttle for transfer of acetyl groups from mitochondria
Слайд 73
Regulation of fatty acid synthesis. (a) In the cells of vertebrates,
Слайд 74
Routes of synthesis of other fatty acids. Palmitate is the precursor
Слайд 77
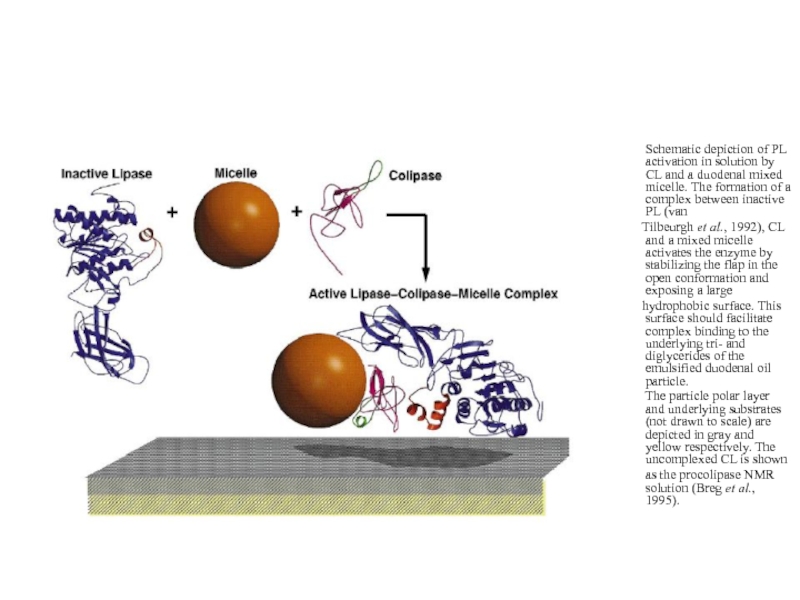
Schematic depiction of PL activation in
Tilbeurgh et al., 1992), CL and a mixed micelle activates the enzyme by stabilizing the flap in the open conformation and exposing a large
hydrophobic surface. This surface should facilitate complex binding to the underlying tri- and diglycerides of the emulsified duodenal oil particle.
The particle polar layer and underlying substrates (not drawn to scale) are depicted in gray and yellow respectively. The uncomplexed CL is shown
as the procolipase NMR solution (Breg et al., 1995).