- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Обмен липидов. Регуляция обмена липидов. Регуляция окисления и синтеза ЖК. (Тема 4) презентация
Содержание
- 1. Обмен липидов. Регуляция обмена липидов. Регуляция окисления и синтеза ЖК. (Тема 4)
- 2. ПЛАН ЛЕКЦИИ 1. Регуляция обмена липидов. Регуляция
- 3. Регуляция обмена липидов Интенсивность обмена липидов в
- 4. . Вместе с тем,
- 5. Нервно-гормональная регуляция липидного
- 6. . В такой форме данный рецептор способен
- 8. Окисление и синтез ЖК регулируется: а) разделением
- 9. БИОСИНТЕЗ ТРИГЛИЦЕРИДОВ Синтез триглицеридов происходит из глицерина
- 10. В почках, а также в стенке кишечника,
- 11. В жировой ткани и мышцах вследствие очень
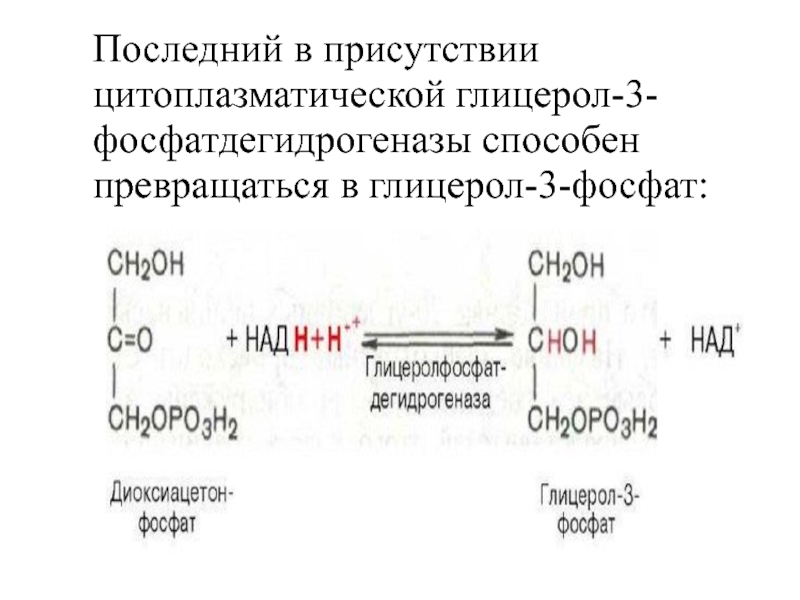
- 12. Последний в присутствии цитоплазматической глицерол-3-фосфатдегидрогеназы способен превращаться в глицерол-3-фосфат:
- 13. Если содержание глюкозы в жировой ткани понижено
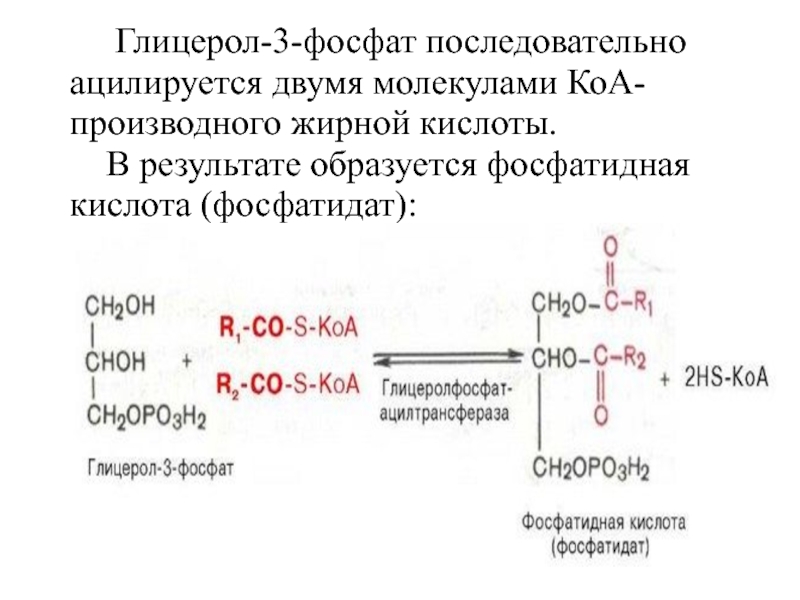
- 14. Глицерол-3-фосфат последовательно ацилируется двумя
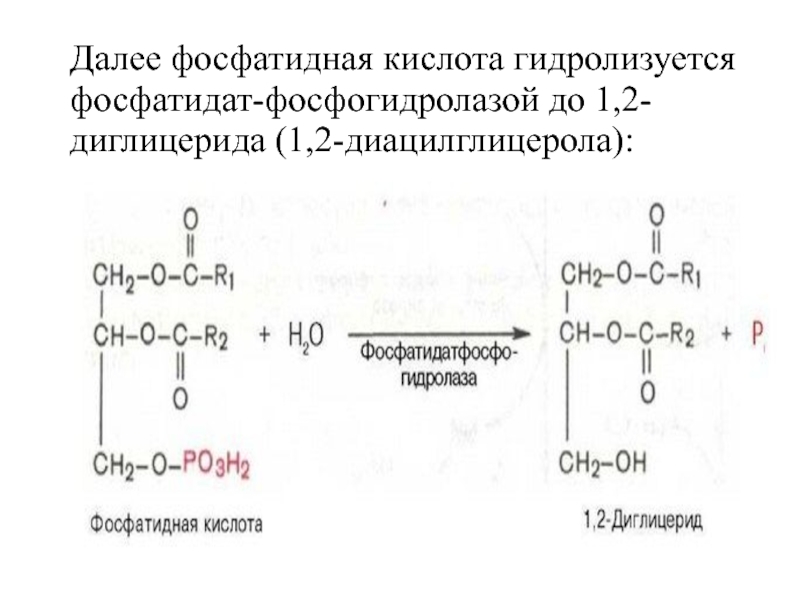
- 15. Далее фосфатидная кислота гидролизуется фосфатидат-фосфогидролазой до 1,2-диглицерида (1,2-диацилглицерола):
- 16. Затем 1,2-диглицерид ацилируется третьей молекулой ацил-КоА и превращается в триглицерид (триацилглицерол). Эта реакция катализируется диацилглицерол-ацилтрансферазой:
- 17. Синтез триглицеридов (триацилглицеролов)
- 18. БИОСИНТЕЗ ХОЛЕСТЕРИНА В синтезе холестерина можно выделить
- 19. Превращение активного ацетата в мевалоновую кислоту
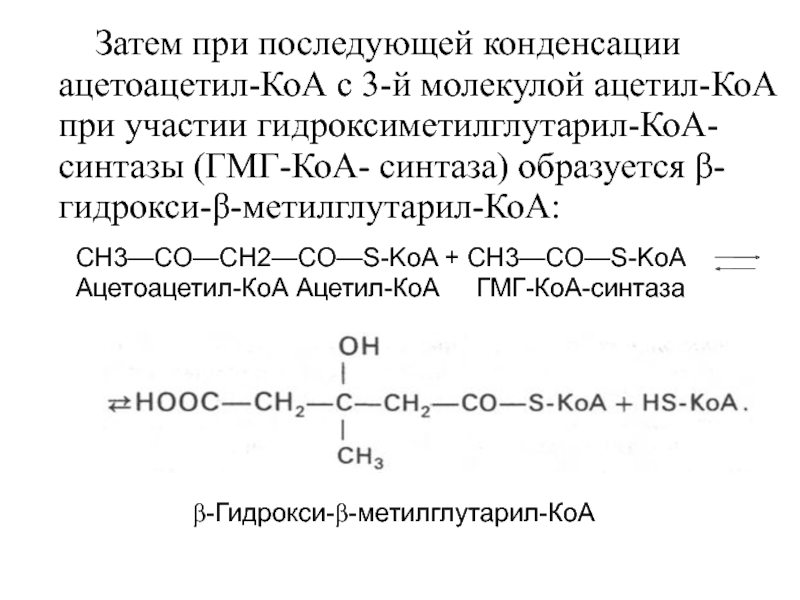
- 20. Затем при последующей конденсации ацетоацетил-КоА
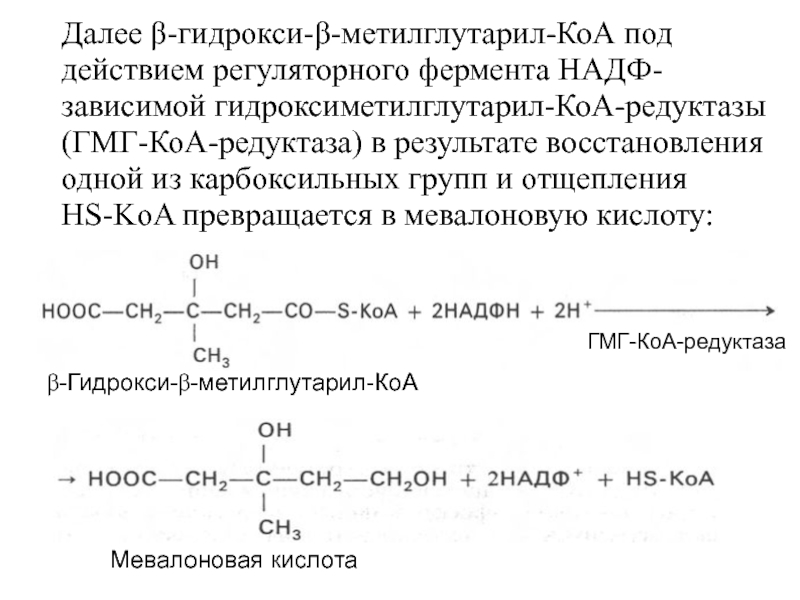
- 21. Далее β-гидрокси-β-метилглутарил-КоА под действием регуляторного фермента НАДФ-зависимой
- 22. На II стадии синтеза холестерина
- 23. 5-пирофосфомевалоновая кислота в результате последующего фосфорилирования третичной
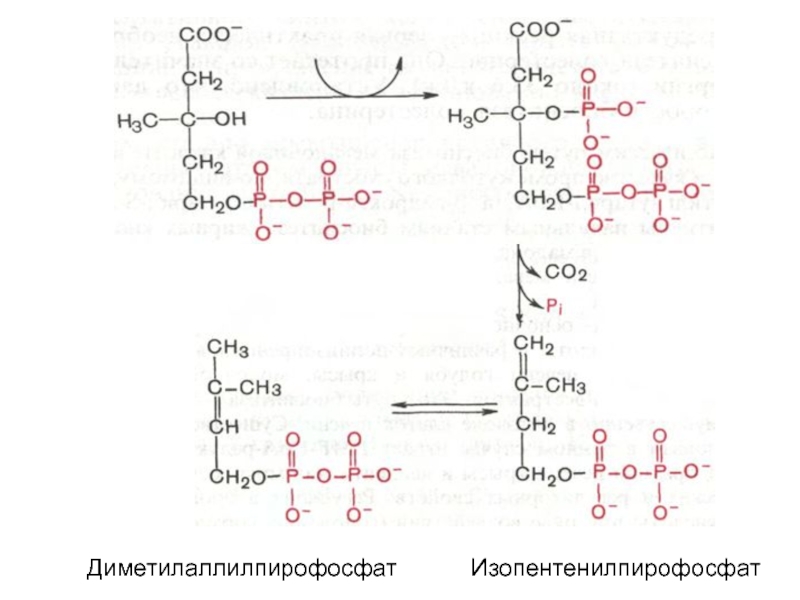
- 24. Диметилаллилпирофосфат Изопентенилпирофосфат
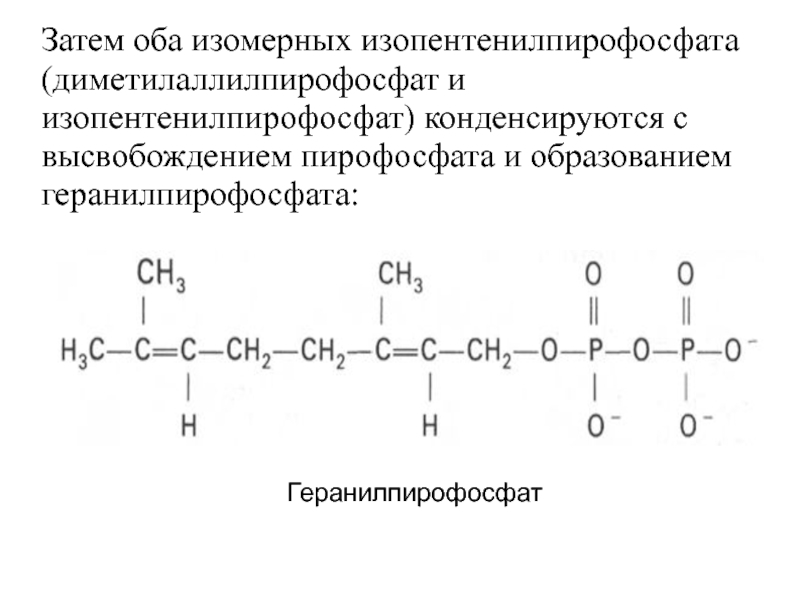
- 25. Затем оба изомерных изопентенилпирофосфата (диметилаллилпирофосфат и изопентенилпирофосфат) конденсируются с высвобождением пирофосфата и образованием геранилпирофосфата: Геранилпирофосфат
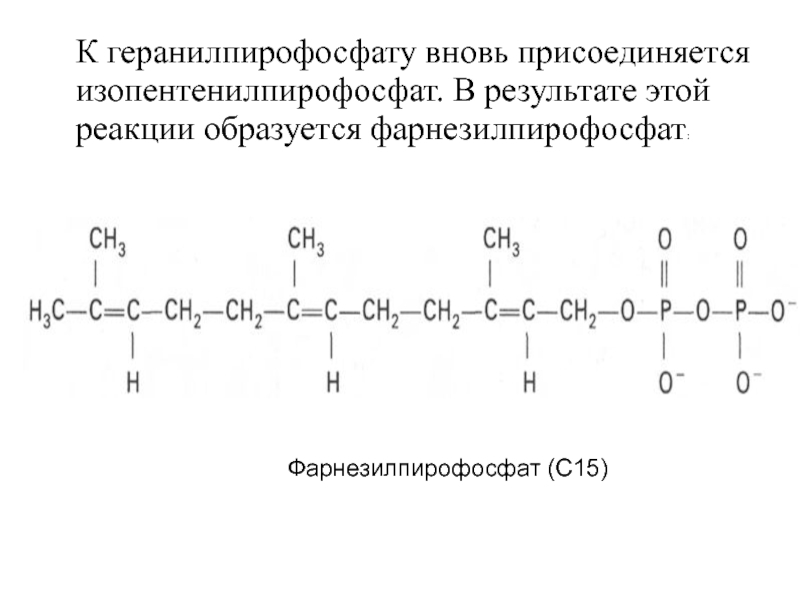
- 26. К геранилпирофосфату вновь присоединяется изопентенилпирофосфат. В результате этой реакции образуется фарнезилпирофосфат: Фарнезилпирофосфат (С15)
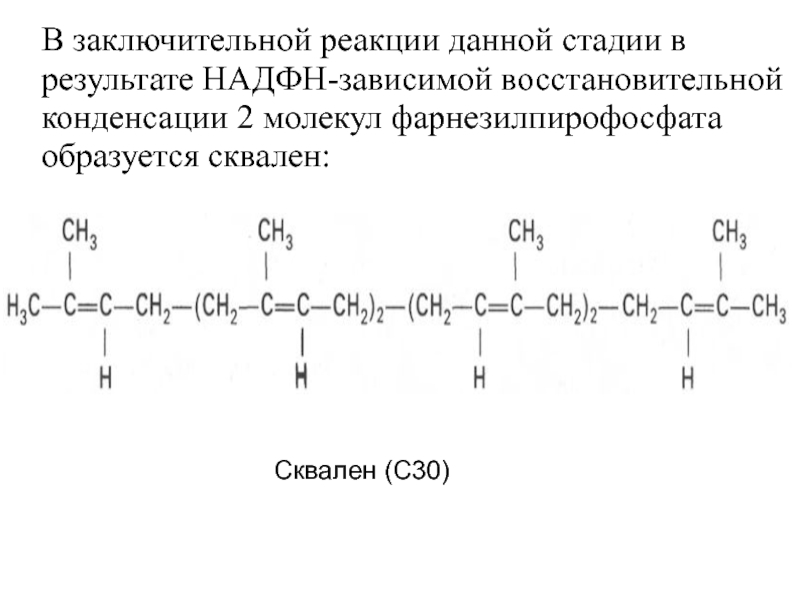
- 27. В заключительной реакции данной стадии в результате
- 28. На III стадии биосинтеза
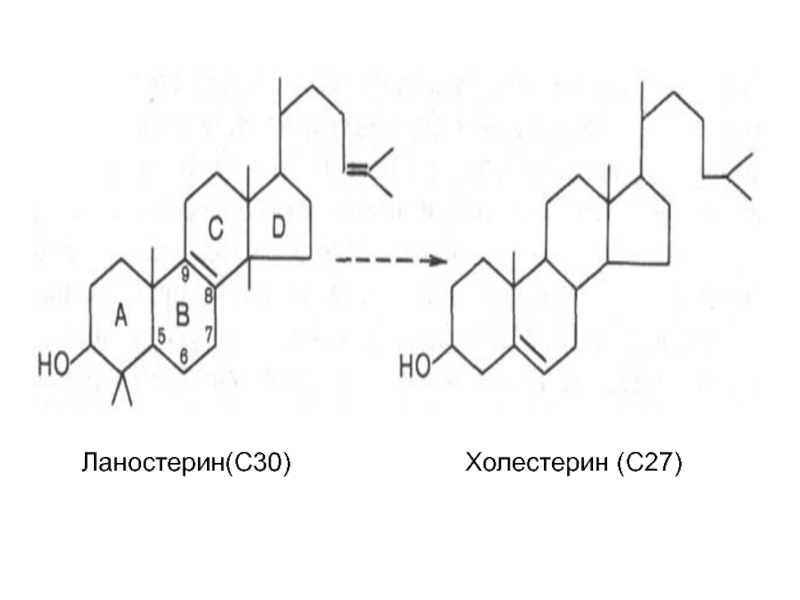
- 29. Ланостерин(С30) Холестерин (С27)
- 30. Начиная со сквалена, все промежуточные продукты биосинтеза
- 31. Реакцией, регулирующей скорость биосинтеза
Слайд 2ПЛАН ЛЕКЦИИ
1. Регуляция обмена липидов. Регуляция окисления и синтеза ЖК.
2. Метаболизм
3. Транспортные липопротеины (ЛП)
4. Липопротеинемии и атеросклероз.
5. Депонирование и мобилизация жиров.
6. Распространение и функции Хс.
7. Синтез Хс.
8. Транспорт Хс.
9. Сложные липиды и миелинизация.
Слайд 3Регуляция обмена липидов
Интенсивность обмена липидов в тканях зависит от:
а) поступления липидов
б) нервно-гумморальной регуляции
Избыточное поступление углеводов и ТАГ с пищей препятствует расходу эндогенных запасов ТАГ в жировой ткани. Прием даже полностью углеводной пищи существенно влияет на синтез ТАГ и Хс.
Слайд 4.
Вместе с тем, растительные масла, содержащие ненасыщенные ЖК напротив, способствуют мобилизации
Слайд 5
Нервно-гормональная регуляция липидного обмена
Стимуляторы тканевой липазы - адреналин, норадреналин, глюкагон, тироксин,
Ингибитор липолиза – инсулин (угнетает аденилатциклазу).
Слайд 6.
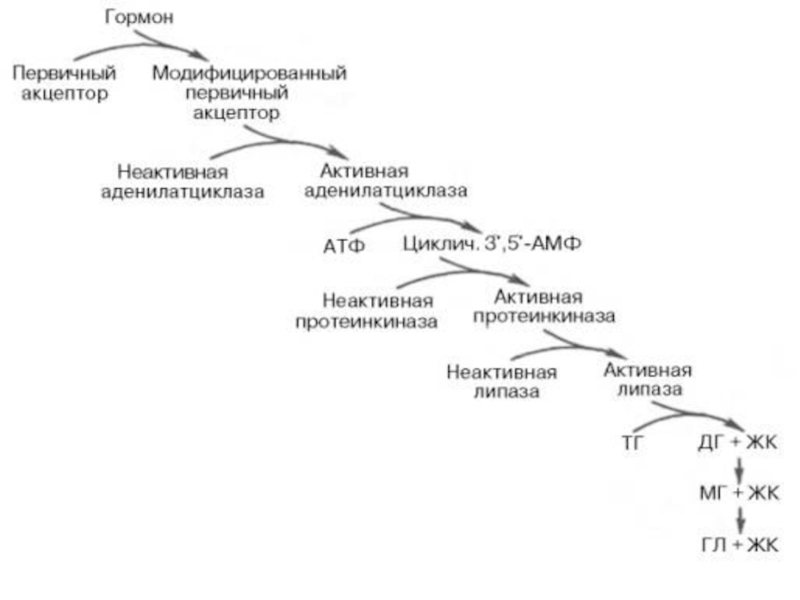
В такой форме данный рецептор способен активировать аденилатциклазу, что стимулирует образование
Липолитический каскад (по Стайнбергу).
Слайд 8Окисление и синтез ЖК регулируется:
а) разделением этих противоположных процессов в пространстве
б) резделением этих процессов во времени потеем аллостерической активации и ингибирования ферментов.
Слайд 9БИОСИНТЕЗ ТРИГЛИЦЕРИДОВ
Синтез триглицеридов происходит из глицерина и жирных кислот
(главным образом стеариновой,
Слайд 10В почках, а также в стенке кишечника, где активность фермента
глицеролкиназы высока,
зованием глицерол-3-фосфата:
Слайд 11В жировой ткани и мышцах вследствие очень низкой активности
глицеролкиназы образование глицерол-3-фосфата
процессами гликолиза и гликогенолиза. В процессе гликолитического распада глюкозы образуется дигидроксиацетонфосфат
Слайд 12
Последний в присутствии цитоплазматической глицерол-3-фосфатдегидрогеназы способен превращаться
Слайд 13Если содержание глюкозы в жировой ткани понижено (например, при голодании), то
глицерол-3-фосфата и освободившиеся в ходе липолиза свободные жирные кислоты не могут быть использованы для ресинтеза триглицеридов, поэтому жирные кислоты покидают жировую ткань.
Напротив, активация гликолиза в жировой ткани способствует накоплению в ней триглицеридов, а также входящих в их состав жирных кислот. В печени наблюдаются оба
пути образования глицерол-3-фосфата.
Слайд 14 Глицерол-3-фосфат последовательно ацилируется двумя молекулами КоА-производного жирной кислоты.
Слайд 15Далее фосфатидная кислота гидролизуется фосфатидат-фосфогидролазой до 1,2-диглицерида (1,2-диацилглицерола):
Слайд 16Затем 1,2-диглицерид ацилируется третьей молекулой ацил-КоА и превращается в триглицерид (триацилглицерол).
Слайд 17 Синтез триглицеридов (триацилглицеролов) в тканях происходит с
Слайд 18БИОСИНТЕЗ ХОЛЕСТЕРИНА
В синтезе холестерина можно выделить три основные стадии: I –
Слайд 19Превращение активного ацетата в мевалоновую кислоту
Начальным этапом синтеза мевалоновой кислоты
является образование ацетоацетил-КоА посредством обратимой тиолазной реакции:
Слайд 20 Затем при последующей конденсации ацетоацетил-КоА с 3-й молекулой ацетил-КоА
СН3—СО—СН2—СО—S-KoA + СН3—СО—S-KoA
Ацетоацетил-КоА Ацетил-КоА ГМГ-КоА-синтаза
β-Гидрокси-β-метилглутарил-КоА
Слайд 21Далее β-гидрокси-β-метилглутарил-КоА под действием регуляторного фермента НАДФ-зависимой гидроксиметилглутарил-КоА-редуктазы (ГМГ-КоА-редуктаза) в результате
β-Гидрокси-β-метилглутарил-КоА
ГМГ-КоА-редуктаза
Мевалоновая кислота
Слайд 22 На II стадии синтеза холестерина мевалоновая кислота превращается в
кислоты с помощью АТФ. В результате образуется 5-фосфорный эфир, а затем 5-пирофосфорный эфир мевалоновой кислоты:
Мевалонат 5-Фосфомевалонат 5-Пирофосфомевалонат
Слайд 235-пирофосфомевалоновая кислота в результате последующего фосфорилирования третичной гидроксильной группы образует нестабильный
промежуточный
Слайд 25Затем оба изомерных изопентенилпирофосфата (диметилаллилпирофосфат и изопентенилпирофосфат) конденсируются с высвобождением пирофосфата
Геранилпирофосфат
Слайд 26К геранилпирофосфату вновь присоединяется изопентенилпирофосфат. В результате этой реакции образуется фарнезилпирофосфат:
Фарнезилпирофосфат
Слайд 27В заключительной реакции данной стадии в результате НАДФН-зависимой восстановительной конденсации 2
образуется сквален:
Сквален (С30)
Слайд 28 На III стадии биосинтеза холестерина сквален под влиянием
Слайд 30Начиная со сквалена, все промежуточные продукты биосинтеза холестерина (включая и холестерин)
ными со стеринпереносящими белками (СПБ). Это обеспечивает их растворимость в цитозоле клетки и протекание соответствующих реакций.
Данный факт имеет важное значение и для вхождения холестерина в клеточные мембраны, окисления в желчные кислоты, превращения в стероидные гормоны.
Слайд 31 Реакцией, регулирующей скорость биосинтеза холестерина, является восстановление β-гидрокси-β-метилглутарил-КоА
Активность ГМГ-редуктазы возрастает при введении инсулина и тиреоидных гормонов. Это приводит к усилению синтеза холестерина и повышению его уровня в крови.
При голодании, тиреоидэктомии, введение глюкагона и глюкокортикоидов, напротив, отмечается угнетение синтеза холестерина, что прежде всего связано со снижением активности ГМГ-КоА-редуктазы.