- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Метаболизм нуклеотидов презентация
Содержание
- 1. Метаболизм нуклеотидов
- 2. Вопросы из билетов по теме Биосинтез и
- 3. Структура темы Классификация нуклеотидов Пуриновые нуклеотиды Синтез
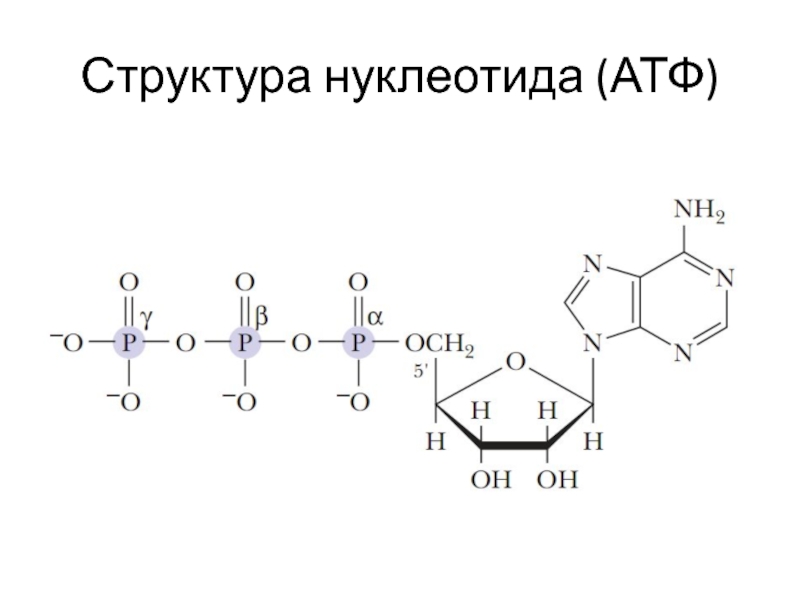
- 4. Структура нуклеотида (АТФ)
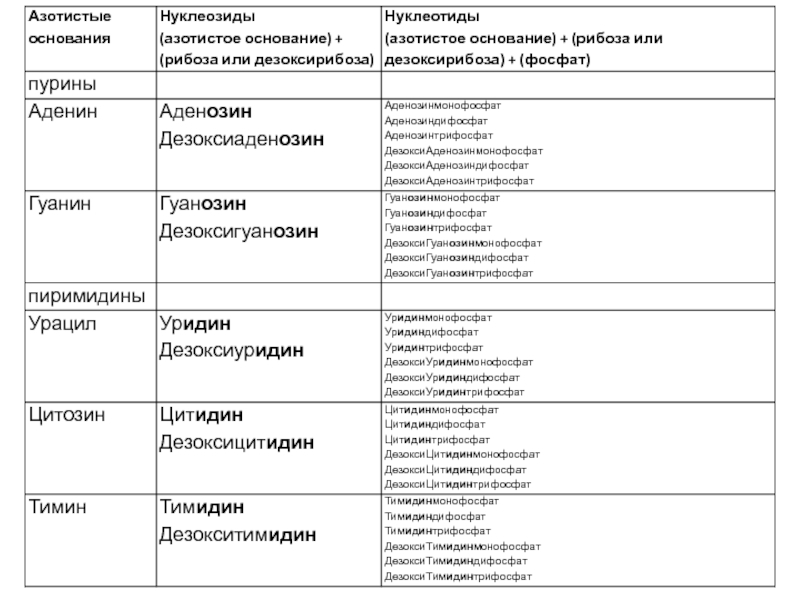
- 5. Классификация азотистых оснований Пурины: Аденин Гуанин
- 7. СИНТЕЗ ПУРИНОВ
- 8. Два пути синтеза нуклеотидов de novo (с
- 9. СИНТЕЗ DE NOVO
- 10. Синтез de novo: источники атомов пуринового кольца
- 11. Особенности синтеза Пуриновое кольцо строится постепенным добавлением
- 12. Синтез 1-я реакция: образование ФРПФ (фосфорибозилпирофосфат) из
- 13. 1-я реакция: образование фосфорибозилпирофосфата (ФРПФ = ФРДФ)
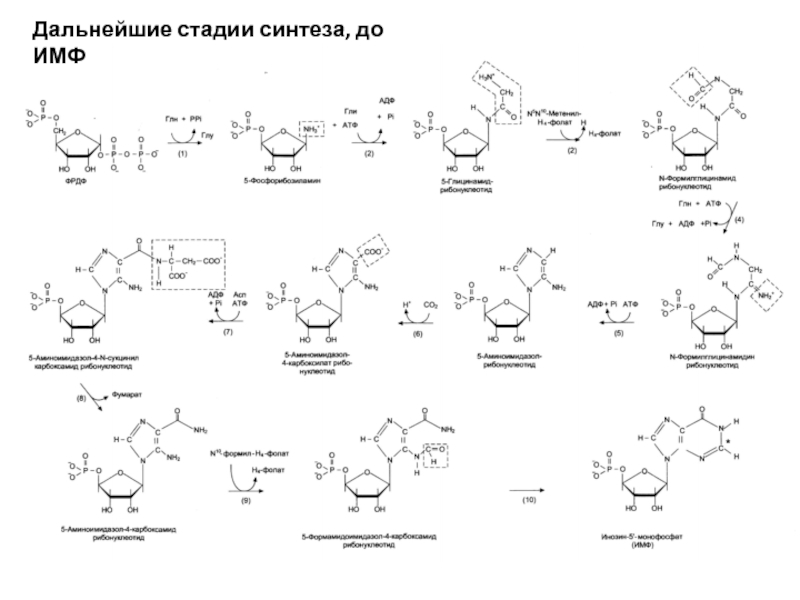
- 14. Дальнейшие стадии синтеза, до ИМФ
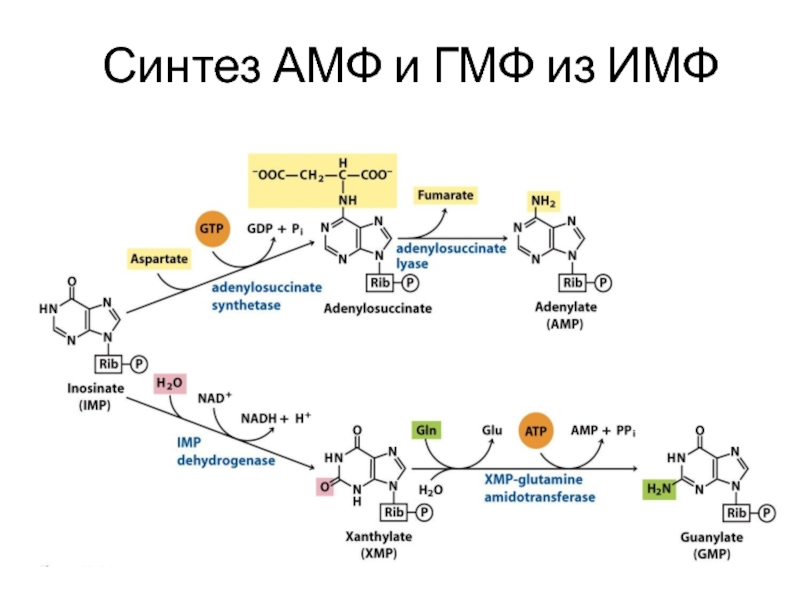
- 15. Синтез АМФ и ГМФ из ИМФ
- 16. Регуляция синтеза de novo Основной регуляторный фермент:
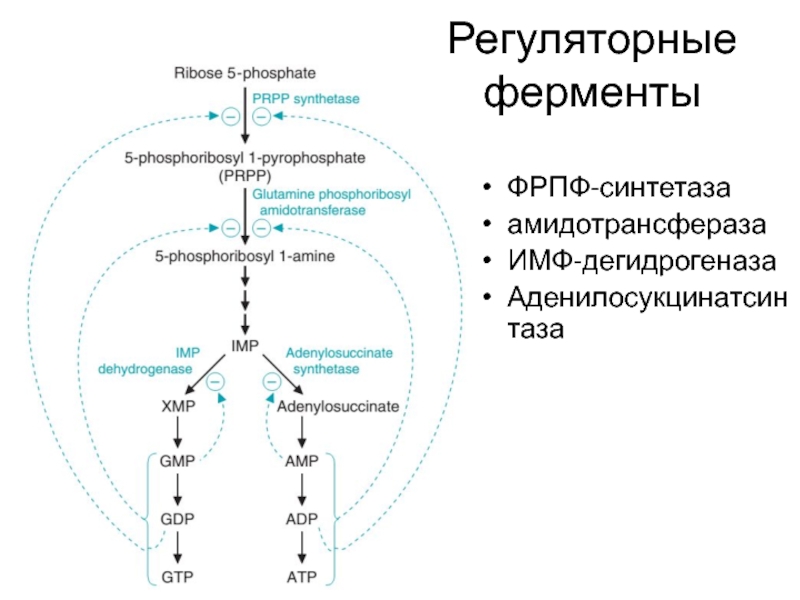
- 17. Регуляторные ферменты ФРПФ-синтетаза амидотрансфераза ИМФ-дегидрогеназа Аденилосукцинатсинтаза
- 18. ЗАПАСНОЙ ПУТЬ СИНТЕЗА (ПУТЬ СПАСЕНИЯ)
- 19. Функция: использовать уже синтезированные азотистые основания и
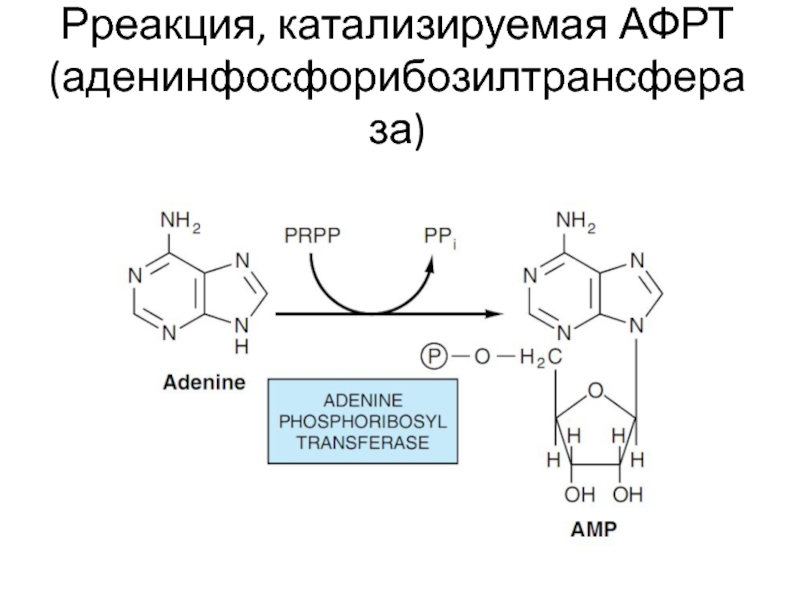
- 20. Рреакция, катализируемая АФРТ (аденинфосфорибозилтрансфераза)
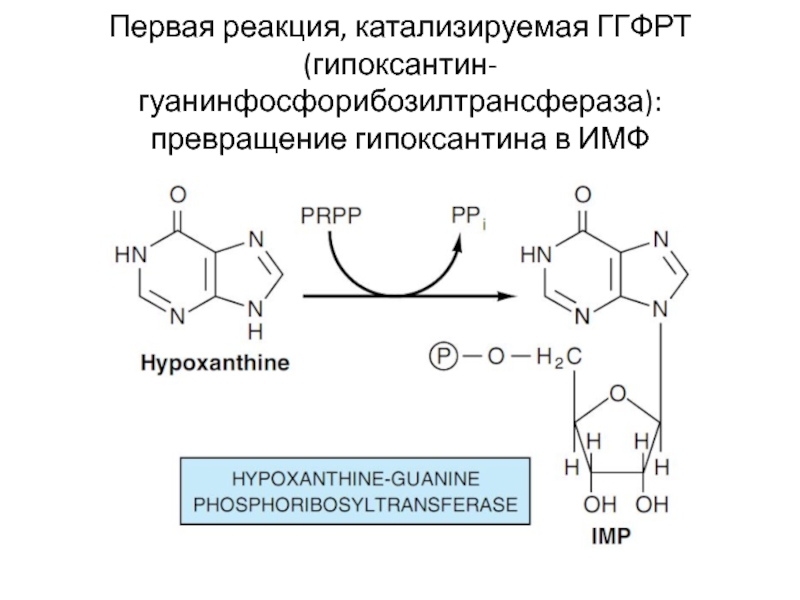
- 21. Первая реакция, катализируемая ГГФРТ (гипоксантин-гуанинфосфорибозилтрансфераза): превращение гипоксантина в ИМФ
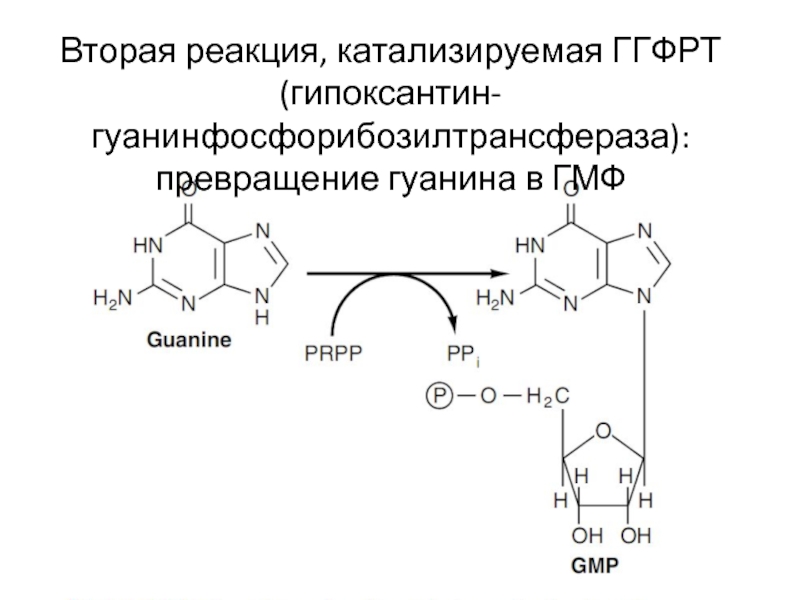
- 22. Вторая реакция, катализируемая ГГФРТ (гипоксантин-гуанинфосфорибозилтрансфераза): превращение гуанина в ГМФ
- 23. РАСПАД ПУРИНОВ
- 24. Конечным продуктом распада является мочевая кислота (содержит
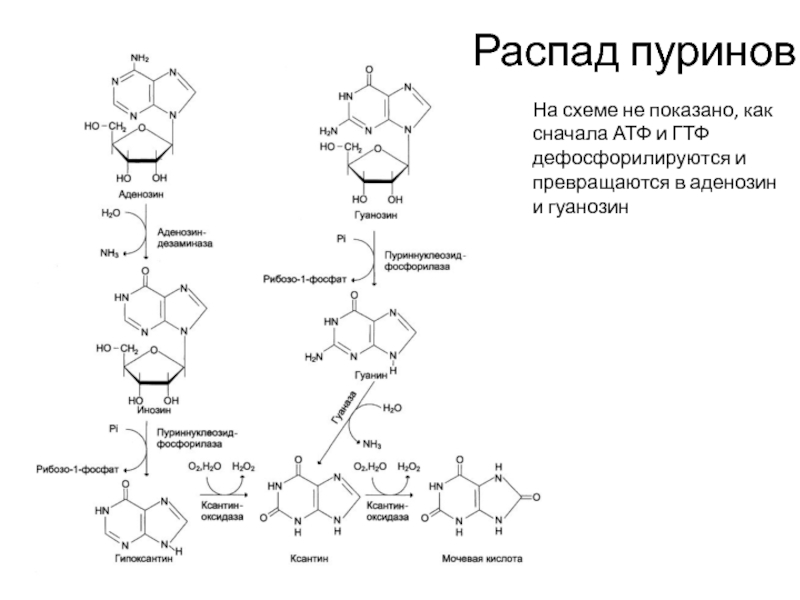
- 25. Распад пуринов На схеме не показано, как
- 26. НАРУШЕНИЯ МЕТАБОЛИЗМА ПУРИНОВ
- 27. Гиперурикемия: повышение содержания мочевой кислоты в крови
- 28. СИНТЕЗ ПИРИМИДИНОВ
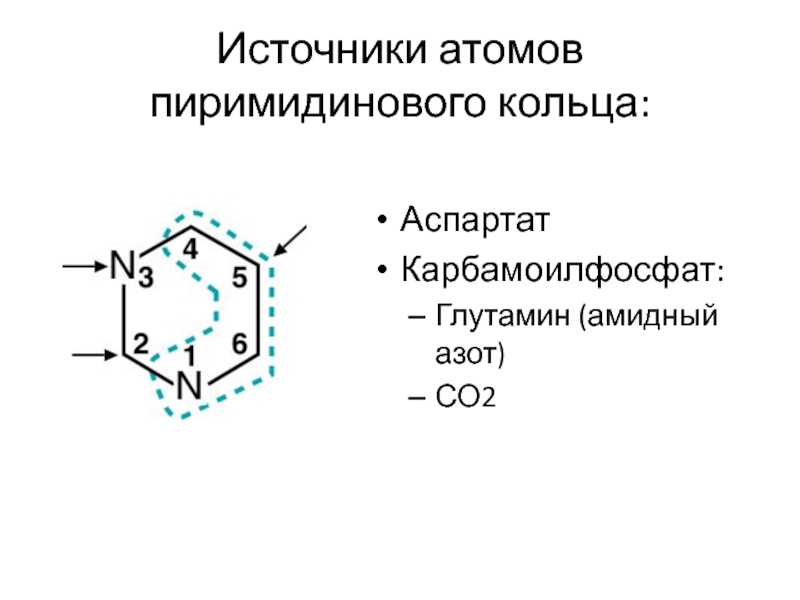
- 29. Источники атомов пиримидинового кольца: Аспартат Карбамоилфосфат: Глутамин (амидный азот) СО2
- 30. Сначала синтезируется свободное азотистое основание, затем оно
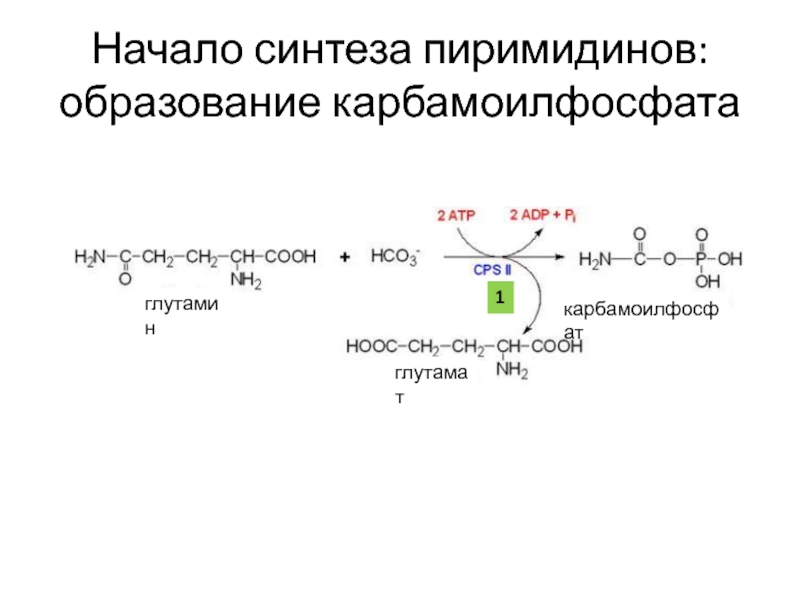
- 31. Начало синтеза пиримидинов: образование карбамоилфосфата глутамин глутамат карбамоилфосфат 1
- 32. Аспартат + карбамоилфосфат N-карбамоиласпартат
- 33. Оротидин-5-монофосфат УМФ (уридинмонофосфат)
- 34. Полифункциональные ферменты синтеза пиримидинов Реакции 1, 2
- 35. Регуляция Регуляторный фермент: карбамоилфосфатсинтетаза II (часть полифункционального
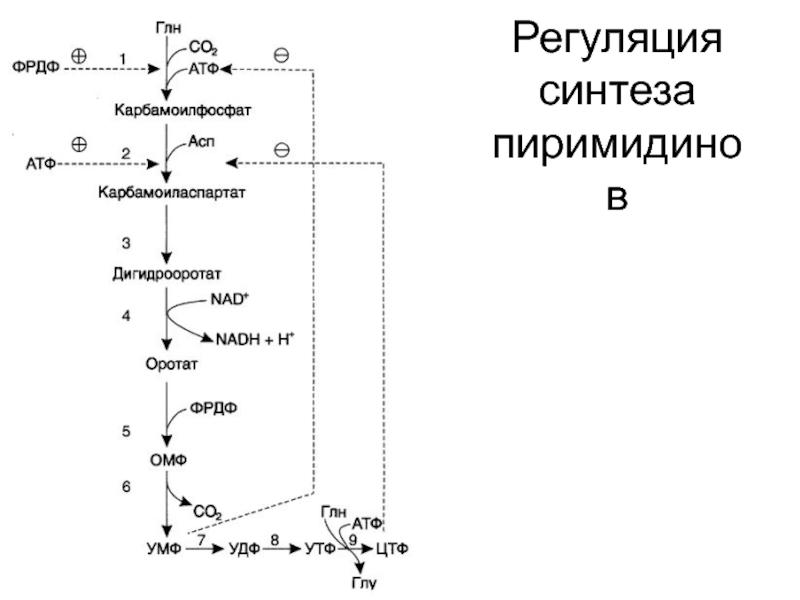
- 36. Регуляция синтеза пиримидинов
- 37. Нарушения: оротацидурия Причина: мутации в ферменте УМФ-синтаза
- 38. РАСПАД ПИРИМИДИНОВ
- 39. Конечные продукты распада УМФ и ЦМФ: СО2
- 40. Распад пиримидинов На схеме не показано, как
- 41. СИНТЕЗ ДЕЗОКСИРИБОНУКЛЕОТИДОВ
- 42. Основные пути синтеза ведут к появлению только
- 43. Фермент рибонуклеотидредуктаза: Синтезирует дезоксирибонуклеотиды (дАДФ, дГДФ, дГДФ,
- 44. Схема реакции, катализируемой рибонуклеотидредуктазой: НДФ (нуклеотиддифосфат) превращается
- 45. Синтез дТМФ Зелеными стрелками
Слайд 2Вопросы из билетов по теме
Биосинтез и распад пиримидиновых нуклеотидов.
Источники атомов пуринового
кольца. Распад пуриновых нуклеотидов. Гиперурикемия и подагра.
Слайд 3Структура темы
Классификация нуклеотидов
Пуриновые нуклеотиды
Синтез
Распад
Нарушения распада и синтеза: подагра
Пиримидиновые нуклеотиды
Синтез
Распад
Нарушения синтеза
Синтез дезоксирибонуклеотидов
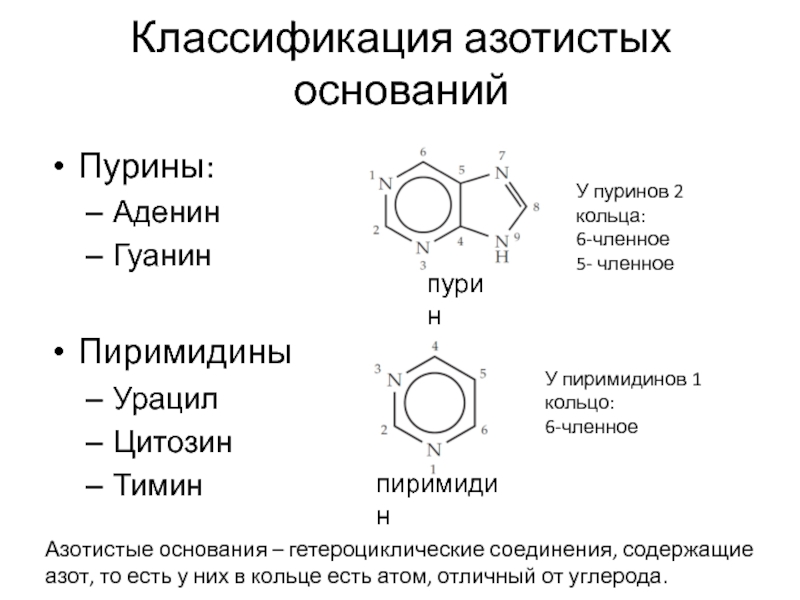
Слайд 5Классификация азотистых оснований
Пурины:
Аденин
Гуанин
Пиримидины
Урацил
Цитозин
Тимин
У пуринов 2 кольца:
6-членное
5- членное
У пиримидинов 1 кольцо:
6-членное
Азотистые основания
– гетероциклические соединения, содержащие азот, то есть у них в кольце есть атом, отличный от углерода.
Слайд 8Два пути синтеза нуклеотидов
de novo (с нуля):
из простых предшественников
Запасной путь
(путь спасения):
из ранее синтезированных азотистых оснований
из ранее синтезированных азотистых оснований
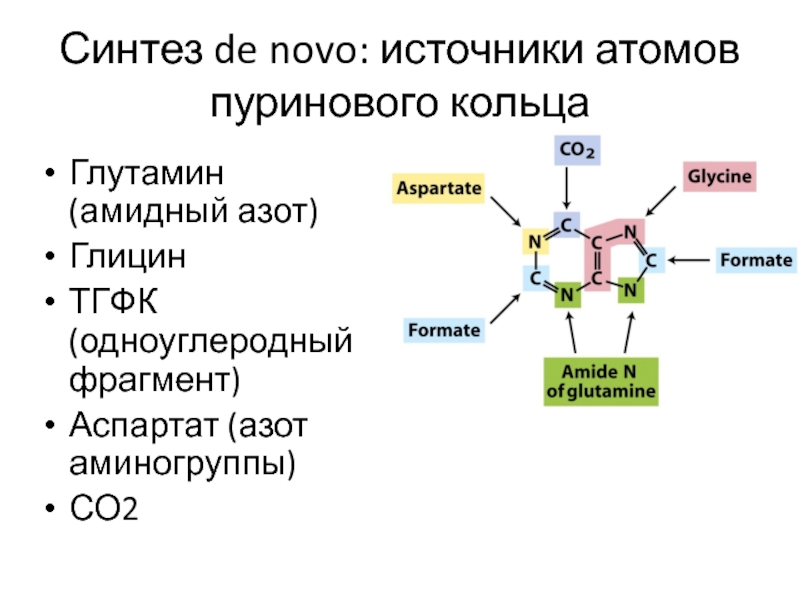
Слайд 10Синтез de novo: источники атомов пуринового кольца
Глутамин (амидный азот)
Глицин
ТГФК (одноуглеродный фрагмент)
Аспартат
(азот аминогруппы)
СО2
СО2
Слайд 11Особенности синтеза
Пуриновое кольцо строится постепенным добавлением новых атомов в строго определенном
порядке
Пуриновое кольцо строится на рибозе (т.е. рибоза присутствует в структуре всех промежуточных веществ метаболического пути)
Инозинмонофосфат (ИМФ) – предшественник всех пуринов, первый пуриновый нуклеотид (хотя он не встречается в ДНК и почти не встречается в РНК, минорный нуклеотид)
АМФ и ГМФ образуются из ИМФ
Пуриновое кольцо строится на рибозе (т.е. рибоза присутствует в структуре всех промежуточных веществ метаболического пути)
Инозинмонофосфат (ИМФ) – предшественник всех пуринов, первый пуриновый нуклеотид (хотя он не встречается в ДНК и почти не встречается в РНК, минорный нуклеотид)
АМФ и ГМФ образуются из ИМФ
Слайд 12Синтез
1-я реакция: образование ФРПФ (фосфорибозилпирофосфат) из рибозо-5-фосфата (см. пентозофосфатный путь) и
АТФ.
Фермент: ФРПФ-синтаза (регуляторный фремент)
Далее путем последовательного добавления атомов кольца строится ИМФ (инозинмонофосфат)
Для образования АМФ из ИМФ нужны:
ГТФ (источник энергии)
аспартат(источник N)
Для образования ГМФ из ИМФ нужны:
АТФ (источник энергии)
Глутамин (источник N)
АМФ и ГМФ затем фосфорилируются специальными киназами (с затратой АТФ) с образованием нуклеотидтрифосфатов (АТФ и ГТФ)
Фермент: ФРПФ-синтаза (регуляторный фремент)
Далее путем последовательного добавления атомов кольца строится ИМФ (инозинмонофосфат)
Для образования АМФ из ИМФ нужны:
ГТФ (источник энергии)
аспартат(источник N)
Для образования ГМФ из ИМФ нужны:
АТФ (источник энергии)
Глутамин (источник N)
АМФ и ГМФ затем фосфорилируются специальными киназами (с затратой АТФ) с образованием нуклеотидтрифосфатов (АТФ и ГТФ)
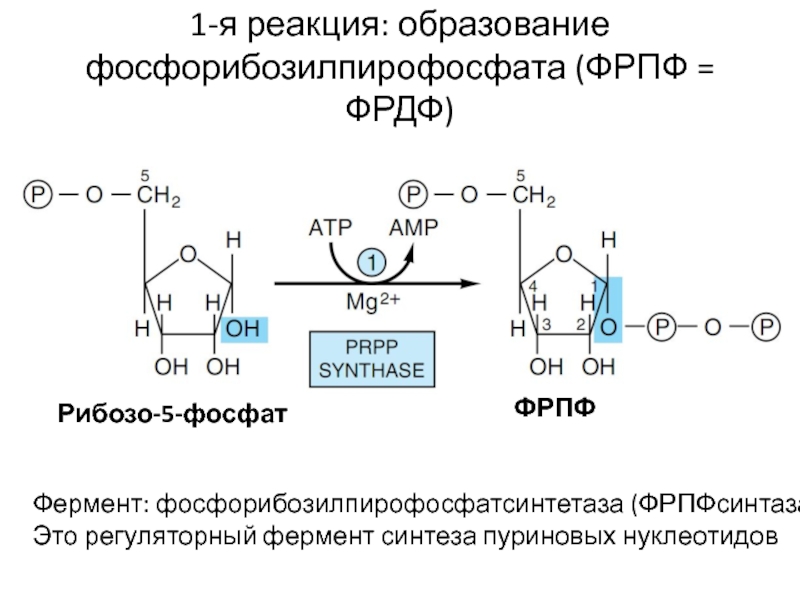
Слайд 131-я реакция: образование фосфорибозилпирофосфата (ФРПФ = ФРДФ)
Фермент: фосфорибозилпирофосфатсинтетаза (ФРПФсинтаза)
Это регуляторный фермент
синтеза пуриновых нуклеотидов
Рибозо-5-фосфат
ФРПФ
Слайд 16Регуляция синтеза de novo
Основной регуляторный фермент: ФРПФ-синтетаза
Другие регуляторные ферменты: глутамин-фосфорибозиламидотрансфераза, ИМФ-дегидрогеназа,
аденилосукцинатсинтаза
ФРПФ-синтетатза ингибируется всеми пуриновыми нуклеотидами (АТФ, АДФ, АМФ, ГТФ, ГДФ, ГМФ)
Это позволяет не производить нуклеотиды в избытке – принцип отрицательной обратной связи
ФРПФ-синтетатза ингибируется всеми пуриновыми нуклеотидами (АТФ, АДФ, АМФ, ГТФ, ГДФ, ГМФ)
Это позволяет не производить нуклеотиды в избытке – принцип отрицательной обратной связи
Слайд 19Функция: использовать уже синтезированные азотистые основания и нуклеозиды
Основные ферменты: ГГФРТ (гипоксантингуанинфосфорибозилтрансфераза)
и АФРТ (аденозинфосфорибозилтрансфераза)
Действие ферментов основано на том, что они присоединяют пуриновое азотистое основание (аденин, гуанин или гипоксантин) к рибозе (из ФРПФ)
Действие ферментов основано на том, что они присоединяют пуриновое азотистое основание (аденин, гуанин или гипоксантин) к рибозе (из ФРПФ)
Слайд 21Первая реакция, катализируемая ГГФРТ (гипоксантин-гуанинфосфорибозилтрансфераза): превращение гипоксантина в ИМФ
Слайд 22Вторая реакция, катализируемая ГГФРТ (гипоксантин-гуанинфосфорибозилтрансфераза): превращение гуанина в ГМФ
Слайд 24Конечным продуктом распада является мочевая кислота (содержит пуриновое кольцо, т.е. сама
является пурином)
При распаде АТФ и ГТФ
удаляются фосфаты и рибоза
Аденин превращается сначала в гипоксантин, потом в ксантин и мочевую кислоту
Гуанин сначала превращается в ксантин, потом мочевую кислоту
Превращение «гипоксантин → ксантин → мочевая кислота» катализируется одним и тем же ферментом (ксантиноксидаза)
При распаде АТФ и ГТФ
удаляются фосфаты и рибоза
Аденин превращается сначала в гипоксантин, потом в ксантин и мочевую кислоту
Гуанин сначала превращается в ксантин, потом мочевую кислоту
Превращение «гипоксантин → ксантин → мочевая кислота» катализируется одним и тем же ферментом (ксантиноксидаза)
Слайд 25Распад пуринов
На схеме не показано, как сначала АТФ и ГТФ дефосфорилируются
и превращаются в аденозин и гуанозин
Слайд 27Гиперурикемия: повышение содержания мочевой кислоты в крови
Мочевая кислота плохо растворима в
воде. Накапливаясь в синовиальной жидкости, она образует кристаллы и повреждает клетки, что приводит к воспалению сустава (подагра)
Причина гиперурикемии: избыточный синтез пуринов, который приводит к их усиленному распаду с образованием мочевой кислоты
Причина усиления синтеза пуринов:
недостаточность запасных путей синтеза (пути спасения) (синдром Леша-Нихона)
Дефектный ответ ФРПФ-синтетазы на ингибирование нуклеотидами или суперактивация ФРПФ-синтетазы
Заболевания, при которых наблюдается гиперурикемия:
подагра (подагрический артрит)
синдром Леша-Нихона
Для лечения подагры используется ингибитор ксантиноксидазы - аллопуринол
Причина гиперурикемии: избыточный синтез пуринов, который приводит к их усиленному распаду с образованием мочевой кислоты
Причина усиления синтеза пуринов:
недостаточность запасных путей синтеза (пути спасения) (синдром Леша-Нихона)
Дефектный ответ ФРПФ-синтетазы на ингибирование нуклеотидами или суперактивация ФРПФ-синтетазы
Заболевания, при которых наблюдается гиперурикемия:
подагра (подагрический артрит)
синдром Леша-Нихона
Для лечения подагры используется ингибитор ксантиноксидазы - аллопуринол
Слайд 30Сначала синтезируется свободное азотистое основание, затем оно прикрепляется к рибозе
первое азотистое
основание – оротовая кислота (оротат), из него потом синтезируются УМФ и ЦМФ
Ферменты синтеза являются полифункциональными – у них имеется несколько активных центров, которые катализируют последовательные реакции метаболического пути. Всего в метаболическом пути синтеза УМФ 6 реакций, но катализируют их 3 белка
Ферменты синтеза являются полифункциональными – у них имеется несколько активных центров, которые катализируют последовательные реакции метаболического пути. Всего в метаболическом пути синтеза УМФ 6 реакций, но катализируют их 3 белка
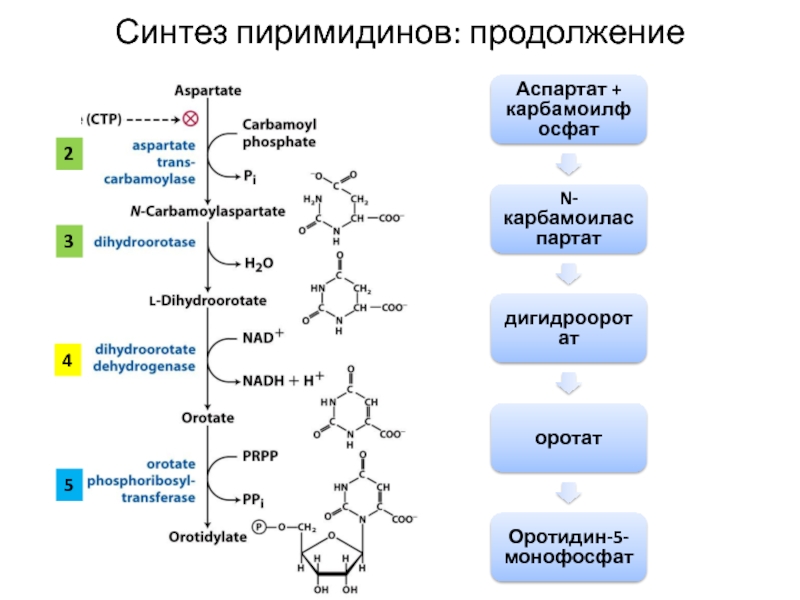
Слайд 32Аспартат + карбамоилфосфат
N-карбамоиласпартат
дигидрооротат
оротат
Оротидин-5-монофосфат
2
3
Синтез пиримидинов: продолжение
4
5
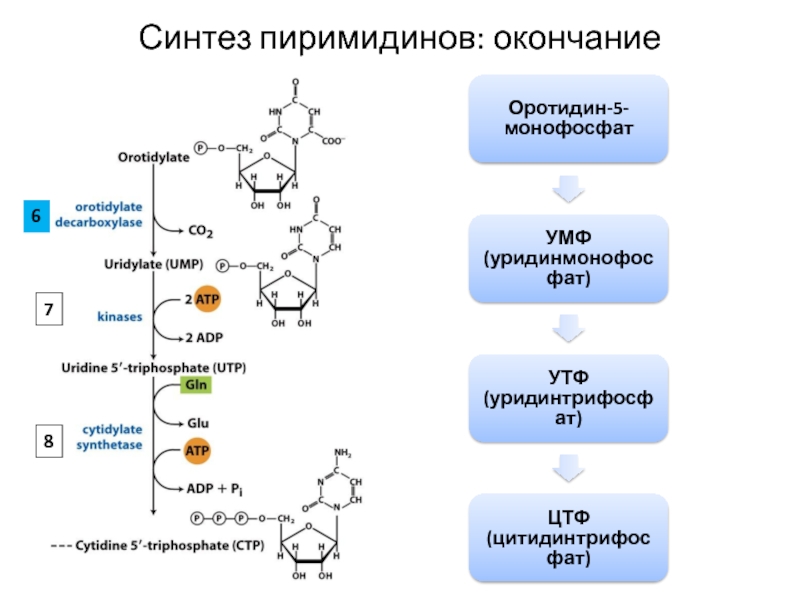
Слайд 33Оротидин-5-монофосфат
УМФ (уридинмонофосфат)
УТФ (уридинтрифосфат)
ЦТФ (цитидинтрифосфат)
Синтез пиримидинов: окончание
6
7
8
Слайд 34Полифункциональные ферменты синтеза пиримидинов
Реакции 1, 2 и 3 катализируются одним ферментом,
у которого есть 3 активных центра
Реакции 5 и 6 катализируются одним ферментом, у которого есть 2 активных центра
Таким образом, всего в синтезе пиримидинов принимают участие 2 полифункциональных фермента
Реакции 5 и 6 катализируются одним ферментом, у которого есть 2 активных центра
Таким образом, всего в синтезе пиримидинов принимают участие 2 полифункциональных фермента
Слайд 35Регуляция
Регуляторный фермент: карбамоилфосфатсинтетаза II (часть полифункционального фермента, катализирующего 3 первые реакции
синтеза)
Ингибируется УМФ и ЦТФ (по принципу отрицательной обратной связи)
Ингибируется УМФ и ЦТФ (по принципу отрицательной обратной связи)
Слайд 37Нарушения: оротацидурия
Причина: мутации в ферменте УМФ-синтаза
Следствия:
гиперпродукция оротата
Мегалобластная анемия
Нарушения умственного развития, двигательной
активности, работы сердца, ЖКТ, иммунитета
Образование камней
не синтезируются все пиримидиновые нуклеотиды
Лечение: необходим прием уридина
Образование камней
не синтезируются все пиримидиновые нуклеотиды
Лечение: необходим прием уридина
Слайд 39Конечные продукты распада УМФ и ЦМФ:
СО2
Аммиак
β-аланин
Конечные продукты распада дТМФ:
СО2
Аммиак
β-аминоизомасляная кислота (β-аминоизобутират)
β-аланин
и β-аминоизомасляная кислота могут превращаться в малонил-КоА и сукцинил-КоА, соответственно
β-аланин входит в состав дипептида карнозина и пантотеновой кислоты (вит. В3)
β-аланин входит в состав дипептида карнозина и пантотеновой кислоты (вит. В3)
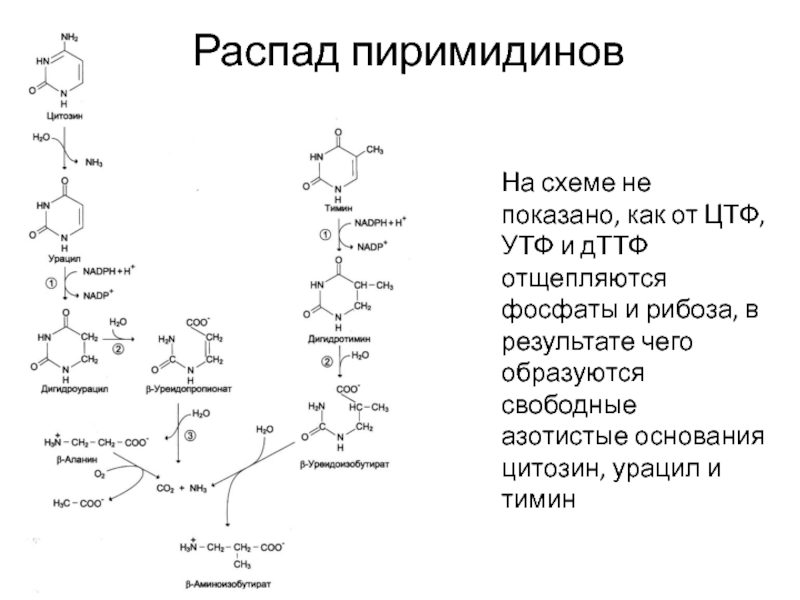
Слайд 40Распад пиримидинов
На схеме не показано, как от ЦТФ, УТФ и дТТФ
отщепляются фосфаты и рибоза, в результате чего образуются свободные азотистые основания цитозин, урацил и тимин
Слайд 42Основные пути синтеза ведут к появлению только РИБОнуклеотидов (для РНК)
1. Путь
синтеза пиримидинов de novo позволяет клетке синтезировать только рибонуклеотиды УТФ и ЦТФ.
2. Путь синтеза пуринов de novo позволяет клетке синтезировать только рибонуклеотиды АТФ и ГТФ.
Поэтому только этих двух путей недостаточно для синтеза ДНК, так как:
нужен Т
Нужны дезоксирибонуклеотиды
2. Путь синтеза пуринов de novo позволяет клетке синтезировать только рибонуклеотиды АТФ и ГТФ.
Поэтому только этих двух путей недостаточно для синтеза ДНК, так как:
нужен Т
Нужны дезоксирибонуклеотиды
Слайд 43Фермент рибонуклеотидредуктаза:
Синтезирует дезоксирибонуклеотиды (дАДФ, дГДФ, дГДФ, дУДФ) из соответствующих рибонуклеотидов
Для этого
он катализирует превращение рибозы в дезоксирибозу в их составе (ОВР)
В этой реакции в качестве кофермента используется тиоредоксин (белок)
Для последующего восстановления тиоредоксина нужен НАДФН (из пентозофосфатного пути)
Синтез дТМФ (ТМФ) происходит из дУДФ
В этой реакции в качестве кофермента используется тиоредоксин (белок)
Для последующего восстановления тиоредоксина нужен НАДФН (из пентозофосфатного пути)
Синтез дТМФ (ТМФ) происходит из дУДФ
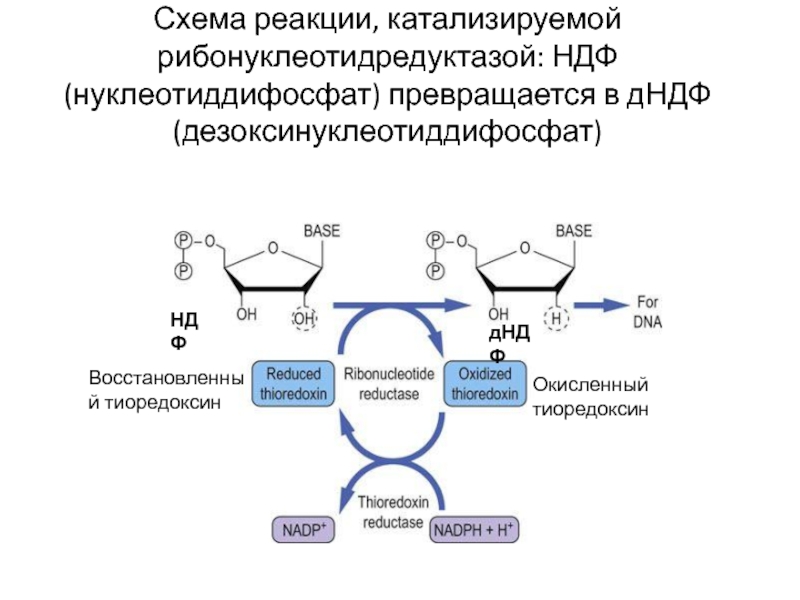
Слайд 44Схема реакции, катализируемой рибонуклеотидредуктазой: НДФ (нуклеотиддифосфат) превращается в дНДФ (дезоксинуклеотиддифосфат)
НДФ
дНДФ
Восстановленный тиоредоксин
Окисленный
тиоредоксин
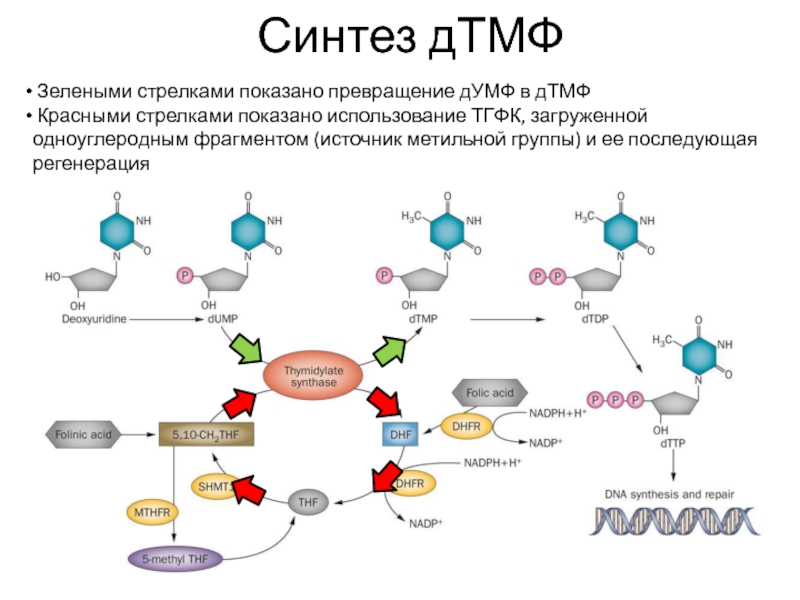
Слайд 45Синтез дТМФ
Зелеными стрелками показано превращение дУМФ в дТМФ
Красными стрелками
показано использование ТГФК, загруженной одноуглеродным фрагментом (источник метильной группы) и ее последующая регенерация