- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Механизмы регуляции пролиферативных процессов клетках презентация
Содержание
- 1. Механизмы регуляции пролиферативных процессов клетках
- 2. 1. Общая характеристика системы регуляции На деление
- 3. Механизм регуляции клеточного размножения – системный.
- 4. NB: На разных уровнях регуляции есть как
- 5. 2. Доказательства генетического контроля цикла Установлено, что
- 6. 1) S + G1 В G1-ядре сразу
- 7. 3) G1, S, G2 + M В интерфазном
- 8. 4) G1 + G2 G1-ядро
- 9. 2.2. Опыты по ингибированию синтезов РНК и
- 10. Результат 1. Запуск S-периода. Если перед
- 11. Результат 2. Запуск митоза. Аналогично, блокада синтезов
- 12. Т.о., ингибиторный анализ показал, что: 1)
- 13. 2.3. Генетические доказательства генной регуляции цикла. Генное
- 14. В делении дрожжей различимы 3 относительно независимых
- 15. Клетки млекопитающих. В различных клеточных культурах
- 16. 3. Гены компетентности к циклу (раннего ответа)
- 17. В частности: Семейство генов myc – кодирует
- 18. Т.о., работает каскад: ФР → Рецептор →
- 19. 4. Гены прогрессии цикла. Циклины
- 20. В 1971 г. у лягушки выявлен MPF
- 21. Так сформировались два конкурирующих (казалось – взаимоисключающих)
- 22. В 1980-х годах была установлена идентичность белков,
- 23. В первой половине митоза (профаза-метафаза) киназа
- 24. Так изменяется концентрация белков в клетке:
- 25. Функции (активности) протеинкиназы Cdk1 в организации митоза:
- 26. Но, как и следовало ожидать, вскоре были
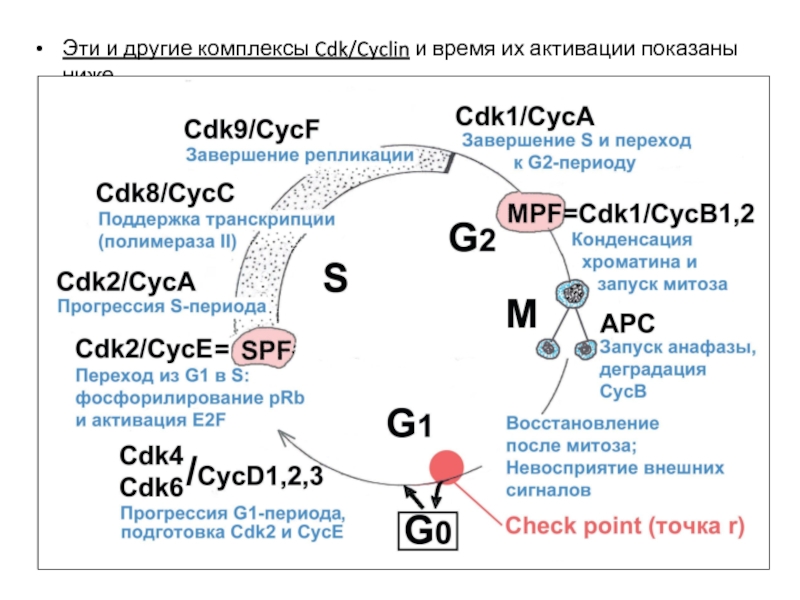
- 27. Эти и другие комплексы Cdk/Cyclin и время их активации показаны ниже.
- 28. NB: В раннем эмбриогенезе (дробление зиготы,
- 29. 5. Система контрольных точек и ингибиторы
- 30. Гипотеза Хартвела: В клетке существует контрольный
- 31. Наиболее важен и сложен р53-р21/Waf1-pRb–зависимый путь (опухолевой
- 32. NB: Транскрипционный фактор р53 участвует также в
- 33. И еще одно важное NB:
- 34. 6. Факторы роста Сколько бы генов не
- 35. Действие ФР в чистом виде можно изучать
- 36. 6.1. Общие свойства и механизм действия факторов
- 37. 3) ФР присутствуют в ткани и работают
- 38. 7) Цитоплазматический сигналинг от рецепторов к ядру
- 39. Пример: система сигналинга при взаимодействии клетки
- 40. Активированная рецепторная тирозинкиназа (RTK) стимулирует также фосфолипазу
- 41. 6.2. Разнообразие факторов роста Известны десятки семейств
- 42. 2. PDGF – Plate Dependent Growth Factor;
- 43. Примеры: FGF-2 играет важную роль при формировании
- 44. 4. SDGF-1 – Spleen Dependent Growth Factor;
- 45. 7. Гемопоэтические ФР. Эритропоэтин. Источник:
- 46. 9. TGF-β – Transforming Growth Factor-β; =
- 47. 10. SDGF – Shwannomous Dependent Growth Factor
- 48. 6.3. Факторы роста препятствуют старению и гибели
- 49. Культура эпидермиса ребенка на обычной среде с
- 50. Т.о., с факторами роста могут быть связаны
- 51. 7. Гормоны и пролиферация клеток В отличие
- 52. 7.1. Моноамины Моноаминовые гормоны образуются из аминокислот
- 53. Согласно теории кейлонов – тканеспецифичных ингибиторов пролиферации,
- 54. Триптофан → серотонин, триптамин и др. (индольные
- 55. Образование более сложных гормонов шло посредством реакций
- 56. Кортикостероиды – гормоны коры надпочечников позвоночных.
- 57. Механизм действия стероидов отличается от действия других
- 58. 7.3. Пептидные гормоны Имеются уже у низших
- 59. - Нейропептиды гипоталамуса (рилизинг-пептиды): соматолиберин, кортиколиберин,
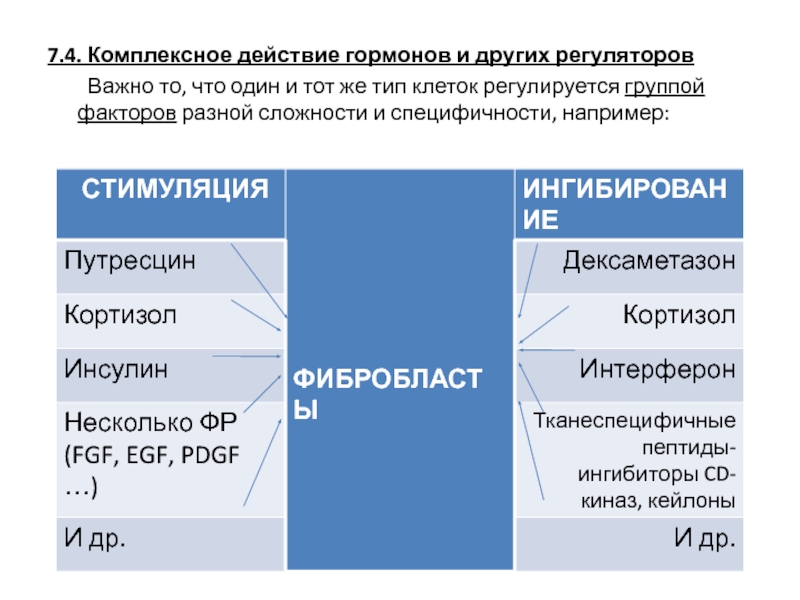
- 60. 7.4. Комплексное действие гормонов и других регуляторов
- 61. При этом сами регуляторы встроены в сложные
- 62. Таким образом, гормоны включены в кооперативное действие
- 63. Заключение В целом получается такая система регуляции
- 64. 3) У одноклеточных переход через точку r
- 65. 4) Другие факторы роста аналогичными путями повышают
Слайд 21. Общая характеристика системы регуляции
На деление клеток могут действовать самые разные
влияющие на синтез нуклеотидов, ДНК, РНК, белков;
влияющие на синтез и накопление АТФ (энергетический «резервуар» митоза), особенно ингибиторы гликолиза и дыхания;
влияющие на формирование митотического веретена.
Это могут быть неспецифические факторы, модифицирующие цикл, часто побочные (температура, оксигенация, токсины и др.).
Нас интересуют здесь специфические регуляторные факторы, специально предназначенные для управления клеточным циклом.
Очевидно, что в гистогенезах изменения параметров
цикла, задержки в G0, выход в дифференцировку –
это отражение действия каких-то регулирующих
факторов.
Действие таких регуляторов возможно в точках
повышенной чувствительности (точка r, check points)
клеточного цикла.
Слайд 3Механизм регуляции клеточного размножения – системный.
Он состоит из многих параллельных
1) Клеточные регуляторы: ядерные (генетические), цитоплазматические (вторичные мессенджеры), мембранные (рецепторы);
2) Организменные регуляторы: гуморальные местные, тканеспецифические (факторы роста, ингибиторы), гуморальные дистантные, ткане- и видо-неспецифические (гормоны – стимуляторы и ингибиторы), нервные, от ЦНС через гипоталамус на аденогипофиз и далее на местные эндокринные железы;
3) Средовые регуляторы: через ЦНС, непосредственные абиотические, модифицирующие (тепло и др.).
Слайд 4NB: На разных уровнях регуляции есть как стимуляторы (+), так и
Давно существовало 2 противоположных взгляда на сам принцип регуляции митозов:
Митогенная регуляция:
нормальное состояние клетки – покоящееся, а для деления необходимы стимуляторы, митогены.
Ингибиторная регуляция:
нормальное состояние клетки – непрерывная пролиферация, которая ограничивается ингибиторами.
Что верно? Или все сложнее?
Слайд 52. Доказательства генетического контроля цикла
Установлено, что последовательность фаз митотического цикла (-G1-S-G2-M-)
В крайнем выражении эта закономерность известна как принцип домино: очередной ген включается продуктами предыдущего гена.
Доказательства генетического контроля цикла складывались из разных фактов, экспериментов: цитологических, биохимических, генетических.
2.1. Опыты по слиянию клеток HeLa
Разработаны методы гибридизации (слияния) клеток. Получение гетерокарионов – клеток с различающимися ядрами.
Объединяли гомологичные однолинейные клетки (культура HeLa), но находящиеся в разных фазах митотического цикла (гетерофазные клетки).
Показали наличие фазово-специфических индукторов и ингибиторов митотического цикла.
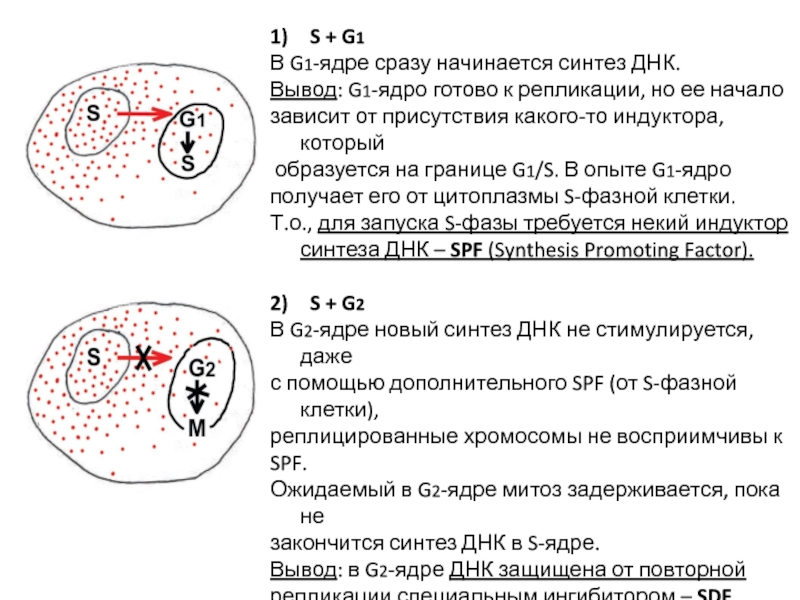
Слайд 61) S + G1
В G1-ядре сразу начинается синтез ДНК.
Вывод: G1-ядро готово
зависит от присутствия какого-то индуктора, который
образуется на границе G1/S. В опыте G1-ядро
получает его от цитоплазмы S-фазной клетки.
Т.о., для запуска S-фазы требуется некий индуктор синтеза ДНК – SPF (Synthesis Promoting Factor).
2) S + G2
В G2-ядре новый синтез ДНК не стимулируется, даже
с помощью дополнительного SPF (от S-фазной клетки),
реплицированные хромосомы не восприимчивы к
SPF.
Ожидаемый в G2-ядре митоз задерживается, пока не
закончится синтез ДНК в S-ядре.
Вывод: в G2-ядре ДНК защищена от повторной
репликации специальным ингибитором – SDF
(Synthesis Delaying Factor).
Для запуска митоза необходим М-индуктор?
В опыте он разбавляется цитоплазмой S-клетки?
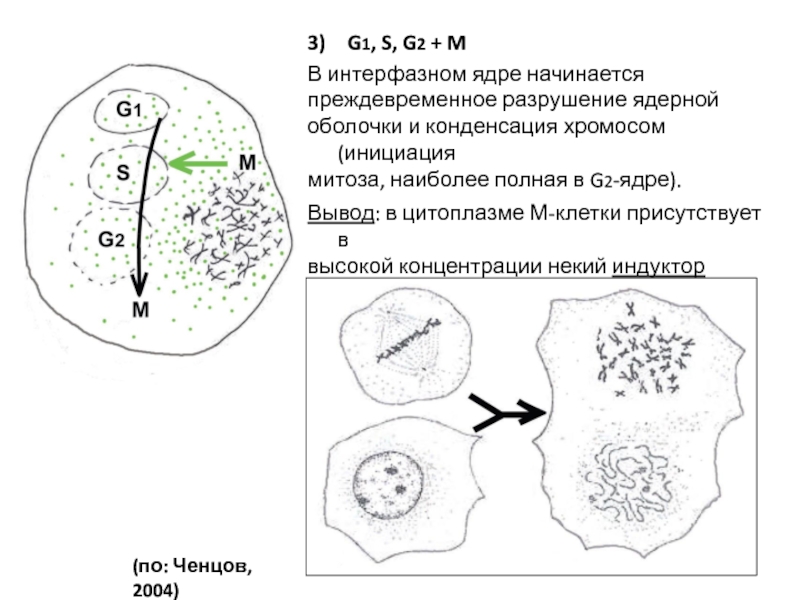
Слайд 73) G1, S, G2 + M
В интерфазном ядре начинается
преждевременное разрушение ядерной
оболочки и конденсация хромосом (инициация
митоза, наиболее полная в G2-ядре).
Вывод: в цитоплазме М-клетки присутствует в
высокой концентрации некий индуктор митоза –
MPF (Mitosis Promoting Factor).
(по: Ченцов, 2004)
Слайд 8 4) G1 + G2
G1-ядро проходит цикл по графику,
в
Вывод: митоз начинается лишь при критическом уровне MPF (в опыте он разбавляется G1-клетой).
Возможно также присутствие в цитоплазме сигнала задержки митоза – MDF (Mitosis Delaying Factor). (Показана задержка митоза избытком одноцепочечной ДНК).
Т.о., смена периодов митотического цикла контролируется выработкой и накоплением в определенных концентрациях специальных индукторов и ингибиторов цикла:
- SPF – активатор синтеза ДНК,
- SDF – S-задерживающий фактор,
- MPF – М-стимулирующий фактор,
- MDF – М-задерживающий фактор.
Регулярная смена этих факторов в цитоплазме и кариоплазме разграничивает ряд событий хромосомного цикла, предотвращая неувязки (вроде конденсации хромосом посреди S-фазы или повторной репликации перед митозом).
Каковы же природа и происхождение этих факторов?
Слайд 92.2. Опыты по ингибированию синтезов РНК и белка в цикле –
ингибиторный анализ для выявления возможной роли РНК и белков в регуляции митотического цикла (Епифанова, 1973).
Опыты на клеточных культурах, синхронизированных по циклу.
Синтезы РНК и белков блокировали соответствующими ингибиторами:
- ингибитор синтеза РНК – антибиотик актиномицин D (связывается с ДНК и блокирует транскрипцию).
- ингибитор синтеза белка – пуромицин (блокировка связи мРНК-тРНК) или циклогексимид (блок мРНК-рибосома).
Ингибиторы добавляли в культуру в точно известное время до ожидаемого наступления S-периода или митоза и регистрировали время наступления их задержки.
Слайд 10Результат 1. Запуск S-периода.
Если перед самым началом ожидаемого S-периода блокировать
Следовательно, для инициации репликации ДНК необходимо:
(1) перед самым началом S-периода – синтез какого-то белка, это SPF;
(2) мРНК для этого синтезируется за 1-2 ч до начала S;
(3) рРНК для рибосом, обеспечивающих этот синтез белка, образуется раньше, в G2-периоде предыдущего цикла.
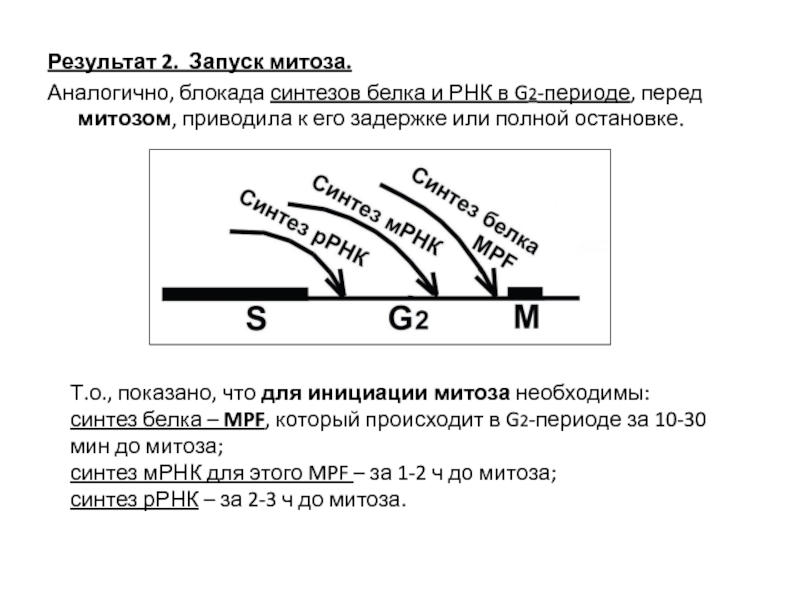
Слайд 11Результат 2. Запуск митоза.
Аналогично, блокада синтезов белка и РНК в G2-периоде,
Т.о., показано, что для инициации митоза необходимы:
синтез белка – MPF, который происходит в G2-периоде за 10-30 мин до митоза;
синтез мРНК для этого MPF – за 1-2 ч до митоза;
синтез рРНК – за 2-3 ч до митоза.
Слайд 12Т.о., ингибиторный анализ показал, что:
1) индукторы SPF и MPF вырабатываются
2) это белки, а значит – продукты определенных генов – регуляторов цикла;
3) активация и экспрессия регуляторных генов цикла происходит непосредственно перед началом контролируемого процесса –
S-фазы или митоза.
NB:
Начало S-периода и запуск митоза – две важнейшие контрольные точки (check points), имеющие генетическое управление.
Существуют ли другие контрольные точки и контролирующие их гены?
Существует ли «система домино», управляющая клеточным циклом?
Слайд 132.3. Генетические доказательства генной регуляции цикла. Генное семейство Сdc
Лучшее доказательство генной
У различных эукариот обнаружены циклоспецифические мутанты.
Дрожжи.
На дрожжах началось систематическое изучение генетики размножения клеток. Большой вклад внесли исследования лаборатории Hartwell’а (1968 – 1978, 1995 гг.).
Дрожжи имеют продолжительную гаплоидную стадию в жизненном цикле (связано с мейозом, образованием спор), что способствует выявлению рецессивных мутаций.
У дрожжей выявлено около 50 фенотипических мутаций по дефектам клеточного (митотического) цикла. Это значит, что не менее 50 генов управляют циклом.
Это семейство генов обозначено как гены cdc – cell division cycle.
Слайд 14В делении дрожжей различимы 3 относительно независимых цикла (как и у
других эукариот), и каждый из них имеет несколько мутаций (значит,
управляется несколькими генами). Ниже показаны только некоторые из них.
Стартовую точку и следующий митоз запускает ген cdc 28 (у почкующихся дрожжей) или его гомолог cdc 2 (у делящихся дрожжей).
Синтез ДНК инициирует ген cdc 8 (в хромосомном цикле).
Репродукция центриолей (у дрожжей – внутриядерные ЦОМТы) зависит от гена cdc 31 (в центросомном цикле).
При подготовке деления (почкования) ядра активен cdc 24, телофазу и цитокинез контролирует cdc 15 (в цитокинетическом цикле) и т.д..
Слайд 15Клетки млекопитающих.
В различных клеточных культурах выявлены циклоспецифические мутации, гомологичные cdc-мутациям
При нормальной температуре (37°) клетки делятся нормально. Но при пониженной (34°) или повышенной (39°) температуре клетки останавливаются в той или иной стадии цикла: возможны блок цитокинеза, блок анафазы, блок распада ядерной оболочки, блок перехода G1/S и другие. Значит, все эти процессы контролируются определенными генами.
Известно более 30 циклоспецифических мутантных (температурочувствительных) линий клеток млекопитающих. Всего, включая протоонкогены, определено более 100 генов, управляющих клеточным (митотическим) циклом.
Слайд 163. Гены компетентности к циклу (раннего ответа)
Гены myc, fos, myb и
Это ключевые гены пролиферации.
Под действием внешних факторов роста и гормонов (см. ниже), через
соответствующие цитоплазматические мессенджеры, эти гены
активируются и экспрессируют белки Myc, Fos, Myb, которые
активируют клетку к переходу G0/G1.
Клетка становится компетентной (способной) к митотическому циклу.
Т.о., гены компетентности работают в раннем пререпликативном
периоде. Соответствующие, белки Myc, Fos, Myb после синтеза
поступают из цитоплазмы (с рибосом) в ядро, где взаимодействуют с
хроматином и ядерным матриксом.
NB: англоязычные навания генов и белков принято писать по-разному:
гены – со строчной буквы курсивом (myc, fos, myb, cdc 8, cyclin D);
белки – с прописной буквы прямым шрифтом (Myc, Fos, Myb, Cyclin D), а для многословных названий – аббревиатурой (семейство киназ CDK, киназы Cdk1, Cdk2 …). Безымянные белки обозначают строчной буквой «p» (protein) и массой в kD (p21, p34, p53 …)
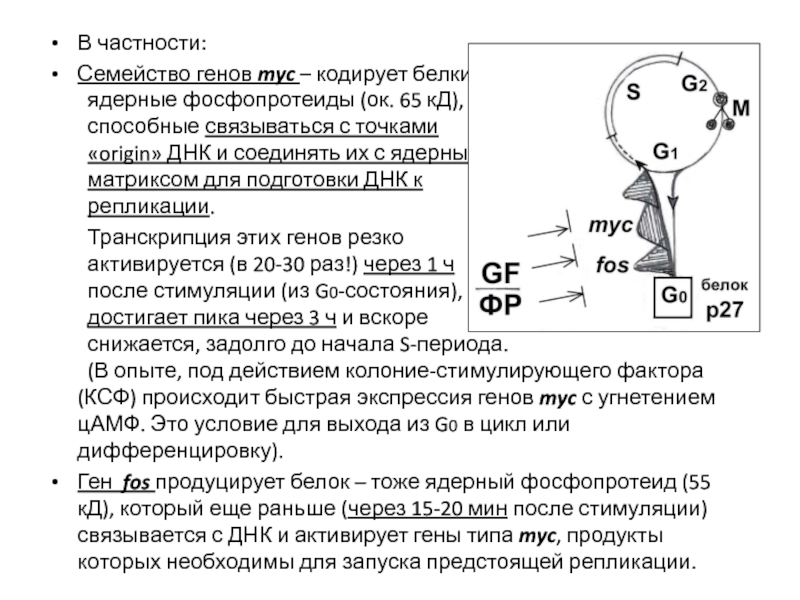
Слайд 17В частности:
Семейство генов myc – кодирует белки,
ядерные фосфопротеиды (ок. 65
способные связываться с точками
«origin» ДНК и соединять их с ядерным
матриксом для подготовки ДНК к
репликации.
Транскрипция этих генов резко
активируется (в 20-30 раз!) через 1 ч
после стимуляции (из G0-состояния),
достигает пика через 3 ч и вскоре
снижается, задолго до начала S-периода.
(В опыте, под действием колоние-стимулирующего фактора (КСФ) происходит быстрая экспрессия генов myc с угнетением цАМФ. Это условие для выхода из G0 в цикл или дифференцировку).
Ген fos продуцирует белок – тоже ядерный фосфопротеид (55 кД), который еще раньше (через 15-20 мин после стимуляции) связывается с ДНК и активирует гены типа myc, продукты которых необходимы для запуска предстоящей репликации.
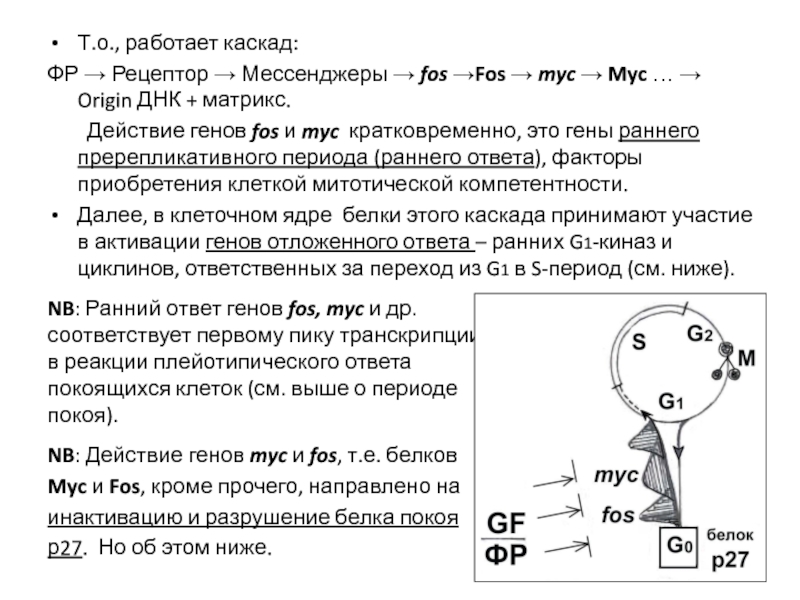
Слайд 18Т.о., работает каскад:
ФР → Рецептор → Мессенджеры → fos →Fos →
Действие генов fos и myc кратковременно, это гены раннего пререпликативного периода (раннего ответа), факторы приобретения клеткой митотической компетентности.
Далее, в клеточном ядре белки этого каскада принимают участие в активации генов отложенного ответа – ранних G1-киназ и циклинов, ответственных за переход из G1 в S-период (см. ниже).
NB: Ранний ответ генов fos, myc и др.
соответствует первому пику транскрипции
в реакции плейотипического ответа
покоящихся клеток (см. выше о периоде
покоя).
NB: Действие генов myc и fos, т.е. белков
Myc и Fos, кроме прочего, направлено на
инактивацию и разрушение белка покоя
р27. Но об этом ниже.
Слайд 194. Гены прогрессии цикла.
Циклины и циклинзависимые киназы
Для других генов
Это гены двух больших семейств – cdc (cell division cycle) и cyclin.
Открытие генов семейства cdc связано с изучением циклоспецифических мутантов дрожжей и культур клеток млекопитающих (см. выше). Позже эти работы были сопоставлены с открытием белкового фактора MPF в процессах созревания ооцитов и дробления зиготы лягушки.
Это интересная и драматичная история в изучении проблем репродукции и дифференцировки клеток.
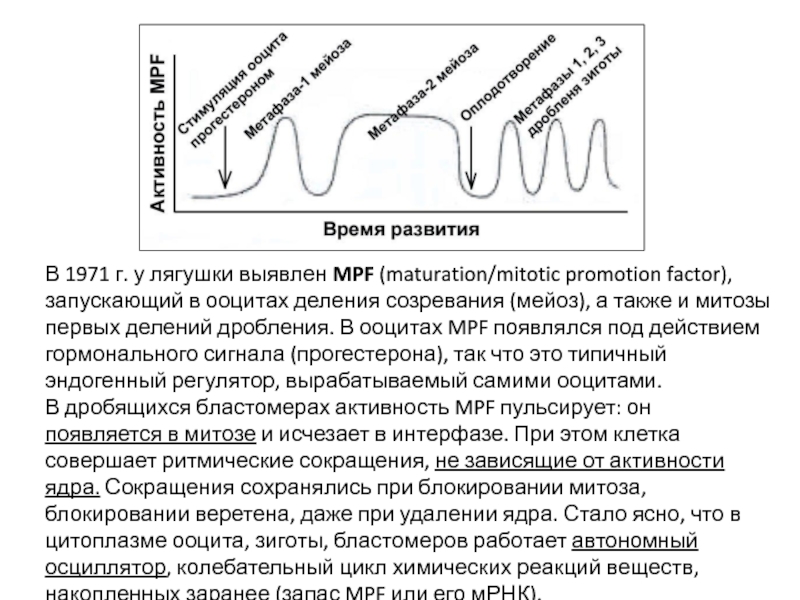
Слайд 20В 1971 г. у лягушки выявлен MPF (maturation/mitotic promotion factor), запускающий
В дробящихся бластомерах активность MPF пульсирует: он появляется в митозе и исчезает в интерфазе. При этом клетка совершает ритмические сокращения, не зависящие от активности ядра. Сокращения сохранялись при блокировании митоза, блокировании веретена, даже при удалении ядра. Стало ясно, что в цитоплазме ооцита, зиготы, бластомеров работает автономный осциллятор, колебательный цикл химических реакций веществ, накопленных заранее (запас MPF или его мРНК).
Слайд 21Так сформировались два конкурирующих (казалось – взаимоисключающих) представления о механизмах регуляции
Механизм генного «домино», представляющий конвейер генетических активностей семейства cdc, в котором каждый отработавший ген включает следующий ген митотического цикла (на основе работ с мутантными по циклу дрожжами и клеточными культурами).
Механизм цитоплазматического осциллятора («часовой механизм»), который заложен заранее и периодически включает весь комплекс биохимических и структурных реакций митоза (на основе работ с ооцитами лягушки и морских ежей).
Вскоре состоялся неожиданный синтез этих двух идей.
Слайд 22В 1980-х годах была установлена идентичность белков, инициирующих митоз в этих
белка-продукта гена cdc-2, запускающего митоз у дрожжей, и
одной из субъединиц MPF лягушки – белка p34, а также аналогичных белков и генов у других животных, включая человека.
Это оказалась одна и та же протеинкиназа – p34cdc-2 – фермент, фосфорилирующий (при расщеплении АТФ) разнообразные белки, участвующие в организации и течении митоза (см. ниже).
[Этим «золотым гвоздем» соединились две линии исследований, две, казалось, альтернативные теории регуляции митотического цикла.]
Вторая субъединица MPF была определена как белок-активатор киназы и названа Cyclin B (циклин Б). То есть, киназа p34 работает только в связке с циклином Б (гетеродимерная форма белка). Поэтому безымянный до тех пор фермент класса протеинкиназ - p34 - получил имя – Cdk1 (cyclin dependent kinaze 1 – циклин-зависимая киназа 1).
Cdk1 + Cyclin B = Cdk1/Cyclin B
Неактивные формы киназы и циклина = Активная димерная форма
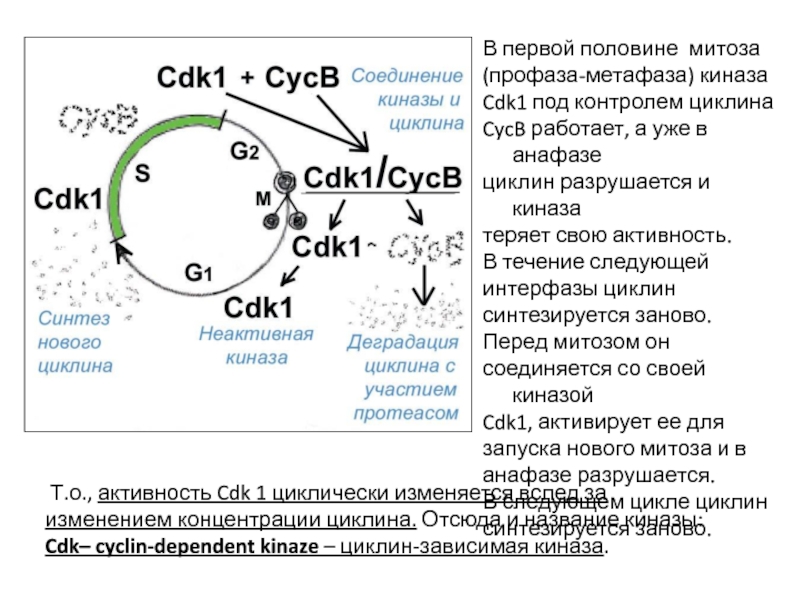
Слайд 23В первой половине митоза
(профаза-метафаза) киназа
Cdk1 под контролем циклина
CycB работает,
циклин разрушается и киназа
теряет свою активность.
В течение следующей
интерфазы циклин
синтезируется заново.
Перед митозом он
соединяется со своей киназой
Cdk1, активирует ее для
запуска нового митоза и в
анафазе разрушается.
В следующем цикле циклин
синтезируется заново.
Т.о., активность Cdk 1 циклически изменяется вслед за изменением концентрации циклина. Отсюда и название киназы:
Cdk– cyclin-dependent kinaze – циклин-зависимая киназа.
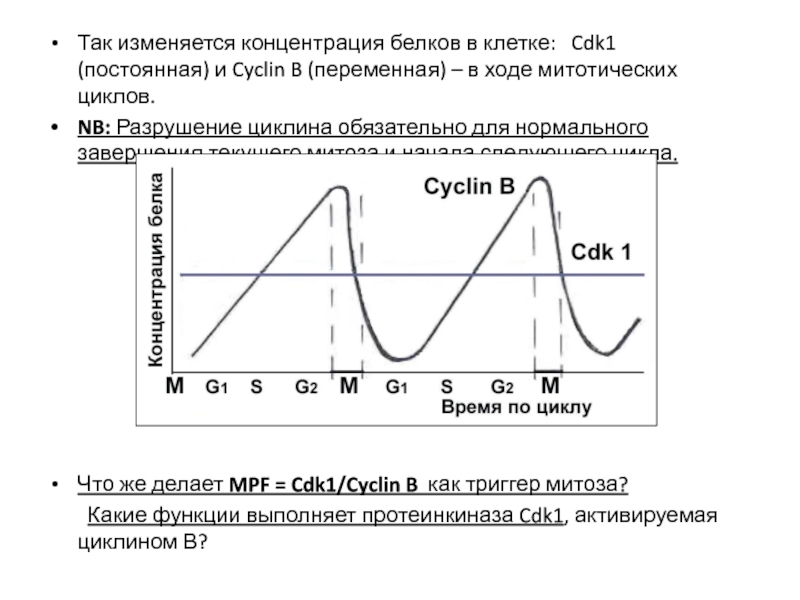
Слайд 24Так изменяется концентрация белков в клетке: Cdk1 (постоянная) и Cyclin
NB: Разрушение циклина обязательно для нормального завершения текущего митоза и начала следующего цикла.
Что же делает MPF = Cdk1/Cyclin B как триггер митоза?
Какие функции выполняет протеинкиназа Cdk1, активируемая циклином В?
Слайд 25Функции (активности) протеинкиназы Cdk1 в организации митоза:
1) фосфорилирует ламины ядерной оболочки
2) фосфорилирует белки конденсины и гистон Н1, способствуя конденсации хромосом;
3) фосфорилирует центросомный белок р225, способствуя сборке веретена;
4) активирует APC (anaphase promoting complex) – ферментная система, которая
- разрушает белок когезин хромосомных связок, делая возможным расхождение сестринских хроматид,
- запускает протеолитическую деградацию собственного циклина В (убиквитинация и расщепление ферментами протеасом).
Т.о., протеинкиназа Cdk1, активированная циклином В, после выполнения работы по запуску митоза сама же инициирует распад своего циклина и становится неактивной.
Эта реакция обеспечивает кратковременность действия MPF.
Так был расшифрован митотический осциллятор – MPF.
Слайд 26Но, как и следовало ожидать, вскоре были открыты и другие осцилляторы,
Это тоже протеинкиназы, белки-ферменты семейства CDK (2, 4, 6…) – продукты генов cdc, активируемые своими циклинами (A, C, D, E…).
Особенно важен SPF – комплекс Cdk2/Cyclin E,
обеспечивающий переход G1/S. Его функция –
фосфорилирование регуляторного белка pRb
(открыт как супрессор опухоли ретинобластомы,
но оказался универсальным супрессором любого
митотического цикла в точке перехода G1/S).
В активной (дефосфорилированной) форме pRb
блокирует фактор транскрипции E2F,
необходимый для синтеза белков, запускающих
и поддерживающих репликацию ДНК.
Т.о., фосфорилирование pRb с помощью киназы Cdk2 освобождает и
активирует фактор транскрипции E2F, разрешая начало синтеза ДНК.
Транскрипционный фактор E2F поддерживает также синтез самого циклина Е, обеспечивая поддержку репликации по всему S-периоду.
Слайд 28NB:
В раннем эмбриогенезе (дробление зиготы, бластула) работают в чистом виде
Это простейший митотический цикл – без G1-периода, часто и без G2.
В соматических клетках, начиная с гаструлы, включается морфогенетическая (транскрипционная) функция ядер, начинает работать вся система генетического контроля цикла.
У млекопитающих, по разным данным, это 7-12 видов Cdk и 9-14 видов циклинов.
При этом одна киназа может работать с несколькими циклинами и наоборот, так что регуляторный пул очень велик и многообразен.
Цикл удлиняется, появляются G1- и G0-периоды, необходимые для исправления возникающих мутаций и ошибок репликации, а также для ожидания сигналов к дифференцировке.
Слайд 295. Система контрольных точек и
ингибиторы митотического цикла
Т.о., события митотического цикла
При этом в нормальном цикле нарушение одной стадии обычно приводит к задержке следующих стадий, хотя далее возможно продолжение цикла с перескоком через стадию.
Например, если в температурочувствительных (ts) мутантах по ДНК-полимеразе остановлена репликация ДНК, то и митоз, и цитокинез останавливаются.
Почему в этих условиях не активируется Cdk1/CyclinB, не собирается веретено, не расходятся хромосомы?
В начале 1990-х годов выдвинута гипотеза (Хартвел и др., 1989-92), которая объясняло этот феномен.
Слайд 30 Гипотеза Хартвела:
В клетке существует контрольный механизм – система надзора за митотическим
Это система контрольных точек (check point) – короткие остановки на переходных стадиях цикла, в которых клетка с помощью специальных молекулярных сенсоров оценивает состояние своих структур, ферментов, ДНК на их готовность к дальнейшим шагам по циклу. Если обнаруживаются нарушения, вырабатывается негативный сигнал и цикл приостанавливается.
Число контрольных точек, по-видимому, равно числу промоторов Cdk/Cyclin. Сначала (дробление зиготы) активны 2 из них – для SPF и MPF. Позже (гаструляция) включаются остальные (у Xenopus от стадии 800-клеточного зародыша). Включение контрольных точек и есть реальная причина замедления циклов, появления G0-, G1-, G2-задержек.
Слайд 31Наиболее важен и сложен р53-р21/Waf1-pRb–зависимый путь (опухолевой супрессии), который останавливает клетки
При неполной или неправильной репликации, при повреждениях ДНК (например радиацией) с помощью специальных сигнальных белков (р19 и др.) активируется главный «сторож цикла» - белок р53 (фактор транскрипции), который активирует промотор и запускает ген для синтеза белка р21/Waf1 из семейства INK4 (от Inhibitor of Cdk). Этот р21 является универсальным ингибитором различных СD-киназ – подавляет активность Cdk1 (=блок митоза) или Cdk2,4,6 (=блок G1/S) до устранения разрывов и завершения репаративных синтезов ДНК.
Если ДНК не репарируется, р53 при достижении критической концентрации стимулирует синтез каспаз и запускает апоптоз.
Другой универсальный ингибитор CD-киназ – белок р27/Kip1 – обеспечивает более стойкое и глубокое блокирование Cdk2,4,6 и перевод клетки в период покоя G0. Преодоление этого блока, разрушение р27, возможно с участием белков/генов компетентности Mycmyc, Fosfos… (см. выше) под влиянием факторов роста и гормонов (см. далее).
Прочие ингибиторы цикла (CKI): из семейства KIP – р57; из семейства INK4 – р15, р16, р18, р19.
Слайд 32NB: Транскрипционный фактор р53 участвует также в запуске синтезов мРНК (и,
Слайд 33И еще одно важное NB:
Все гены белков-стимуляторов и промоторов
Соответственно, все гены белков-ингибиторов цикла (белков CKI, особенно р53 – сторож цикла, pRb и др.) должны быть обозначены как антионкогены, в онкологии это опухолевые супрессоры. Однако их мутации, недостача, утрата в результате неправильного митоза – тоже путь к опухолевой трансформации клеток, причем гораздо более короткий и радикальный, чем накопление мутаций протоонкогенов. Достаточно одной р53-дефицитной клетки, чтобы породить мутантный клеточный клон и быстро растущую раковую опухоль.
Но это отдельная большая тема, можно сказать, специальная медико-биологическая наука – онкобиология. Ее изучение за пределами нашего спецкурса.
Слайд 346. Факторы роста
Сколько бы генов не было задействовано в обеспечении цикла
Исторически идея стимуляции митозов развивалась через ряд теорий.
Теория митогенетических лучей (полей), испускаемых яйцеклеткой, зиготой, зародышем (Гурвич, 1930-е годы).
Теория некрогормонов (1950-е годы), согласно которой поврежденные клетки освобождают активные митогенные вещества – стимуляторы пролиферации (некрогормоны, раневые гормоны). Это – продукты распада белков или НК.
Современное представление о «факторах роста», которые совместно с гормонами управляют размножением и дифференцировкой клеток. Сегодня этой системе отводится центральная роль в организации роста и морфогенезов.
Слайд 35Действие ФР в чистом виде можно изучать на клеточных культурах in
Давно известно, что для роста клеточных культур в искусственную питательную среду необходимо добавлять 5-10% сыворотки крови, лучше фетальной (эмбриональной, плодной). В ней содержатся различные биогенные стимуляторы, которые и были названы факторами роста. Для растительных культур это – соответствующие гормоны роста (ауксины и др.).
Без этих факторов клетки не размножаются, переходят в G0-, реже в G2-период.
Слайд 366.1. Общие свойства и механизм действия факторов роста (ФР-GF)
1) ФР синтезируются
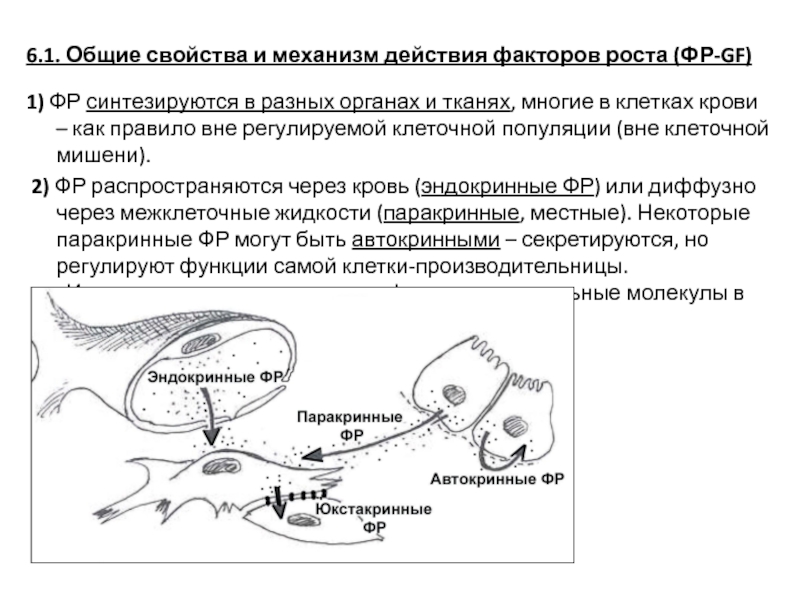
2) ФР распространяются через кровь (эндокринные ФР) или диффузно через межклеточные жидкости (паракринные, местные). Некоторые паракринные ФР могут быть автокринными – секретируются, но регулируют функции самой клетки-производительницы.
Известны также юкстакринные факторы – сигнальные молекулы в форме
интегральных
белков плазмалеммы
(не секретируются,
действуют контактно
на рецепторы
соседних клеток).
Слайд 373) ФР присутствуют в ткани и работают в очень малых концентрациях
4) ФР действуют, как правило, на несколько функционально связанных типов клеток – относительно тканеспецифично.
5) ФР – это несколько семейств полипептидов, многие с тремя -S-S-связями (6 остатков цистеина) (гомология в пределах семейства).
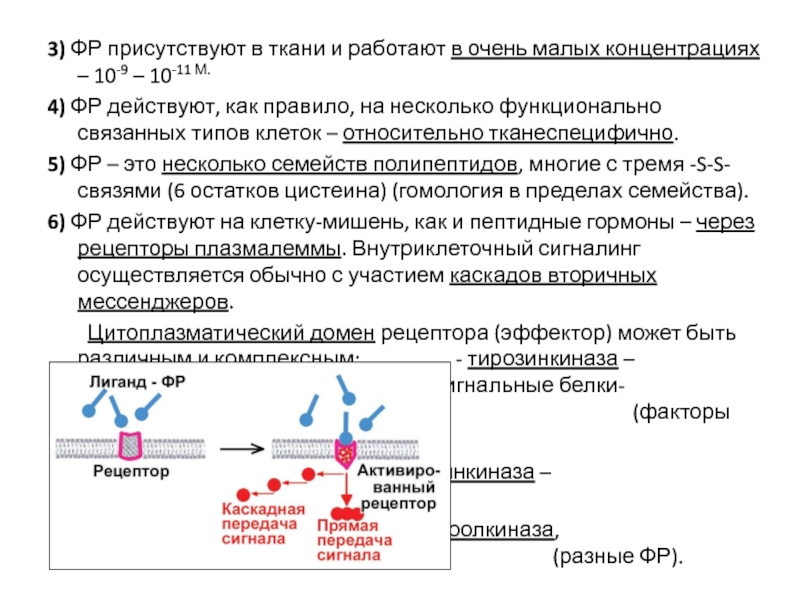
6) ФР действуют на клетку-мишень, как и пептидные гормоны – через рецепторы плазмалеммы. Внутриклеточный сигналинг осуществляется обычно с участием каскадов вторичных мессенджеров.
Цитоплазматический домен рецептора (эффектор) может быть различным и комплексным: - тирозинкиназа – фосфорилирует сигнальные белки- мессенджены по тирозину (факторы FGF, EGF, IGF и др.);
- серин-треонинкиназа – по серину и треонину (TGF-β);
- диацилглицеролкиназа, фосфолипаза С и другие (разные ФР).
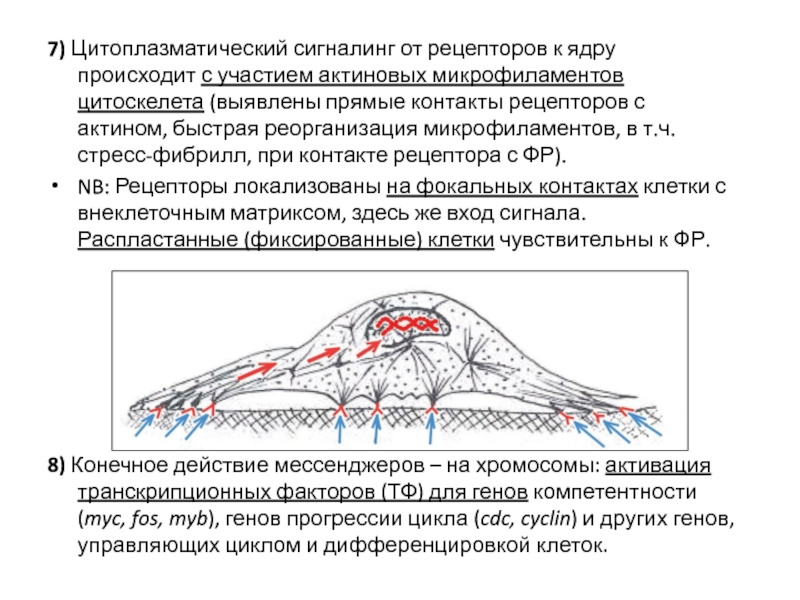
Слайд 387) Цитоплазматический сигналинг от рецепторов к ядру происходит с участием актиновых
NB: Рецепторы локализованы на фокальных контактах клетки с внеклеточным матриксом, здесь же вход сигнала. Распластанные (фиксированные) клетки чувствительны к ФР.
8) Конечное действие мессенджеров – на хромосомы: активация транскрипционных факторов (ТФ) для генов компетентности (myc, fos, myb), генов прогрессии цикла (cdc, cyclin) и других генов, управляющих циклом и дифференцировкой клеток.
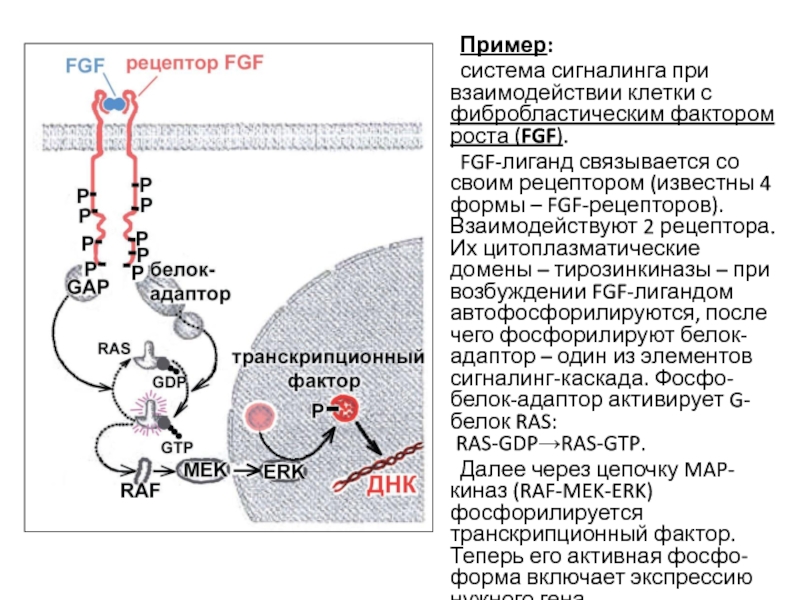
Слайд 39 Пример:
система сигналинга при взаимодействии клетки с фибробластическим фактором роста (FGF).
FGF-лиганд связывается со своим рецептором (известны 4 формы – FGF-рецепторов). Взаимодействуют 2 рецептора. Их цитоплазматические домены – тирозинкиназы – при возбуждении FGF-лигандом автофосфорилируются, после чего фосфорилируют белок-адаптор – один из элементов сигналинг-каскада. Фосфо-белок-адаптор активирует G-белок RAS:
RAS-GDP→RAS-GTP.
Далее через цепочку MAP-киназ (RAF-MEK-ERK) фосфорилируется транскрипционный фактор. Теперь его активная фосфо-форма включает экспрессию нужного гена.
Слайд 40Активированная рецепторная тирозинкиназа (RTK) стимулирует также фосфолипазу С, которая расщепляет фосфатидилинозитолдифосфат
NB: Как правило, ФР регулируют не только репродукцию клеток, но и их дифференцировку, выступая не только стимуляторами митоза, но где-то и ингибиторами.
Т.е. ФР в целом контролируют весь морфогенез.
Слайд 416.2. Разнообразие факторов роста
Известны десятки семейств ФР (GF). Рассмотрим некоторые, наиболее
1. EGF – Epidermal Growth Factor; = ЭФР – Эпидермальные ФР.
Полипептид из 53 аминокислот, включающий 6 остатков цистеина, т.е. 3 S-S-мостика. Сигналинг через тирозинкиназный эффектор, белок-адаптор и цепочку киназ (как показано выше).
Основной источник: синтезируется и выделяется в кровь клетками протока подчелюстной слюнной железы (здесь же ФРН – фактор роста нервов).
Мишени: деление эпидермоцитов, фибробластов дермы и др. клеток.
Дополнительный источник: клетки стромы и теки яичника.
Мишень: клетки гранулёзы фолликулов.
Хороший пример взаимодействия эпителия и соединительной ткани.
NB: ЭФР уже используется при выращивании in vitro кожных пластов для имплантации в заместительной терапии.
Слайд 422. PDGF – Plate Dependent Growth Factor; = ТФР – Тромбоцитарные
Разновидности из 2 цепей по 125 (А) и 160 (В) аминокислот: АА, АВ, ВВ.
Источник: кровяные пластинки (тромбоциты).
Мишени: стимулируют размножение гладкомышечных клеток поврежденных сосудов, а также фибробластов и нейроглии в очаге повреждения (и в культуре).
NB: регулирует комплекс функционально связанных клеток.
3. FGF – Fibroblast Growth Factor; = ФРФ – Фибробластные ФР.
Название возникло от первого обнаруженного фактора этого семейства, который стимулировал размножение культуры клеток фибробластов.
Это – обширное семейство FGF-белков, синтезируемых с соответствующих генов fgf, насчитывающее много представителей (до 19 у млекопитающих) и сотни изоформ от альтернативного сплайсинга.
Основные формы: FGF-1 – кислый, 140 аминокислот. FGF-2 – основный (щелочной), 146 аминокислот.
Мишени: стимулируют размножение многих типов клеток, в основном из мезенхимного ряда: фибробластов, эндотелия, миобластов, мезенхимы, но также клеток тимуса, печени.
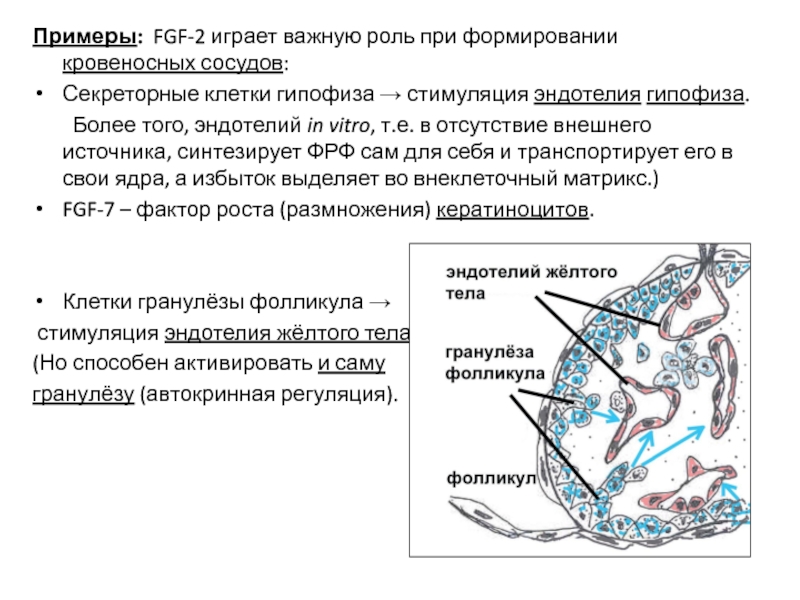
Слайд 43Примеры: FGF-2 играет важную роль при формировании кровеносных сосудов:
Секреторные клетки гипофиза
Более того, эндотелий in vitro, т.е. в отсутствие внешнего источника, синтезирует ФРФ сам для себя и транспортирует его в свои ядра, а избыток выделяет во внеклеточный матрикс.)
FGF-7 – фактор роста (размножения) кератиноцитов.
Клетки гранулёзы фолликула →
стимуляция эндотелия жёлтого тела.
(Но способен активировать и саму
гранулёзу (автокринная регуляция).
Слайд 444. SDGF-1 – Spleen Dependent Growth Factor; = ФР из селезенки.
Гомологичен с ФРФ.
Источник: клетки селезенки.
Мишени: стимулирует пролиферацию гепатоцитов, фибробластов, эндотелия.
В целом стимулирует рост печени.
5. IGF-I, IGF-II – Insulin-like Growth Factor; = ИФР – Инсулиноподобный ФР.
2 основные формы – 70 и 73 аминокислот.
Действует совместно с ТФР и ЭФР.
Стимулирует размножение соединительно-тканных и жировых клеток.
6. Остеопоэтин.
Из клеток красного костного мозга.
Стимулирует пролиферацию остеобластов.
Слайд 457. Гемопоэтические ФР.
Эритропоэтин.
Источник: юкстагломерулярные клетки почек. Мишень: эритробласты (эритропоэз).
Гранулоцитопоэтин.
Источник: строма костного мозга. Мишень: миелоидные бласты (миелопоэз).
Тимопоэтин.
Источник: строма тимуса. Мишень: лимфобласты в тимусе.
Интерлейкины (цитокины) и лимфокины (колониестимулирующие факторы).
Участвуют в реакциях клеточного иммунитета, стимулируют размножение и дифференцировку лимфоцитов.
8. TGF-α – Transforming Growth Factor-α; = ТФР-α – Трансформирующий ФР-α.
30% гомологии с ЭФР, содержит 6 остатков цистеина. Взаимодействует с теми же рецепторами.
Выделен из раковых опухолей (т.е. из трансформированных клеток). Но работает и в нормальном эмбриональном развитии: в клетках плаценты, печени (стимулирует овальные стволовые клетки печени).
Т.е., TGF-α – нормальный ФР раннего развития и регенерации. В опухолях активируется вторично.
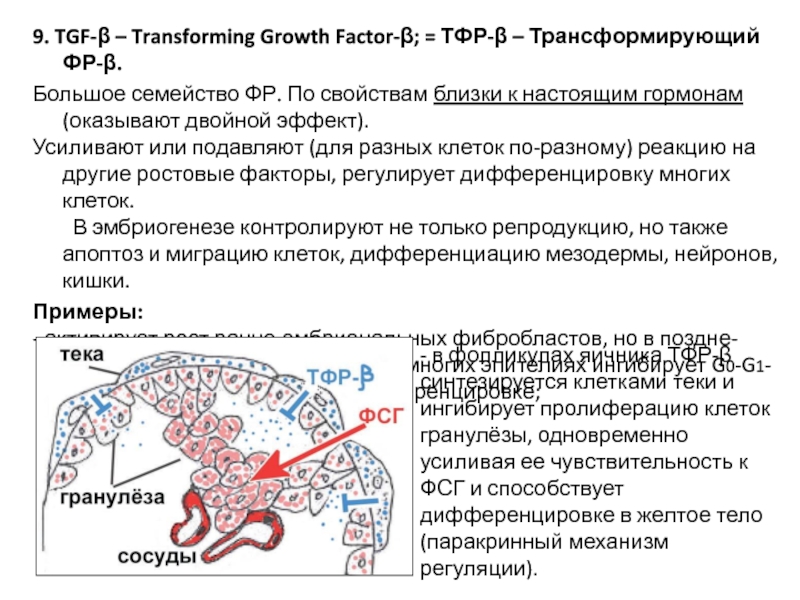
Слайд 469. TGF-β – Transforming Growth Factor-β; = ТФР-β – Трансформирующий ФР-β.
Большое семейство ФР. По свойствам близки к настоящим гормонам (оказывают двойной эффект).
Усиливают или подавляют (для разных клеток по-разному) реакцию на другие ростовые факторы, регулирует дифференцировку многих клеток.
В эмбриогенезе контролируют не только репродукцию, но также апоптоз и миграцию клеток, дифференциацию мезодермы, нейронов, кишки.
Примеры:
- активирует рост ранне-эмбриональных фибробластов, но в поздне-эмбриональных фибробластах и многих эпителиях ингибирует G0-G1-переход и способствует их дифференцировке;
- в фолликулах яичника ТФР-β синтезируется клетками теки и ингибирует пролиферацию клеток гранулёзы, одновременно усиливая ее чувствительность к ФСГ и способствует дифференцировке в желтое тело (паракринный механизм регуляции).
Слайд 4710. SDGF – Shwannomous Dependent Growth Factor – ФР из шванномы.
Еще один пример гормоноподобного (двойственного) действия ФР.
Является митогеном (стимулятором размножения) нейроглии и фибробластов оболочек нервов. Но одновременно индуцирует дифференцировку нейронов и образование их аксонов (индуцирует синтез мРНК и специальных белков для роста аксонов).
…………………………………
В целом, факторы роста в разных условиях, концентрациях и комбинациях могут работать и как стимуляторы, и как ингибиторы пролиферации, управляя ростом и специализацией зачатков, тканей, органов.
Тканеспецифичность факторов роста тоже относительна, как и у гормонов. Клетки реагируют, как правило, не на один ФР, а на специфическую комбинацию ФР и гормонов.
Разнообразие ФР не так велико, но комбинаций очень много – на разные типы клеточной спецификации (дифференцировки).
Слайд 486.3. Факторы роста препятствуют старению и гибели клеток
Для многих клеток в
Фибробласты от плода человека переживают до 50 пассажей, т.е. удвоений популяции;
Фибробласты от 40-летнего человека – до 40 пассажей;
Фибробласты от 80-летнего человека – до 30 пассажей.
(NB: потенциальный возраст истощения соединительных тканей человека – 200 лет).
Оказалось, что старение клеток и отмирание культуры ускоряется при недостатке ФР и, наоборот, замедляется при их избытке.
Примеры:
Слайд 49Культура эпидермиса ребенка на обычной среде с сывороткой дает 50 циклов
«Бессмертные» клетки перевиваемой линии 3Т3 при недостатке в среде факторов роста все же проявляют признаки старения.
(ФР поддерживают активность теломеразных генов?)
Клетки эмбриона мыши на обычной среде с сывороткой тоже дают ограниченное число поколений, а в присутствии очищенных ФР (вместо сыворотки) растут без признаков старения. Но при добавлении сыворотки рост останавливается.
Т.о., старение клеточной популяции (частично) обусловлено какими-то компонентами сыворотки, которые перевешивают действие ростовых факторов.
Фибробласты от больных синдромом Вернера (преждевременное старении в 40-50 лет, наследуемое) быстро стареют в культуре (дают мало циклов удвоения). Они оказались не чувствительны к ТФР (PDGF) и ФРФ (FGF) – мутация с утратой рецепторов?
Слайд 50Т.о., с факторами роста могут быть связаны причины старения тканей, органов
(наряду с другими):
1) утрата клетками рецепторов к ФР (мутации);
2) снижение выработки ФР;
3) снижение выработки гормонов, управляющих синтезом ФР (эндокринное старение).
Слайд 517. Гормоны и пролиферация клеток
В отличие от факторов роста настоящие гормоны
Биохимически различаются три группы гормонов:
моноамины,
стероиды,
пептиды.
Роль гормонов состоит в регуляции роста, развития и функционирования органов и тканей, включая регуляцию клеточного размножения и дифференцировки.
Слайд 527.1. Моноамины
Моноаминовые гормоны образуются из аминокислот путем небольшой перестройки. Это –
Тирозин → норадреналин, адреналин (катехоламины мозгового вещества надпочечников), тироксин (гормон щитовидной железы).
Норадреналин – стимулятор, сокращает клеточный цикл в различных тканях.
Адреналин – действует на другие рецепторы и подавляет клеточное размножение, работает как универсальный ингибитор пролиферации. При этом запускает в организме комплексную стрессовую реакцию.
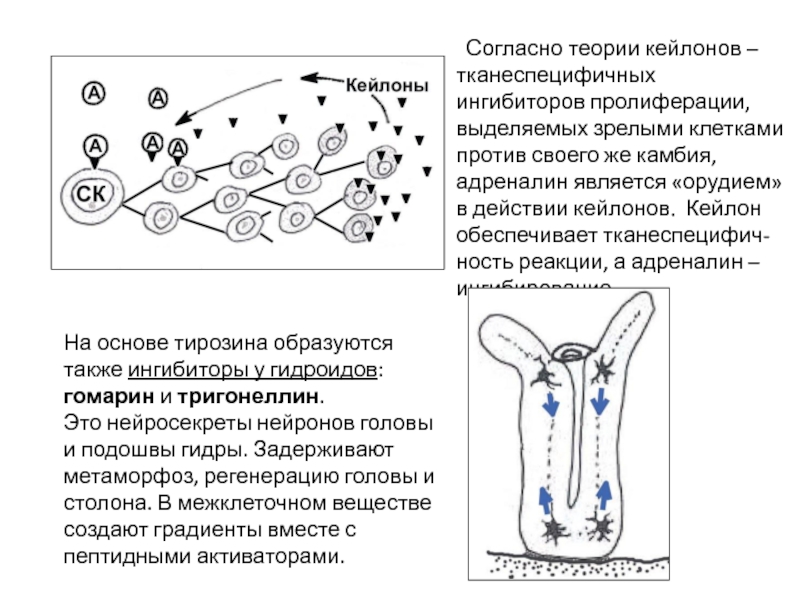
Слайд 53 Согласно теории кейлонов – тканеспецифичных ингибиторов пролиферации, выделяемых зрелыми клетками против
На основе тирозина образуются также ингибиторы у гидроидов: гомарин и тригонеллин.
Это нейросекреты нейронов головы и подошвы гидры. Задерживают метаморфоз, регенерацию головы и столона. В межклеточном веществе создают градиенты вместе с пептидными активаторами.
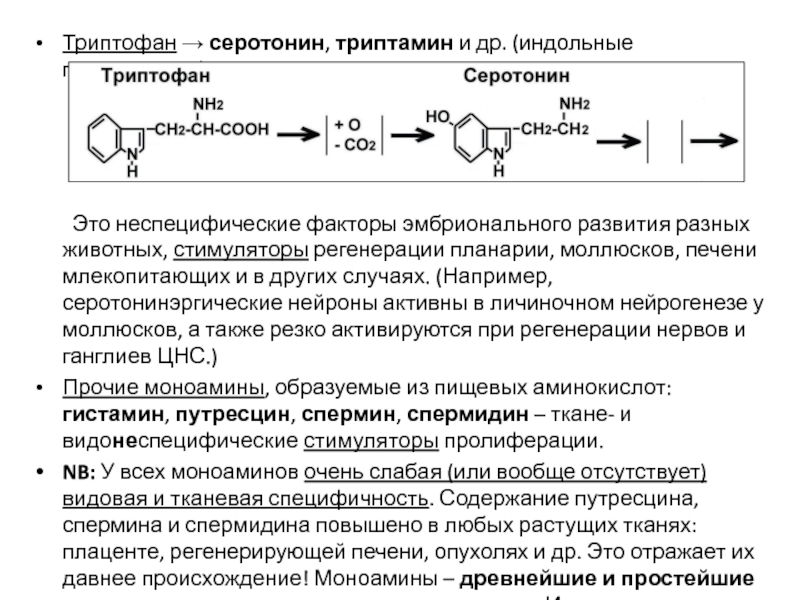
Слайд 54Триптофан → серотонин, триптамин и др. (индольные производные).
Это неспецифические факторы эмбрионального
Прочие моноамины, образуемые из пищевых аминокислот: гистамин, путресцин, спермин, спермидин – ткане- и видонеспецифические стимуляторы пролиферации.
NB: У всех моноаминов очень слабая (или вообще отсутствует) видовая и тканевая специфичность. Содержание путресцина, спермина и спермидина повышено в любых растущих тканях: плаценте, регенерирующей печени, опухолях и др. Это отражает их давнее происхождение! Моноамины – древнейшие и простейшие регуляторы клеточного размножения и роста. Имеются уже у цианобактерий.
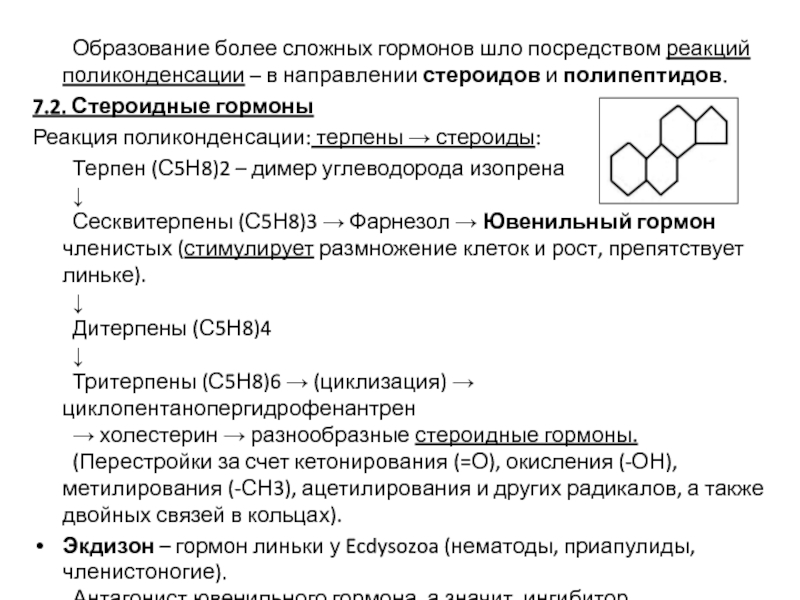
Слайд 55 Образование более сложных гормонов шло посредством реакций поликонденсации – в направлении
7.2. Стероидные гормоны
Реакция поликонденсации: терпены → стероиды:
Терпен (С5Н8)2 – димер углеводорода изопрена
↓
Сесквитерпены (С5Н8)3 → Фарнезол → Ювенильный гормон членистых (стимулирует размножение клеток и рост, препятствует линьке).
↓
Дитерпены (С5Н8)4
↓
Тритерпены (С5Н8)6 → (циклизация) → циклопентанопергидрофенантрен
→ холестерин → разнообразные стероидные гормоны.
(Перестройки за счет кетонирования (=О), окисления (-ОН), метилирования (-СН3), ацетилирования и других радикалов, а также двойных связей в кольцах).
Экдизон – гормон линьки у Ecdysozoa (нематоды, приапулиды, членистоногие).
Антагонист ювенильного гормона, а значит, ингибитор пролиферации.
Слайд 56Кортикостероиды – гормоны коры надпочечников позвоночных.
Функционально
Характерен двойственный эффект (±) в зависимости от дополнительных факторов.
Например, гидрокортизон в чистом виде (без сыворотки) усиливает действие EGF на клетки HeLa (способствует связыванию ФР с клеточными рецепторами), но в присутствии сыворотки (т.е. в сумме с другими ФР) ингибирует размножение тех же клеток.
Тот же гидрокортизон на фибробластах 3Т3 усиливает действие EGF (работает как синергист ФР), но ингибирует действие FGF (антагонист ФР). Дексаметазон вместе с сывороткой стимулирует миобласты, но ингибирует фибробласты.
Половые гормоны.
Мужские половые гормоны семенников (частично коры надпочечников, яичников): тестостерон, андростерон и др.
Женские гормоны яичников (частично семенников, коры надпочечников): прогестерон, эстрадиол, эстрон и др.
Кроме прочего, стимулируют мейоз – запускают сигнальный путь на синтез MPF.
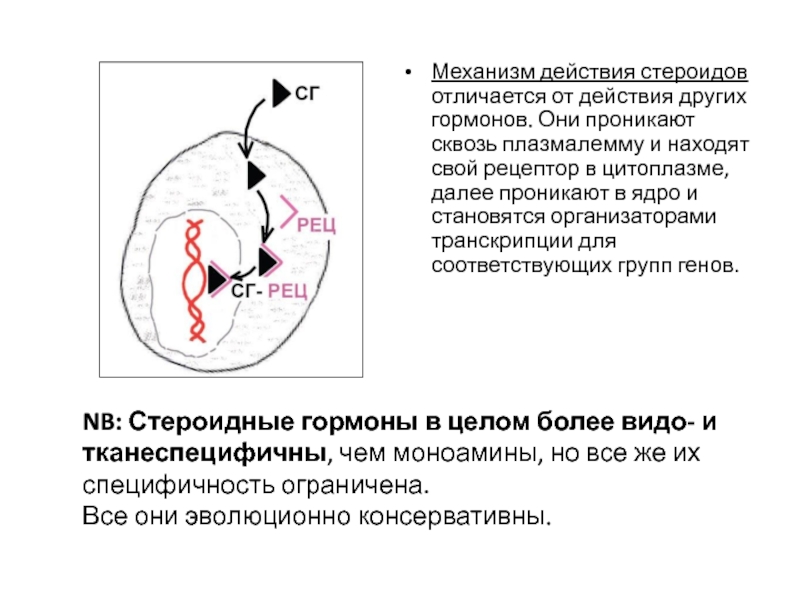
Слайд 57Механизм действия стероидов отличается от действия других гормонов. Они проникают сквозь
NB: Стероидные гормоны в целом более видо- и тканеспецифичны, чем моноамины, но все же их специфичность ограничена.
Все они эволюционно консервативны.
Слайд 587.3. Пептидные гормоны
Имеются уже у низших многоклеточных.
ПМГ – пептидный морфоген гидры
нейропептид из 11 аминокислот.
Секретируется нейронами «головы» и
стимулирует деление стволовых (i) клеток,
которые дают в первую очередь новые нейроны,
потом эпителий (ПМГ – активатор головы).
Вместе с активатором подошвы, а также
моноаминовыми ингибиторами (см. выше)
создает морфогенетические градиенты (поля)
вдоль тела гидры, направляющие векторный
рост и регенерацию: от подошвы растет голова,
от головы – подошва.
NB: ПМГ еще малоспецифичен, его гомологи есть у других животных.
ПМГ активен даже в отношении клеток млекопитающих. Используется в медицине для стимуляции роста легочного, кожного и других эпителиев.
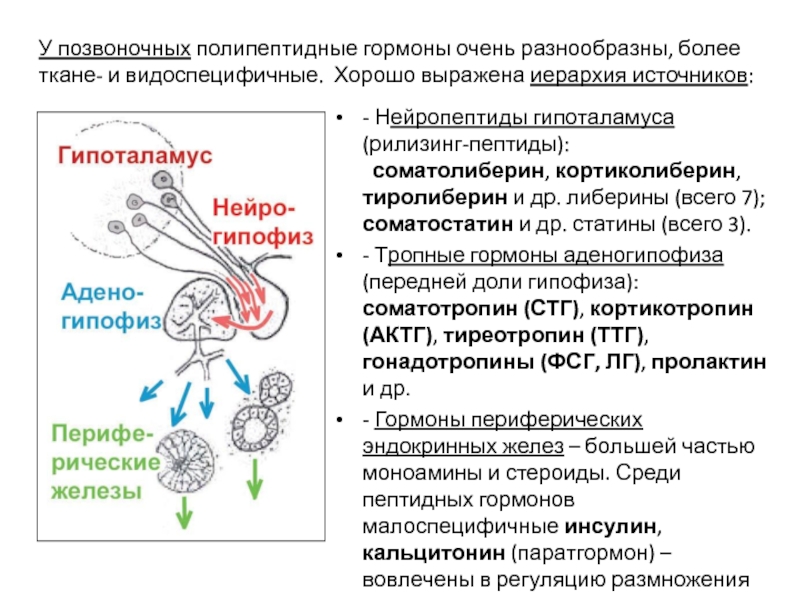
Слайд 59- Нейропептиды гипоталамуса (рилизинг-пептиды):
соматолиберин, кортиколиберин, тиролиберин и др. либерины (всего
- Тропные гормоны аденогипофиза (передней доли гипофиза): соматотропин (СТГ), кортикотропин (АКТГ), тиреотропин (ТТГ), гонадотропины (ФСГ, ЛГ), пролактин и др.
- Гормоны периферических эндокринных желез – большей частью моноамины и стероиды. Среди пептидных гормонов малоспецифичные инсулин, кальцитонин (паратгормон) – вовлечены в регуляцию размножения клеток в красном костном мозге, тимусе, печени и др.
У позвоночных полипептидные гормоны очень разнообразны, более ткане- и видоспецифичные. Хорошо выражена иерархия источников:
Слайд 607.4. Комплексное действие гормонов и других регуляторов
Важно то, что один и
Слайд 61При этом сами регуляторы встроены в сложные иерархические цепи (сети) управления
Например, сеть управления через СТГ (соматотропный гормон) включает:
ГИПОТАЛАМУС ЭПИФИЗ
↓ ↓ ↓
рилизинг-пептиды ↓
↓соматолиберин – (стимуляция) → (+) ГИПОФИЗ (+) ← серотонин – (стимуляция)
соматостатин – (угнетение) →→→ (–) ↓ ↓ ↓
СТГ ТТГ АКТГ и др.
↓↓↓
Пролиферация гепатоцитов, энтероцитов и др.
Стимулирует выделение печенью соматомедина -
- ускоряет рост костной и др. тканей.
Стимулирует образование в тканях полиаминов –
- неспецифическая стимуляция…
Причем в сетях возможны каскадные реакции превращения неактивных форм регулятора в активные и наоборот, с участием разнообразных ферментов, например:
кортизон → кортизол (= гораздо более сильный стимулятор);
норадреналин → адреналин (= смена стимуляции на угнетение).
Слайд 62Таким образом, гормоны включены в кооперативное действие всех регуляторов пролиферации и
Система экзогенной регуляции пролиферативных процессов и дифференцировки клеток многоклеточных организмов усложнялась в ходе биологической эволюции.
У высших животных клеточная пролиферация в тканях регулируется сочетанием филогенетически древних факторов – видо- и тканенеспецифических (амины, стероиды) и более молодых – специфичных (полипептидные гормоны и факторы роста). При этом действие древних неспецифических факторов становилось подчиненным, они использовались как усилители сигналов от новых, более ткане- и видоспецифичных регуляторов. Т.е. специфические регуляторы (полипептидные гормоны и ФР) в ходе эволюции дополняли систему регуляции, которая изначально (у одноклеточных) была довольно примитивной – неспецифической. Появлялись и соответствующие наборы клеточных рецепторов, усложнялись межклеточные и межтканевые взаимодействия.
Слайд 63Заключение
В целом получается такая система регуляции клеточного размножения.
1) Клетка генетически
Синтез белков – стимуляторов клеточного цикла (Cdk) идет постоянно, и вместе с соответствующими циклинами они задают график течения цикла. Главные из них (и минимально достаточные) – белки SPF (Cdk2/Cyclin E) и MPF (Cdk1/Cyclin B).
2) Но в клетке есть и гены негативного контроля цикла, экспрессирующие белки-ингибиторы циклинзависимых киназ (CKI): p19, p21, p27,…p53, p57, pRb, а также TGF β, интерферон и другие ингибиторы.
В G1-периоде каждого очередного цикла (в точке r, check point) эти белки подавляют гены подготовки нового синтеза ДНК (cdk 6, 4, 2, cyclin D, E) и направляют клетку в период покоя G0.
Слайд 643) У одноклеточных переход через точку r в новый цикл регулируется
У первых многоклеточных экзогенные индукторы – моноамины, стероиды, олигопептиды – дополнили систему регуляции, и далее она усложнялась с участием нейросекреторных, эндокринных (гормоны) и паракринных (факторы роста) полипептидов.
Факторы роста через рецепторы и внутриклеточные мессенджеры активируют транскрипционные факторы (ТФ) генов компетентности (myc, fos, myb и др.); экспрессируемые этими генами белки блокируют белки-ингибиторы (прежде всего p27), изменяют структуру хроматина и выводят клетку из состояния покоя G0.
Слайд 654) Другие факторы роста аналогичными путями повышают экспрессию генов прогрессии цикла
5) Гормоны и пептидные ингибиторы модифицируют (подавляют или усиливают) действие факторов роста, регулируя переходы к дифференцировке клеток и апоптозу.
Т.о., у высших многоклеточных животных, с их сложной органно-тканевой структурой, в экзогенной регуляции клеточного размножения факторы роста специализируют действие гормонов и других неспецифических регуляторов. Центральная нервная система (через гипоталамус) и факторы внешней среды выступают как еще более удаленные эпигенетические регуляторы роста и развития.