- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Ферменты. Уравнение Михаэлиса-Ментен презентация
Содержание
- 1. Ферменты. Уравнение Михаэлиса-Ментен
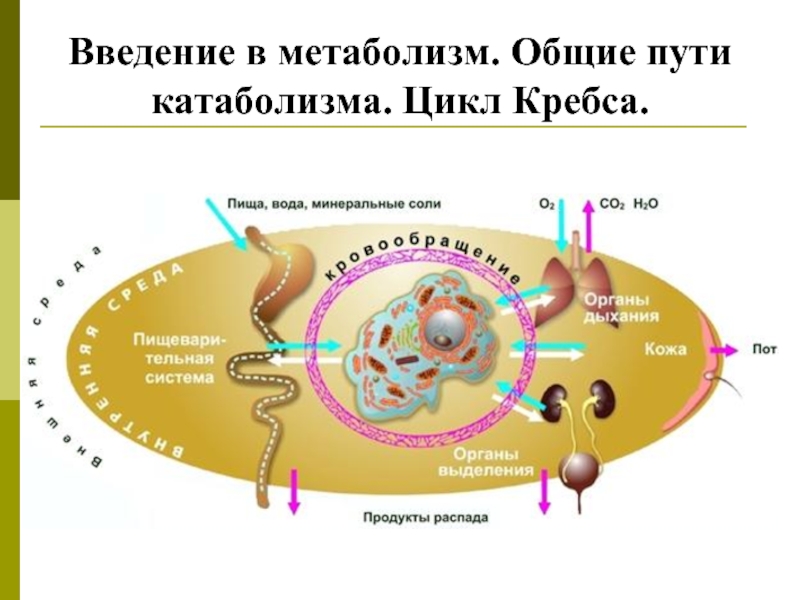
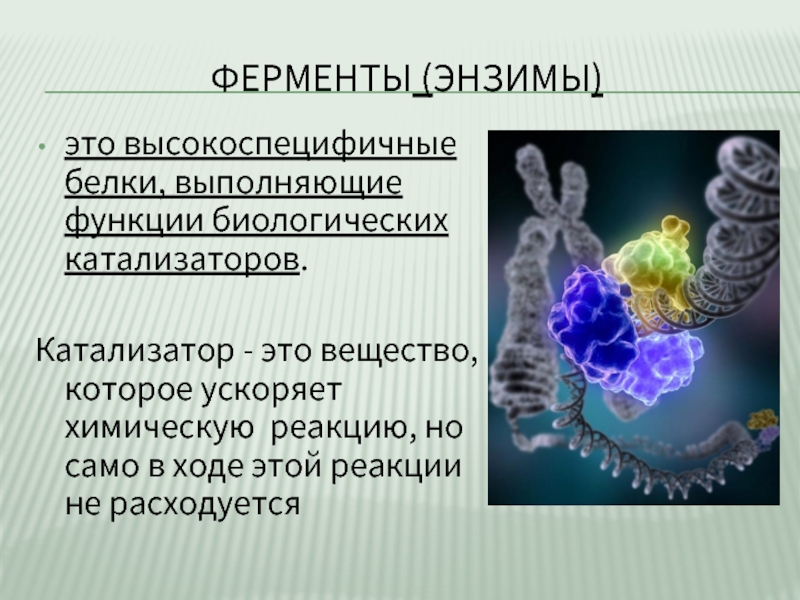
- 2. ФЕРМЕНТЫ (ЭНЗИМЫ) это высокоспецифичные белки, выполняющие функции
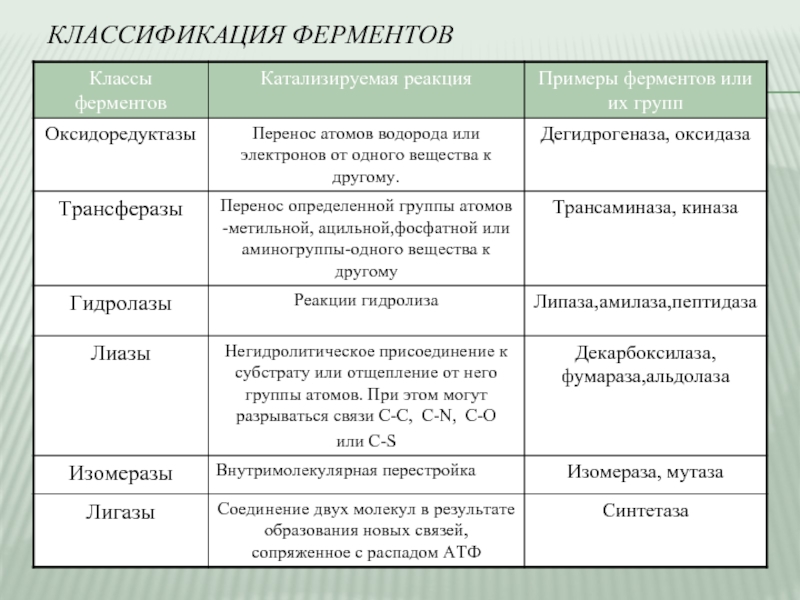
- 3. КЛАССИФИКАЦИЯ ФЕРМЕНТОВ
- 4. Белок~кофактор белок кофактор Связь может
- 5. Энергия исходных продуктов
- 6. Связывание фермента с субстратом происходит в
- 7. Высокая избирательность действия фермента обеспечивается тем,
- 8. Способы регуляции: 1. Аллостерическая регуляция
- 9. 1. Аллостерическая регуляция эффектор Каталитическая субъединица
- 10. 2. Ковалентная модификация Неактивный Е СН2ОН Акт.Е
- 11. Регуляция действия ферментов E4 E3 E2 E1
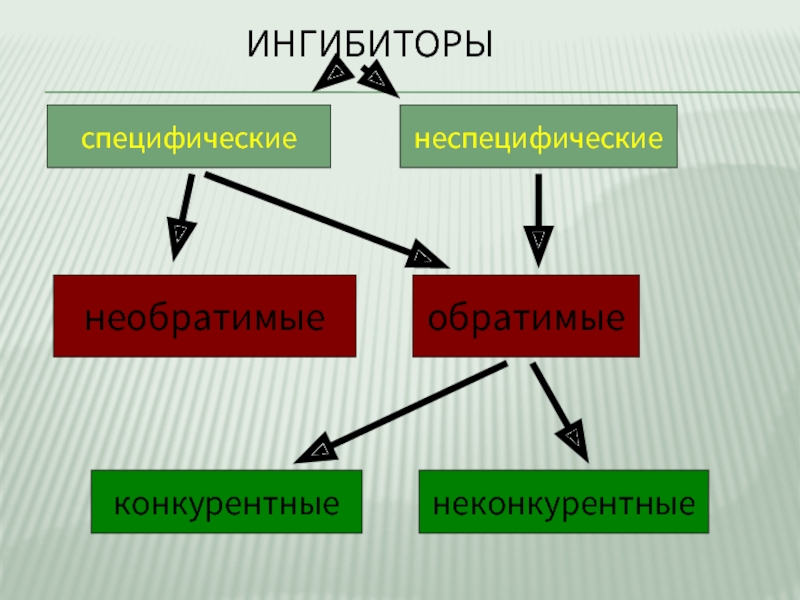
- 12. ИНГИБИТОРЫ специфические неспецифические обратимые необратимые конкурентные неконкурентные
- 13. Необратимое ингибирование путем ковалентной модификации Фермент -
- 14. Обратимое ингибирование ферментов Конкурентное ингибирование Неконкурентное ингибирование
- 15. Иммобилизация фермента - закрепление на полимерном
- 16. Каждый фермент имеет определенный оптимум рН Относи-
- 17. Оптимальная температура 00 700 Активность ферментов зависит
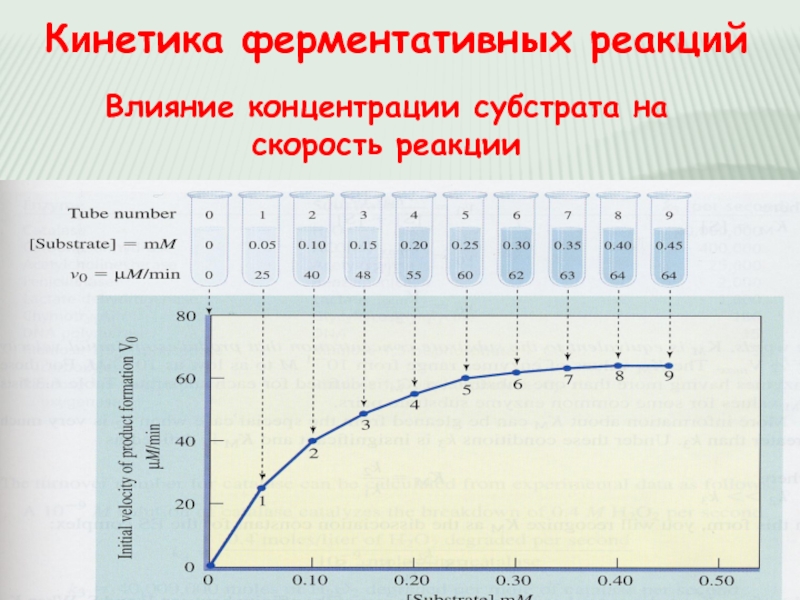
- 18. Кинетика ферментативных реакций Влияние концентрации субстрата на скорость реакции
- 19. УРАВНЕНИЕ МИХАЭЛИСА-МЕНТЕН В чем его смысл? —
- 20. Анализ уравнения Михаэлиса -Ментен 3. Km =
- 21. СМЫСЛ KM Km выводится из констант скоростей
- 22. Спасибо за внимание
Слайд 2ФЕРМЕНТЫ (ЭНЗИМЫ)
это высокоспецифичные белки, выполняющие функции биологических катализаторов.
Катализатор - это
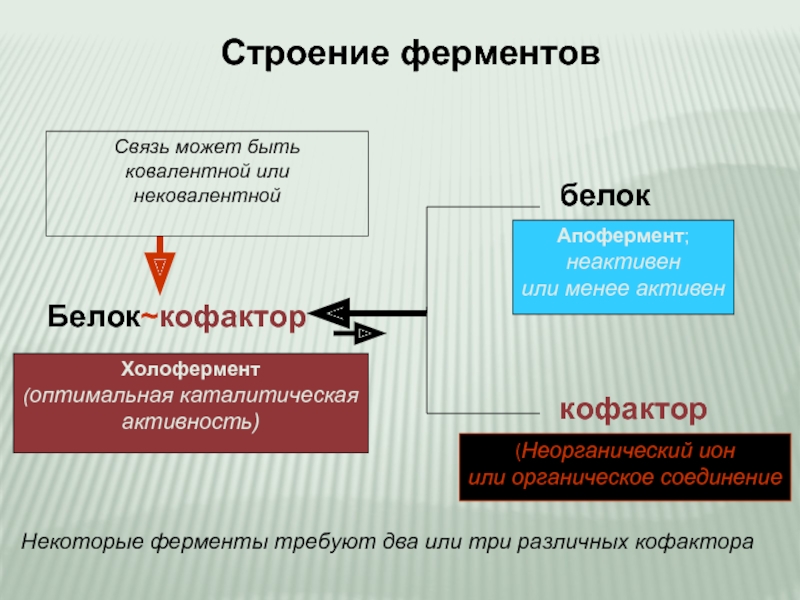
Слайд 4 Белок~кофактор
белок
кофактор
Связь может быть
ковалентной или
нековалентной
Холофермент
(оптимальная каталитическая
активность)
Апофермент;
неактивен
или менее активен
(Неорганический ион
или
Некоторые ферменты требуют два или три различных кофактора
Строение ферментов
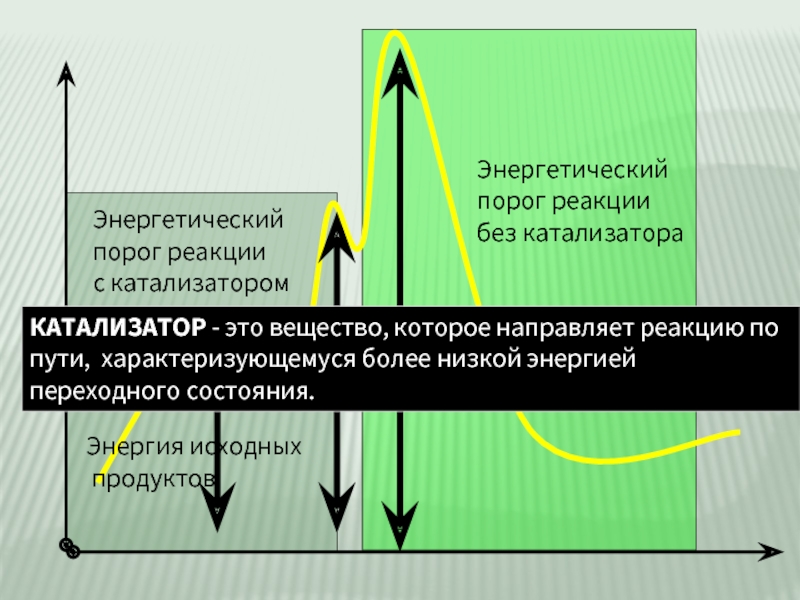
Слайд 5
Энергия исходных
продуктов
Энергетический
порог реакции
без катализатора
Энергетический
порог реакции
с катализатором
КАТАЛИЗАТОР
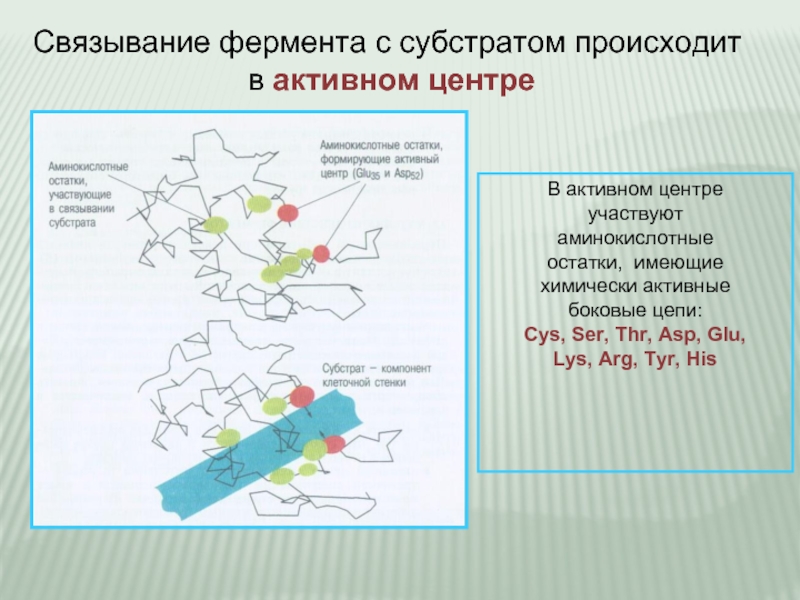
Слайд 6Связывание фермента с субстратом происходит
в активном центре
В активном центре
участвуют
аминокислотные
остатки, имеющие
химически активные
боковые цепи:
Cys, Ser, Thr, Asp, Glu,
Lys, Arg, Tyr, His
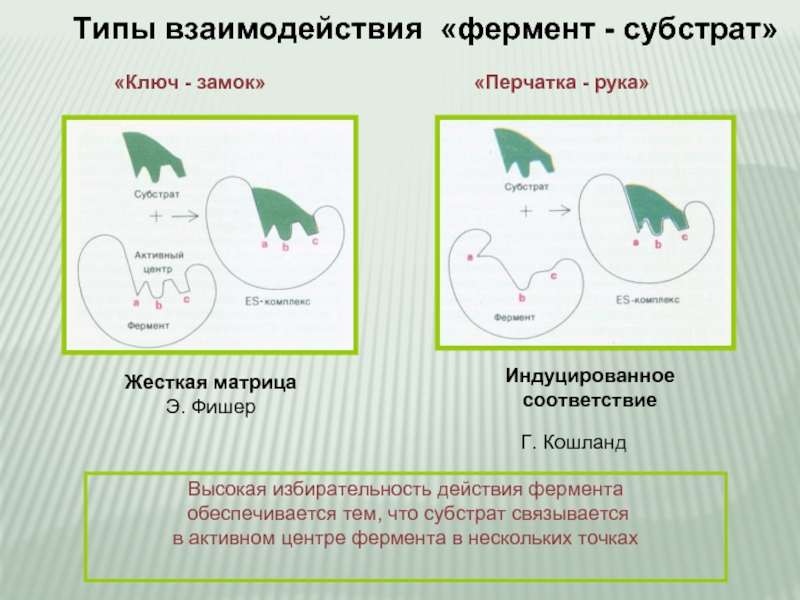
Слайд 7Высокая избирательность действия фермента
обеспечивается тем, что субстрат связывается
в активном
Типы взаимодействия «фермент - субстрат»
«Ключ - замок»
«Перчатка - рука»
Индуцированное
соответствие
Жесткая матрица
Э. Фишер
Г. Кошланд
Слайд 8Способы регуляции:
1. Аллостерическая регуляция
2. Ковалентная модификация
3. Диссоциация неактивного
предшественника (зимогена),
на активный
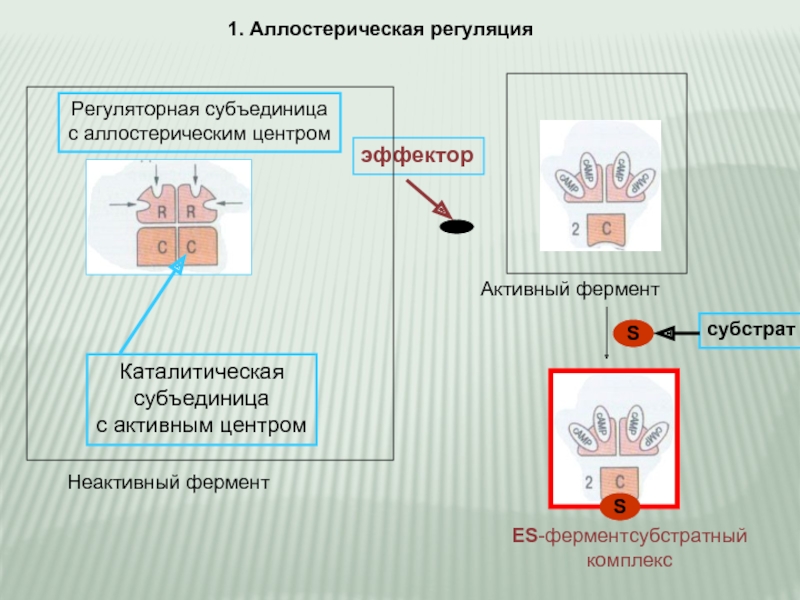
Слайд 91. Аллостерическая регуляция
эффектор
Каталитическая
субъединица
с активным центром
Неактивный фермент
Регуляторная субъединица
с аллостерическим центром
Активный фермент
S
субстрат
S
ES-ферментсубстратный
комплекс
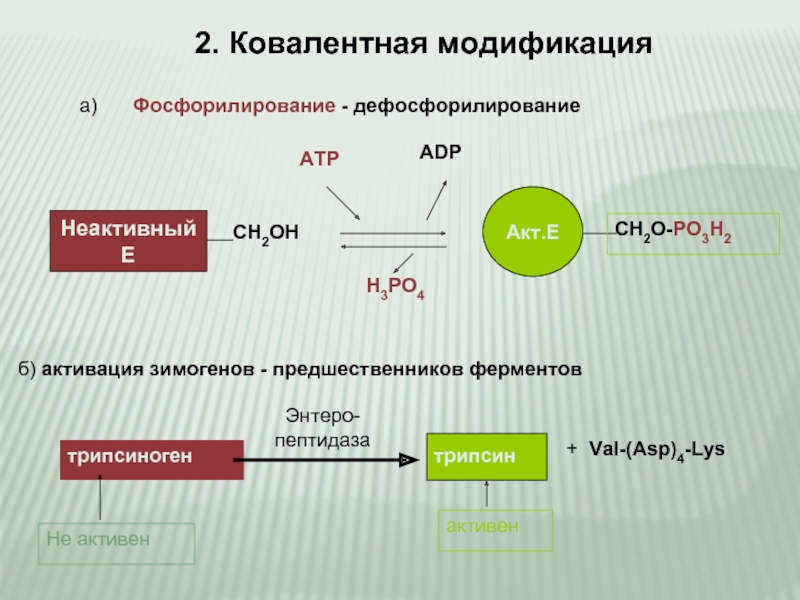
Слайд 102. Ковалентная модификация
Неактивный
Е
СН2ОН
Акт.Е
СН2О-РО3Н2
АТР
АDP
Н3РО4
Фосфорилирование - дефосфорилирование
a)
б) активация зимогенов - предшественников ферментов
трипсиноген
+
Энтеро-
пептидаза
Не активен
трипсин
активен
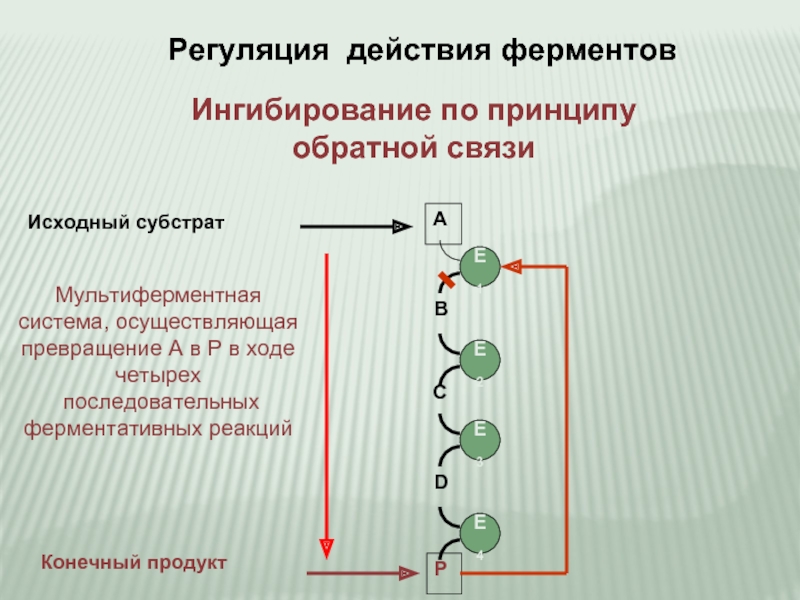
Слайд 11Регуляция действия ферментов
E4
E3
E2
E1
A
B
C
D
P
Ингибирование по принципу
обратной связи
Исходный субстрат
Конечный продукт
Мультиферментная
система, осуществляющая
превращение А в
четырех
последовательных
ферментативных реакций
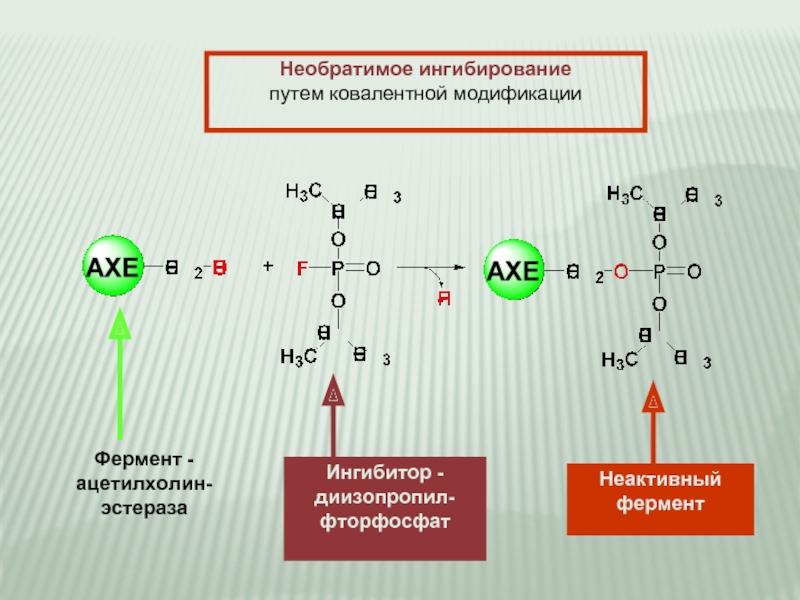
Слайд 13Необратимое ингибирование
путем ковалентной модификации
Фермент -
ацетилхолин-
эстераза
Ингибитор -
диизопропил-
фторфосфат
Неактивный
фермент
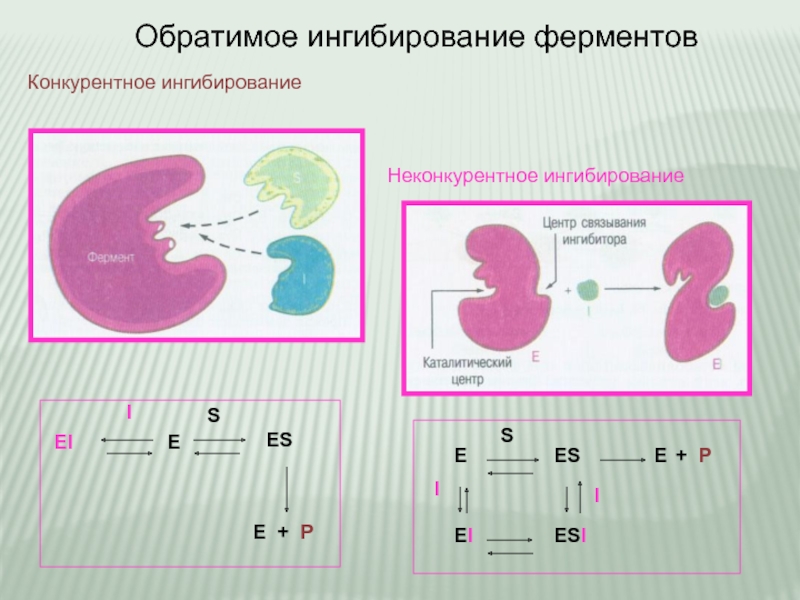
Слайд 14Обратимое ингибирование ферментов
Конкурентное ингибирование
Неконкурентное ингибирование
E
EI
ES
E + P
I
E
ES
E + P
ESI
EI
I
I
S
S
Слайд 15Иммобилизация фермента - закрепление
на полимерном носителе (полистироле)
Иммобилизованный фермент не смешивается
с
денатурации
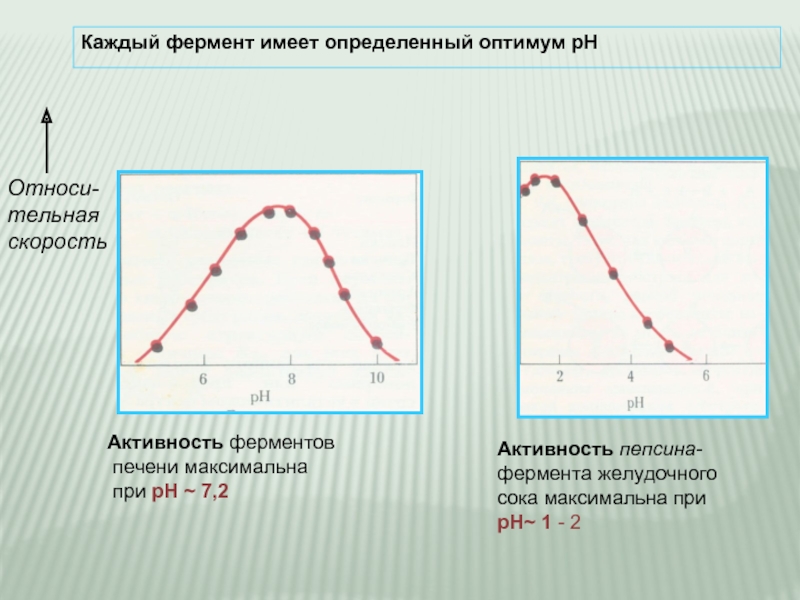
Слайд 16Каждый фермент имеет определенный оптимум рН
Относи-
тельная
скорость
Активность пепсина-
фермента желудочного
сока максимальна при
рН~ 1
Активность ферментов
печени максимальна
при рН ~ 7,2
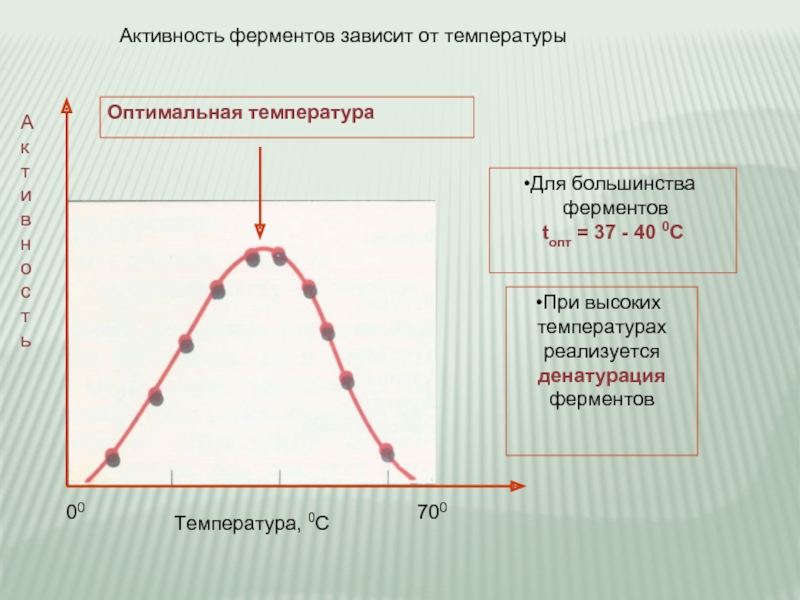
Слайд 17Оптимальная температура
00
700
Активность ферментов зависит от температуры
А
к
т
и
в
н
о
с
т
ь
Температура, 0С
Для большинства
ферментов
tопт = 37
При высоких
температурах
реализуется
денатурация
ферментов
Слайд 19УРАВНЕНИЕ МИХАЭЛИСА-МЕНТЕН
В чем его смысл? — Позволяет получить формальные характеристики скорости
Уравнение реакции превращения субстрата (S) в продукт (P), катализируемой ферментом (E);
Уравнение Михаэлиса-Ментен описывает зависимость скорости реакции от концентрации субстрата и, в частности, демонстриует явление насыщения. Условия, при которых работает уравнение Михаэлиса-Ментен:
Стационарная фаза реакции, т.е. [ES]=const, d[ES]/dt=0;
Измеряется начальная скорость; [S] ≈ [S0]
[E] = [E0] – [ES]
Слайд 20Анализ уравнения Михаэлиса -Ментен
3. Km = [S], тогда V0 = 1/2
Vmax [S]
Km + [S]
V0 =
1. [S] << Km, тогда V ~ K [S]
1
2
1
2. [S] >> Km, тогда V0 ~ Vmax
2
3
3
Слайд 21СМЫСЛ KM
Km выводится из констант скоростей
Km в условиях Михаэлиса-Ментен определяет скорость
при равновесии,
Константа диссоциации
Маленькая Km означает сильное связывание; высокая Km означает слабое связывание.
Km равна концентрации субстрата, при которой скорость реакции равна половине максимальной v=1/2vmax




![Анализ уравнения Михаэлиса -Ментен3. Km = [S], тогда V0 = 1/2 VmaxVmax [S]Km + [S]V0](/img/tmb/2/194827/a3fdd4eeae193ffa31581339f5b382f5-800x.jpg)