Лекции: ЭНЗИМОЛОГИЯ
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Ферменты: строение, свойства, регуляция активности презентация
Содержание
- 1. Ферменты: строение, свойства, регуляция активности
- 2. ЛЕКЦИЯ № 1 ФЕРМЕНТЫ: строение, свойства, регуляция активности
- 3. Актуальность темы Изучение ферментов способствует познанию
- 4. История энзимологии Пищеварение — это идущие внутри
- 5. Артур Корнберг (1918 – 2007) Кэри Мюллис
- 6. План лекции Понятие о ферментах и особенности
- 7. Цель Знать: строение, свойства и роль
- 8. Понятие о ферментах Ферменты – белковые
- 9. Особенности ферментативного катализа: сравнение с неорганическими катализаторами
- 10. Высокая эффективность ферментативного катализа 2Н2О2 → 2Н2О
- 11. Структура фермента: активный центр Активный центр
- 12. Схема строения активного центра Субстрат (S) –
- 13. Связывание субстрата в активном центре фермента
- 14. Механизм действия ферментов: этапы ферментативного катализа
- 15. Фермент-субстратный комплекс (ES) Образование ES – это
- 16. Пример индуцированного соответствия Каталаза – гемопротеин (сложный
- 17. Итак, высокая каталитическая эффективность ферментов обусловлена
- 18. Специфичность ферментов Каталитическая (реакционная) специфичность – способность
- 19. Специфичность ферментов Субстратная специфичность – способность фермента
- 20. Сложные ферменты Белок (апофермент) + кофактор (кофермент)
- 21. Кофакторы По химической природе: неорганические вещества (ионы
- 22. Кофакторы – ионы металлов: способы участия в
- 23. Cu, Zn-супероксиддисмутаза (СОД) Zn необходим для стабилизации
- 24. Коферменты, обратимо связанные с апоферментом NAD+ ,
- 25. Простетические группы флавиновые нуклеотиды FAD, FMN –
- 26. Мультиферментные комплексы Комплексы ферментов, катализирующие последовательные этапы
- 27. Кинетика ферментативного катализа: условия протекания ферментативных реакций
- 28. Факторы, определяющие активность фермента (скорость реакции) Количество
- 29. Скорость реакции и температура Влияние температуры обусловлено
- 30. Скорость реакции и рН Влияние рН обусловлено
- 31. Скорость реакции и концентрация субстрата Константа Михаэлиса
- 32. Скорость реакции и концентрация субстрата Зависимость скорости
- 33. Активаторы ферментов Активаторы – вещества, повышающие каталитическую
- 34. Ингибиторы ферментов Ингибиторы – вещества, снижающие каталитическую
- 35. Конкурентные ингибиторы Структурные аналоги субстратов (структурное сходство
- 36. Неконкурентное ингибирование Ингибитор связывается не с активным
- 37. Регуляция активности ферментов – основа регуляции метаболических
- 38. Изменение количества фермента Регуляция на уровне транскрипции:
- 39. Конститутивные ферменты – ферменты, которые синтезируются постоянно,
- 40. Механизмы регуляция каталитической активности ферментов Взаимодействие с
- 41. Взаимодействие с белком-активатором Фермент переваривания пищевого жира
- 42. Ассоциация-диссоциация протомеров
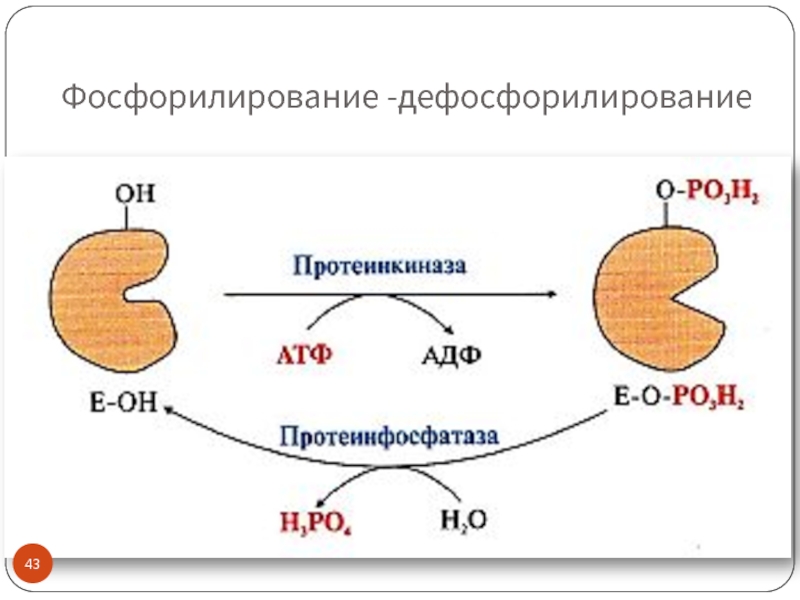
- 43. Фосфорилирование -дефосфорилирование
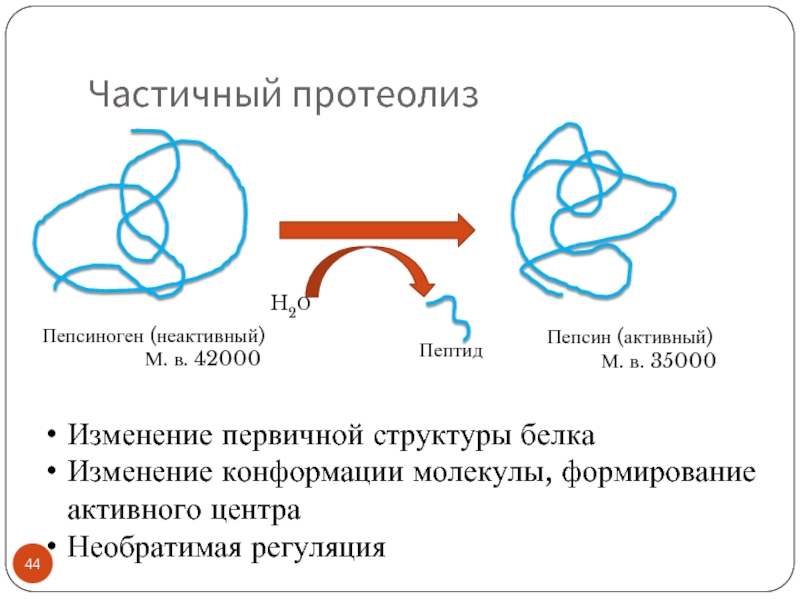
- 44. Частичный протеолиз Изменение первичной структуры белка Изменение конформации молекулы, формирование активного центра Необратимая регуляция
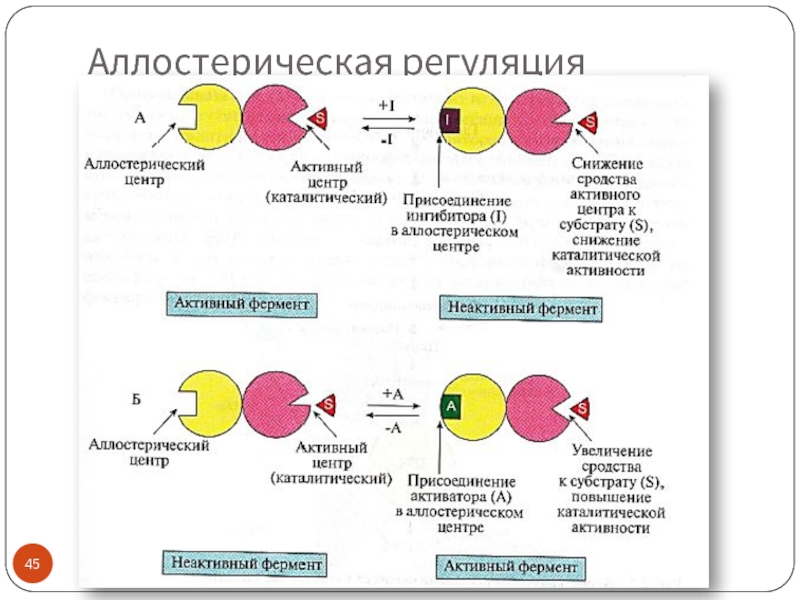
- 45. Аллостерическая регуляция
- 46. Аллостерические ферменты Олигомерные белки (2 и более
- 47. Задание для самостоятельной работы 1. Используя материал
- 48. Заключение Основа физиологических процессов – биохимические реакции
- 49. Литература Биохимия: учебник для вузов / ред.
Слайд 1
Дисциплина: биохимия (Б1.Б.15)
Специальность: педиатрия (31.05.02)
НГМУ, кафедра медицинской химии
Д.б.н., доцент Суменкова Дина
Слайд 3Актуальность темы
Изучение ферментов способствует познанию феномена жизни
Биохимические реакции – основа физиологических
Ферменты – «возбудители всех химических превращений у живых существ» (И.П. Павлов)
Изучение ферментов необходимо для понимания связи между ферментами и наследственными болезнями обмена веществ
Изучение ферментов позволяет расширять область их использования в медицине
Успехи биохимии, молекулярной биологии и медицины связаны с развитием энзимологии
Слайд 4История энзимологии
Пищеварение — это идущие внутри тела химические реакции, важнейшую роль
Ян Баптист Ван Гельмонт (17 в):
Лат. fermentum, греч. enzym
Слайд 5Артур Корнберг (1918 – 2007)
Кэри Мюллис (р. 1944)
Открытие ДНК-полимеразы (1956)
Открытие механизма
Создание высокоэффективного метода ПЦР-диагностики (1983)
Нобелевская премия совместно с Майклом Смитом (1993)
Слайд 6План лекции
Понятие о ферментах и особенности ферментативного катализа (свойства ферментов)
Структура
Сложные ферменты и их кофакторы Мультиферментные комплексы
Кинетика ферментативных реакций
Регуляция активности ферментов
Слайд 7Цель
Знать:
строение, свойства и роль ферментов в организме человека
химико-биологическую сущность ферментативного
механизмы регуляции активности ферментов для понимания биохимических основ функционирования организма
Знания о ферментативном катализе необходимы для понимания принципов методов определения активности ферментов в клинической лабораторной диагностике с целью выявления патологических процессов в органах и системах детей и подростков
Слайд 8Понятие о ферментах
Ферменты – белковые катализаторы химических реакций в живом
состоят из L-α-аминокислот, соединенных пептидными связями
имеют 4 уровня организации молекул
характерна конформационная лабильность
при денатурации теряют активность
синтезируются как белковые молекулы
И.П. Павлов: переваривающая способность желудочного сока зависит от количества белка в нем (отсюда следует, что пепсин – белок)
Слайд 9Особенности ферментативного катализа: сравнение с неорганическими катализаторами
Сходства
Различия
(свойства ферментов)
Катализируют реакции возможные по
Снижают энергию активации реакции
Не изменяют термодинамических характеристик реакции (не смещают равновесие)
Многие ферменты катализируют прямую и обратную реакции
Не расходуются в процессе реакции
Уникальность структуры
Высокая эффективность катализа
Высокая специфичность действия
Конформационная лабильность
Регулируемая активность
Проявляют активность в оптимальных для организма условиях
Слайд 10Высокая эффективность ферментативного катализа
2Н2О2 → 2Н2О + О2
самопроизвольно (Еа = 70
при участии железа (Еа = 42 кДж/моль), скорость реакции увеличивается в 103 раз
в присутствии каталазы (Еа = 7 кДж/моль), скорость реакции увеличивается в 1010 раз
Что лежит в основе высокой эффективности ферментативного катализа?
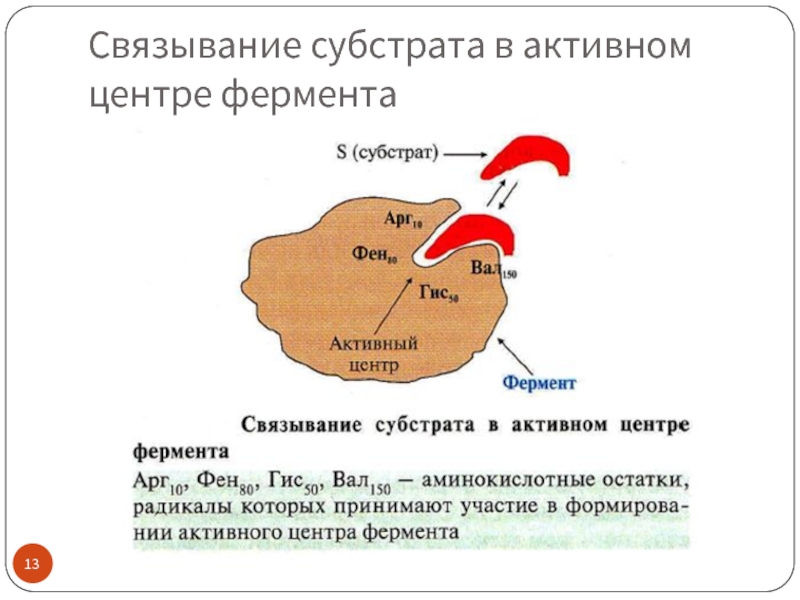
Слайд 11Структура фермента: активный центр
Активный центр фермента (АЦ) – это участок
Формируется на уровне III структуры белка
У простых ферментов состоит только из аминокислотных остатков
У сложных ферментов имеет кофактор (кофермент)
Участок связывания активного центра обеспечивает сродство к субстрату и формирование фермент-субстратного комплекса (ES), например, за счет ионных взаимодействий
Каталитический участок активного центра осуществляет химическую реакцию
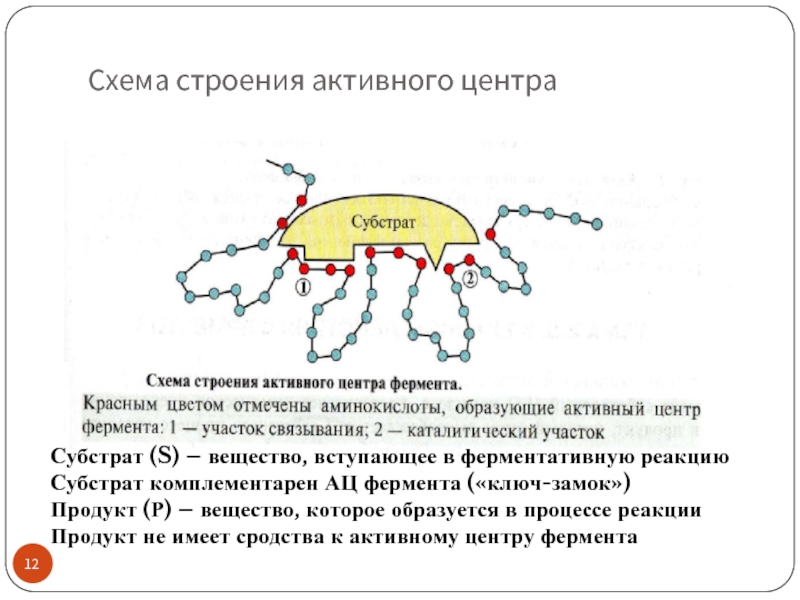
Слайд 12Схема строения активного центра
Субстрат (S) – вещество, вступающее в ферментативную реакцию
Субстрат
Продукт (Р) – вещество, которое образуется в процессе реакции
Продукт не имеет сродства к активному центру фермента
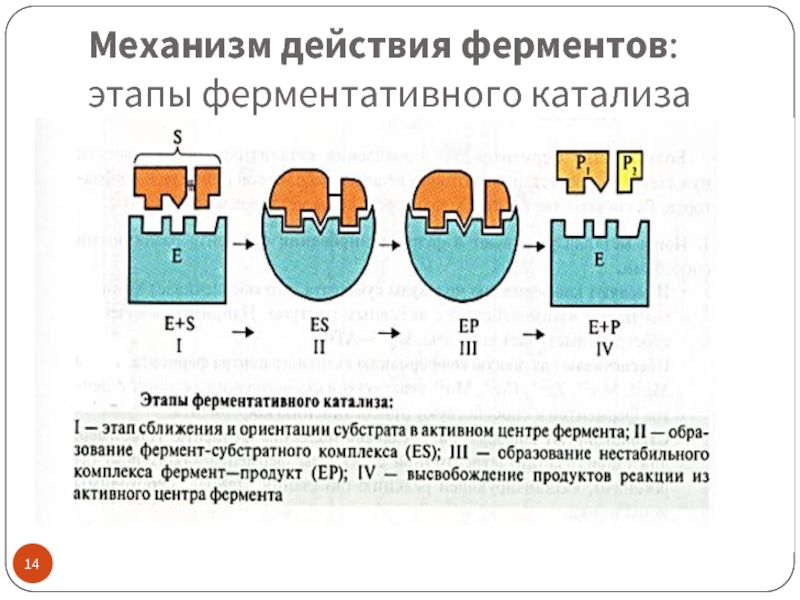
Слайд 15Фермент-субстратный комплекс (ES)
Образование ES – это ключевой момент ферментативной реакции, основа
ES образуется в результате индуцированного соответствия фермента и субстрата
(теория Д. Кошленда, 1958) :
субстрат индуцирует конформационные изменения фермента и его активный центр принимает необходимую для связывания с субстратом пространственную ориентацию
(фермент активен только в присутствии субстрата)
субстрат также претерпевает конформационные перестройки
Слайд 16Пример индуцированного соответствия
Каталаза – гемопротеин
(сложный фермент: белковая часть + гем)
неактивная каталаза:
активная каталаза: при взаимодействии с Н2О2 железо перемещается в плоскость кольца, «настраивая» активный центр фермента
Слайд 17Итак, высокая каталитическая эффективность ферментов обусловлена
Высокой специфичностью связывания АЦ фермента и
Конформационной лабильностью ферментов, которая является основой их высокой специфичности
Слайд 18Специфичность ферментов
Каталитическая (реакционная) специфичность – способность фермента катализировать одну химическую реакцию
Пример: реакции гидролиза, окисления-восстановления
Исключение: лиазы, в одном направлении, катализируют негидролитическое расщепление субстрата, а в другом – присоединение простой молекулы по кратной связи
Слайд 19Специфичность ферментов
Субстратная специфичность – способность фермента взаимодействовать с одним (абсолютная) или
абсолютная субстратная специфичность
уреаза: гидролиз мочевины
аргиназа: гидролиз аргинина
относительная субстратная специфичность
пищеварительные ферменты
стереоспецифичность
лактатдегидрогеназа: окисление только L-лактата
Слайд 20Сложные ферменты
Белок (апофермент) + кофактор (кофермент) → активный фермент (холофермент)
апофермент –
большинство природных ферментов – сложные белки-протеиды
кофактор – небелковая часть сложного фермента (лат. «вместе делающий»)
Слайд 21Кофакторы
По химической природе:
неорганические вещества (ионы металлов)
органические вещества (производные витаминов) - коферменты
По
слабые взаимодействия (присутствуют в активом центре фермента только в момент реакции, являясь косубстратом)
ковалентная связь (простетическая группа)
Роль кофактора:
изменение конформации фермента, субстрата
непосредственное участие в реакции
Слайд 22Кофакторы – ионы металлов: способы участия в ферментативном катализе
Изменяют конформацию субстрата
Стабилизируют конформацию апофермента (Zn2+ стабилизирует IV структуру алкогольдегидрогеназы)
Участвует в катализе (ионы железа, меди участвуют в переносе электронов)
Слайд 23Cu, Zn-супероксиддисмутаза (СОД)
Zn необходим для стабилизации молекулы
Cu – активный участник в
О2 - + О2 - + 2Н+ = Н2О2 + О2
1) О2 - + Cu2+ + Н+ = Cu1+ + О2
2) О2 - + Cu1+ + Н+ = Cu2+ + Н2О2
Слайд 24Коферменты, обратимо связанные с апоферментом
NAD+ , NADP+ – кофермент оксидоредуктаз (анаэробных
HS-CoA (кофермент А) - кофермент ацетил-, ацилтрансфераз, некоторых лигаз, источник синтеза – пантотеновая кислота (vit B5)
тетрагидрофолат (Н4 –фолат) - кофермент трансфераз - переносчиков С1-фрагментов, источник синтеза – фолиевая кислота (vit B9)
Слайд 25Простетические группы
флавиновые нуклеотиды FAD, FMN – коферменты оксидоредуктаз (аэробных и некоторых
пиридоксальфосфат - кофермент аминотрансфераз и некоторых других ферментов, источник синтеза - пиридоксин (vit В6)
тиаминпирофосфат - кофермент в реакциях окислительного декарбоксилирования кетокислот и кетосахаров, источник синтеза – тиамин (vit В1)
биоцитин - кофермент лигаз, образующих связи С – С и карбоксильные группы, источник синтеза - биотин (vit Н, или В7)
Слайд 26Мультиферментные комплексы
Комплексы ферментов, катализирующие последовательные этапы превращения какого-либо субстрата
Отличительные особенности комплексов:
прочность
молекулярные массы от 2,3•106 до 10•106
определенный порядок расположения ферментов в соответствии с последовательностью прохождения этапов превращения исходного субстрата
Биологическая значимость комплексов: повышение эффективности процесса превращения
сокращение расстояния, на которые молекулы промежуточных продуктов должны перемещаться при действии изолированных ферментов
Примеры комплексов:
митохондриальная пируватдегидрогеназа и α-кетоглутаратдегидрогеназа
цитоплазматическая синтаза высших жирных кислот
ферментные комплексы дыхательной цепи митохондрий
Слайд 27Кинетика ферментативного катализа:
условия протекания ферментативных реакций
Активность фермента, или скорость ферментативной реакции
активность фермента (1МЕ) = мкмоль (S или P) / мин
1 кат = 6 х 107 МЕ
уд. активность фермента = мкмоль (S или P) / (мин • мг белка)
Слайд 28Факторы, определяющие активность фермента (скорость реакции)
Количество фермента
Количество субстрата
Количество продукта (для аллостерических
Концентрация кофактора (для сложных ферментов)
Присутствие активаторов или ингибиторов
Температура
рН среды
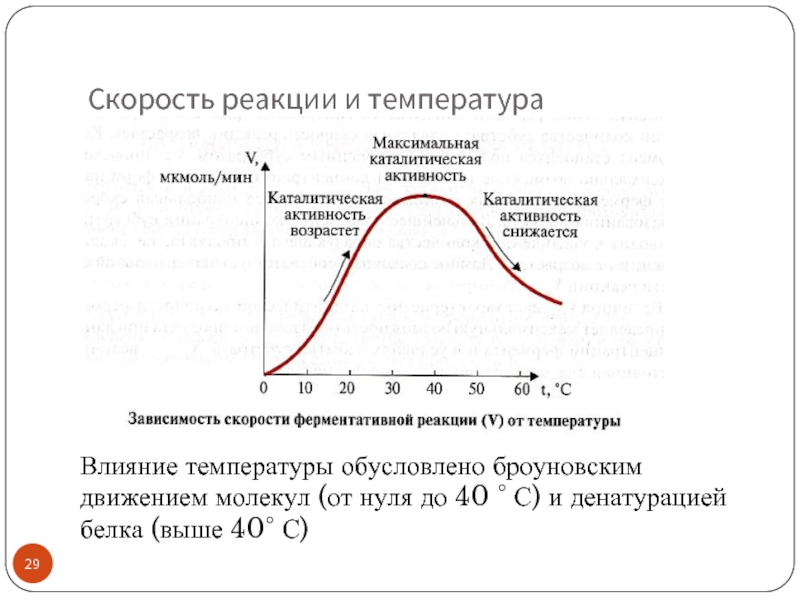
Слайд 29Скорость реакции и температура
Влияние температуры обусловлено броуновским движением молекул (от нуля
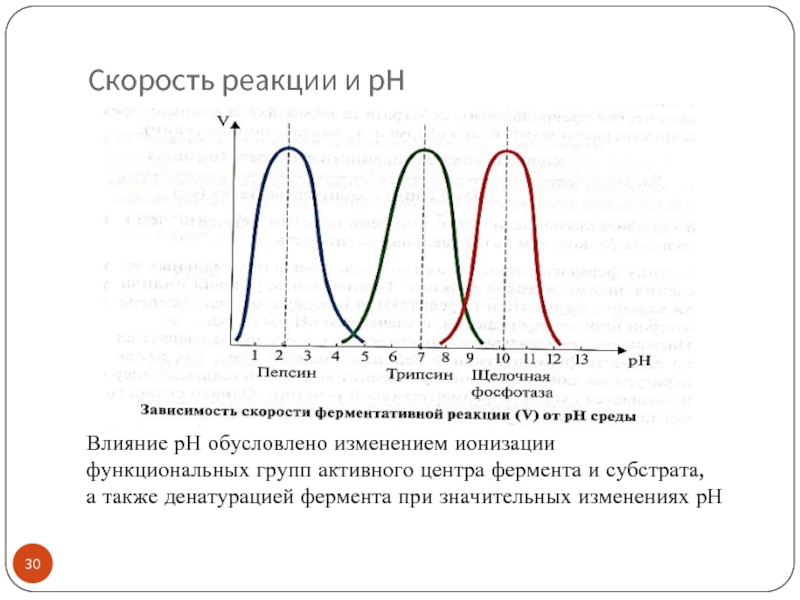
Слайд 30Скорость реакции и рН
Влияние рН обусловлено изменением ионизации
функциональных групп активного центра
а также денатурацией фермента при значительных изменениях рН
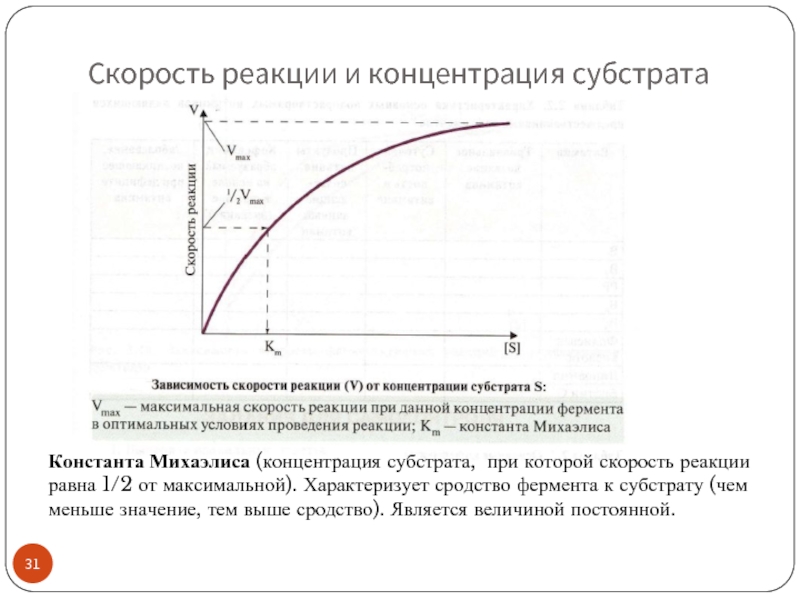
Слайд 31Скорость реакции и концентрация субстрата
Константа Михаэлиса (концентрация субстрата, при которой скорость
Слайд 32Скорость реакции и концентрация субстрата
Зависимость скорости реакции от концентрации субстрата описывает
V = V max · [ S] / [ S] + Km
Отсюда,
[ S] = Km · V / V max - V
Слайд 33Активаторы ферментов
Активаторы – вещества, повышающие каталитическую активность ферментов
Часто активаторами являются микро-,
Активаторы не являются кофакторами
Известно, что в присутствии хлорид-ионов активность амилазы слюны значительно возрастает, а в отсутствии катионов кальция не проявляется. Какую роль в проявлении активности фермента играют кальций и хлор?
Слайд 34Ингибиторы ферментов
Ингибиторы – вещества, снижающие каталитическую активность фермента
По типу химической связи:
обратимые
необратимые (ковалентная связь)
По механизму действия:
конкурентные
неконкурентные
Слайд 35Конкурентные ингибиторы
Структурные аналоги субстратов (структурное сходство той части молекулы, которая взаимодействует
Связываются в активном центре фермента
Формируется комплекс EI
Не изменяют структуры фермента
Продукт реакции не образуется (часть молекулы ингибитора, которая попадает в каталитический участок, не имеет структурного сходства с соответствующей частью молекулы субстрата)
Ингибитор вытесняется из активного центра фермента при увеличении концентрации субстрата
Снижают скорость реакции, но не изменяют Vmax. Почему?
«Изменяют» (повышают) Кm. В чем состоит условность «изменения» Кm?
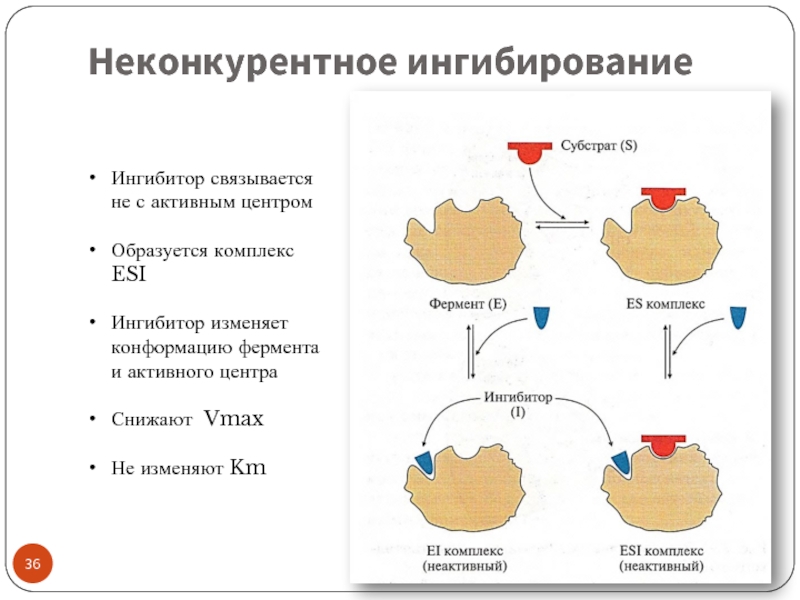
Слайд 36Неконкурентное ингибирование
Ингибитор связывается не с активным центром
Образуется комплекс ESI
Ингибитор изменяет конформацию
Снижают Vmax
Не изменяют Km
Слайд 37Регуляция активности ферментов – основа регуляции метаболических путей
Способы регуляции активности ферментов:
Изменение
Изменение каталитической активности фермента вследствие изменения его конформации
Ферменты, активность которых регулируется при участии гормонов или каких-либо метаболитов, называются регуляторными, или ключевыми. С помощью ключевых ферментов регулируется скорость метаболических процессов.
Слайд 38Изменение количества фермента
Регуляция на уровне транскрипции: индукция синтеза
Инсулин индуцирует синтез ключевых
Активация гликолиза в клетках приводит к снижению уровня глюкозы в крови.
Слайд 39Конститутивные ферменты – ферменты, которые синтезируются постоянно, независимо от наличия субстрата
Индуцибельные
ПРИМЕР: алкогольдегидрогеназа
Слайд 40Механизмы регуляция каталитической активности ферментов
Взаимодействие с белком-активатором
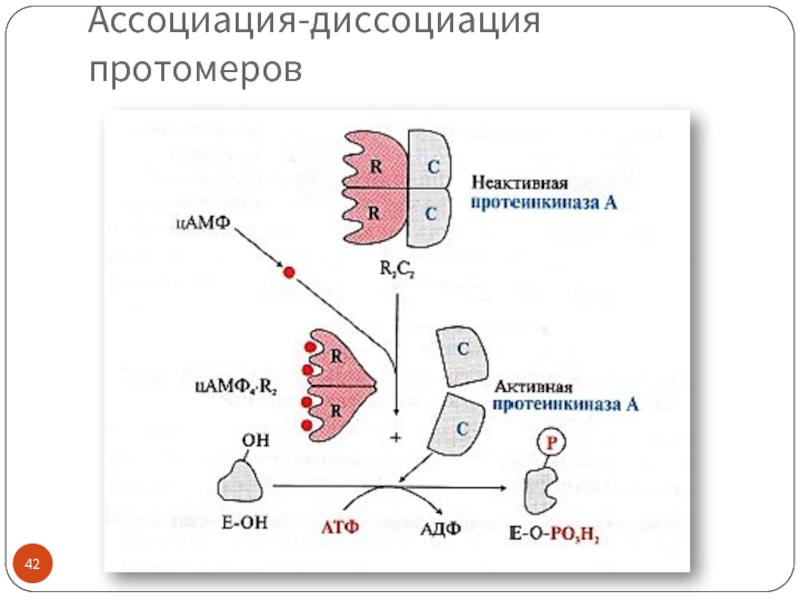
Ассоциация и диссоциация протомеров
Фосфорилирование и
Частичный протеолиз
Аллостерическая регуляция
Слайд 41Взаимодействие с белком-активатором
Фермент переваривания пищевого жира в тонком кишечнике – панкреатическая
Мембранный фермент аденилатциклаза, участвующий в передаче сигнала гормонов в клетку, активируется путем взаимодействия с альфа-субъединицей G-белка
Слайд 44Частичный протеолиз
Изменение первичной структуры белка
Изменение конформации молекулы, формирование активного центра
Необратимая регуляция
Слайд 46Аллостерические ферменты
Олигомерные белки (2 и более субъединиц)
Имеют аллостерический центр (один или
Активный и аллостерический центры находятся в разных протомерах
Регуляторы активности - эффекторы (активаторы, ингибиторы)
Изменение конформации регуляторного протомера приводит к изменению конформации молекулы в целом, а значит и активного центра
Катализируют ключевые реакции
Аллостерическая регуляция обратима
ПРИМЕРЫ эффекторов:
продукты реакции (ингибиторы)
ATP – ингибитор, ADP – активатор ключевых ферментов энергетического обмена
Слайд 47Задание для самостоятельной работы
1. Используя материал слайдов 24, 25 закончите таблицу:
2. Используя интернет-ресурсы, найдите информацию о лекарственных препаратах, механизм действия которых связан с ингибированием активности ферментов. Приведите примеры лекарственных препаратов и назовите область их применения.
Слайд 48Заключение
Основа физиологических процессов – биохимические реакции
Скорость биохимических реакций в организме катализируют
Ферментам свойственна высокая каталитическая эффективность, специфичность действия, конформационная лабильность, способность осуществлять катализ в «мягких» условиях внутренней среды организма
Активность ферментов регулируется. Это свойство ферментов является основой регуляции метаболических процессов в организме
Слайд 49Литература
Биохимия: учебник для вузов / ред. Е. С. Северин. - М.:
Биологическая химия с упражнениями и задачами: учебник / ред. С.Е. Северин. – М.: ГЭОТАР-Медиа, 2013. - 624 с. (С. 65-72; 76-86)
Биологическая химия: учебник для студентов медицинских вузов / А.Я. Николаев. – М.: Мед. информ. агенство, 2007. – 568 с.