- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Ферменты. (лекция 2) презентация
Содержание
- 1. Ферменты. (лекция 2)
- 2. Классификация ферментов
- 3. II. Трансферазы. а) п/кл фосфотрансферазы. Все трансферазы
- 4. III. Гидролазы. Ферменты, катализирующие расщепление веществ с
- 5. Механизм действия ферментов Биологический ферментативный катализ является
- 6. Основы катализа А. Энергетический профиль в отсутствии катализатора Б. Энергетический профиль в присутствии катализатора
- 7. Снижение энергии активации достигается за счет: 1.
- 8. 3. теория индуцированного соответствия. Предложил Кошланд. После
- 9. График зависимости скорости ферментативной реакции от температуры Температура Активность ферментов
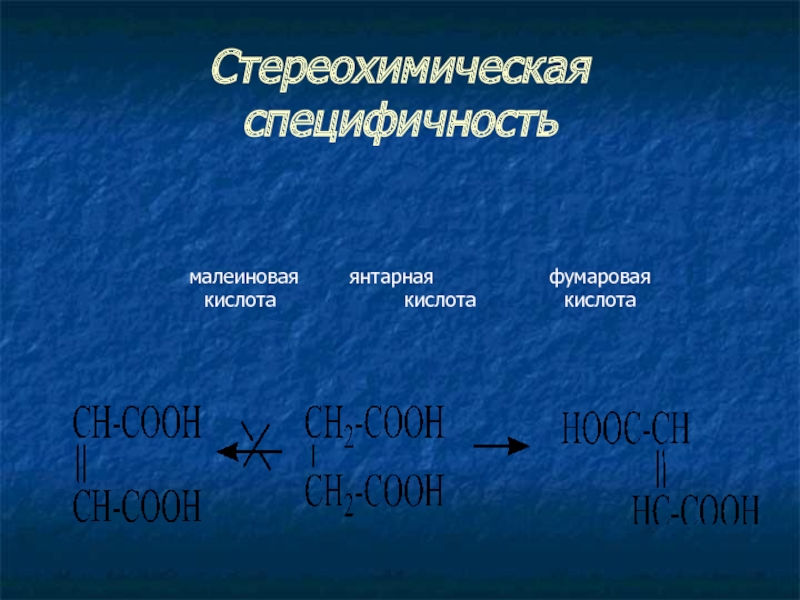
- 11. Стереохимическая специфичность малеиновая янтарная фумаровая кислота кислота кислота
- 12. Реакционная специфичность
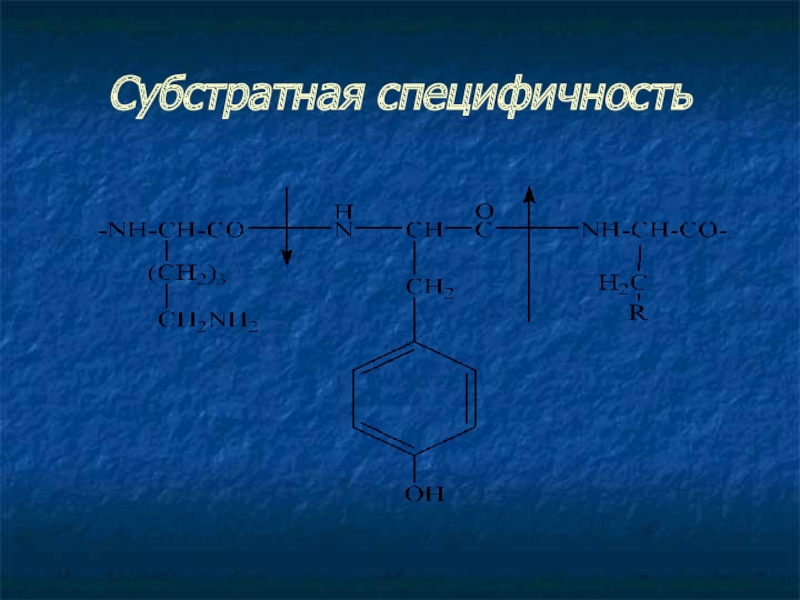
- 13. Субстратная специфичность
- 14. Факторы, влияющие на активность фермента Концентрация субстрата.
- 15. Стадии ферментативного процесса Е +
- 16. Km - константа Михаэлиса. Лимитирующим фактором протекания
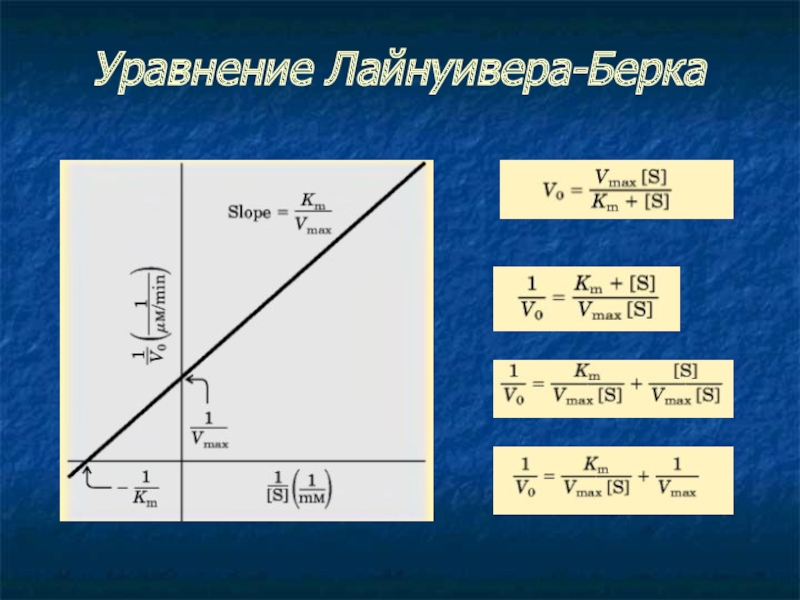
- 17. Уравнение Лайнуивера-Берка
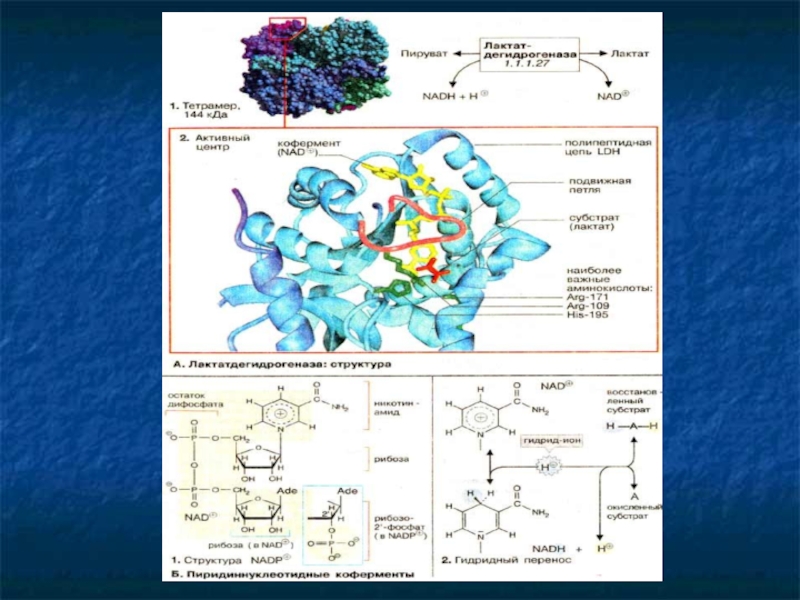
- 18. Структура фермента со связанным в активном центре субстратом
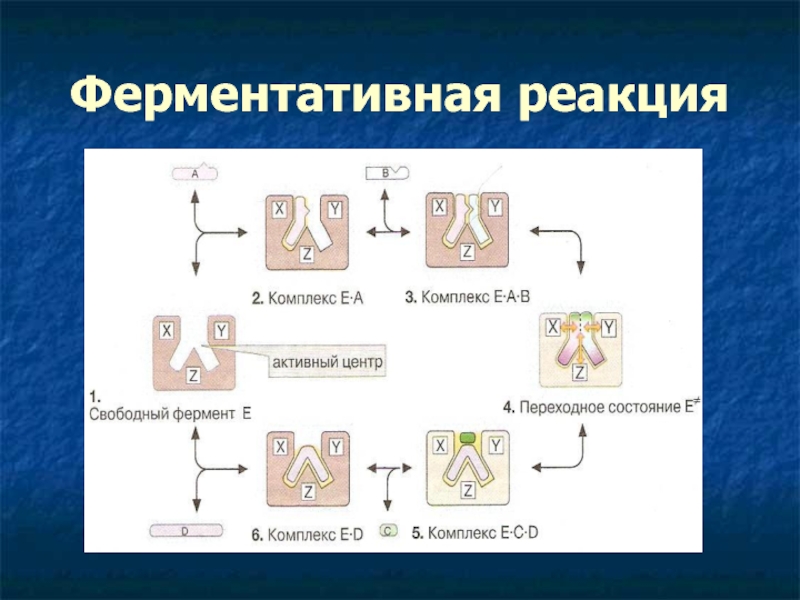
- 19. Ферментативная реакция
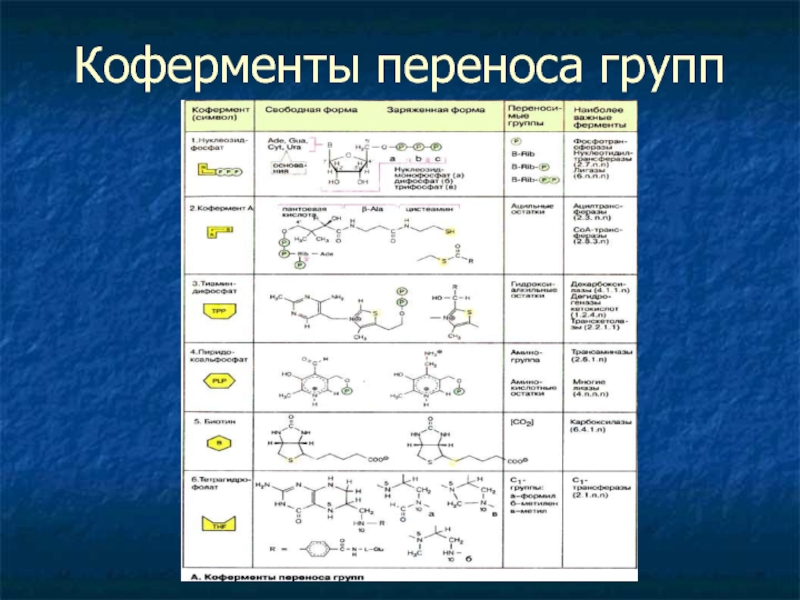
- 20. Коферменты переноса групп
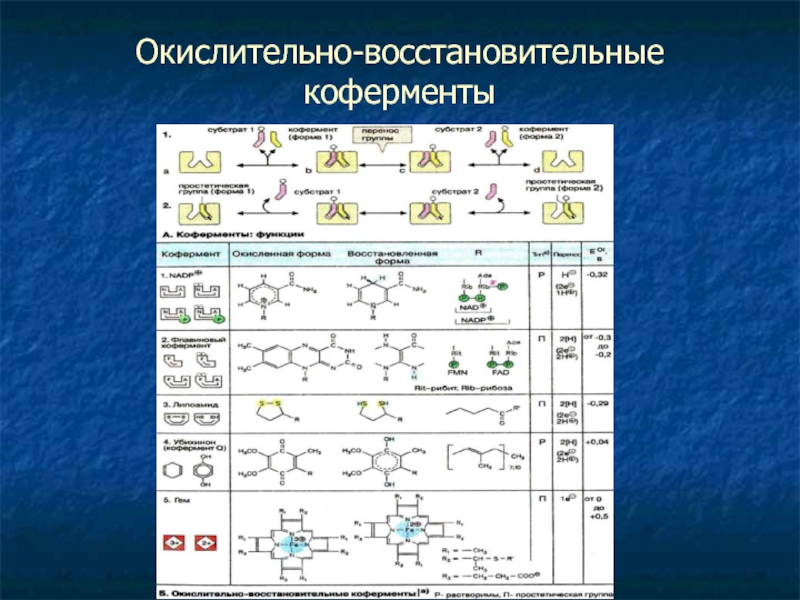
- 21. Окислительно-восстановительные коферменты
- 24. IV. Влияние ингибиторов и активаторов. Модулятор −
- 25. Конкурентное ингибирование Ингибитор по своему строению
- 26. Неконкурентное ингибирование Ингибитор связывается с ферментом
- 27. Сравнение кинетических характеристик при различных типах ингибирования
- 28. бесконкурентное ингибирование При это меняются максимальная
- 29. Аллостерические ферменты. не подчиняются уравнению Михаэлиса-Ментен.
- 30. При связывании модулятора с аллостерическим центром,
- 31. Аллостерические модуляторы бывают положительные и отрицательные.
- 32. Ковалентная модификация. Ферменты, регулируемые с помощью
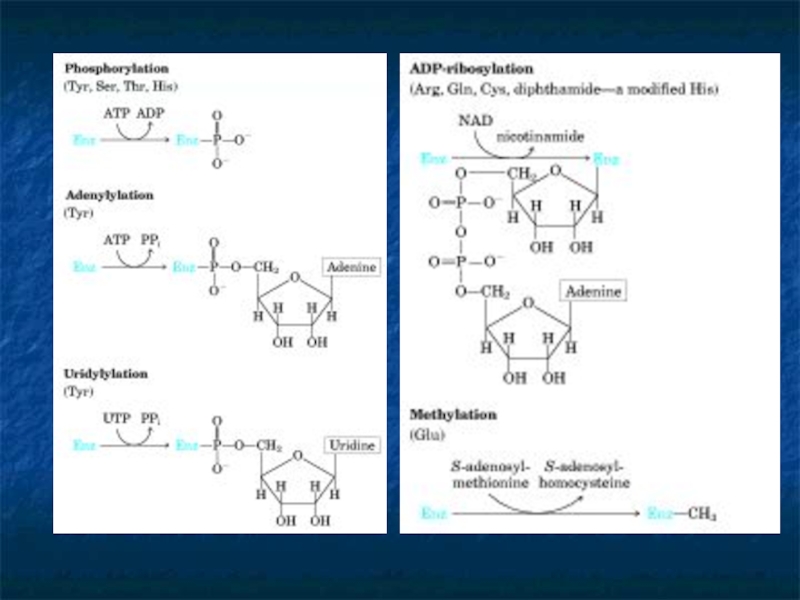
Слайд 3II. Трансферазы.
а) п/кл фосфотрансферазы.
Все трансферазы переносят функционольные группы. Фосфотрансферазы катализируют перенос
фосфатной группы. Коферментом является АТФ. В этой молекуле остатки фосфорной кислоты связаны между собой макроэргической связью. Кроме АТФ могут учавствовать молекулы ЦТФ, ГТФ, УТФ.
б) п/кл аминотрансферазы.
Ферменты отвечают за перенос аминогрупп.
Коферментом является передоксильфосфат, является производным пиридоксина − витамина В6.
в) п/кл ацилтрансферазы.
Переносят остатки органических кислот. Коферментом является кофермент А, производное пантотеновой кислоты.
г) п/кл переносящие одноуглеродные группы(СН, СН3).
Коферментом является тетрагидрофолиевая кислота, производная витамина − фолиевая кислота.
б) п/кл аминотрансферазы.
Ферменты отвечают за перенос аминогрупп.
Коферментом является передоксильфосфат, является производным пиридоксина − витамина В6.
в) п/кл ацилтрансферазы.
Переносят остатки органических кислот. Коферментом является кофермент А, производное пантотеновой кислоты.
г) п/кл переносящие одноуглеродные группы(СН, СН3).
Коферментом является тетрагидрофолиевая кислота, производная витамина − фолиевая кислота.
Слайд 4III. Гидролазы.
Ферменты, катализирующие расщепление веществ с участием воды. Они не нуждаются
в коферментах.
IV. Лиазы.
Ферменты, катализирующие присоединение веществ по двойным связям.
V. Изомеразы.
Катализируют внутримолекулярные перегруппировки. Имеют окончание –изомераза или –мутаза. Могут осуществлять рацимизацию, транс-,цисизомеризацию, внутримолекулярный перенос функциональных групп. Коферментом является цианкобаламин − производное витамина В12.
VI. Лигазы = синтетазы.
Ферменты, осуществляющие энергозависимый синтез. Поставщиком обычно является внутриклеточный пирофосфат(АТФ, АДФ).
IV. Лиазы.
Ферменты, катализирующие присоединение веществ по двойным связям.
V. Изомеразы.
Катализируют внутримолекулярные перегруппировки. Имеют окончание –изомераза или –мутаза. Могут осуществлять рацимизацию, транс-,цисизомеризацию, внутримолекулярный перенос функциональных групп. Коферментом является цианкобаламин − производное витамина В12.
VI. Лигазы = синтетазы.
Ферменты, осуществляющие энергозависимый синтез. Поставщиком обычно является внутриклеточный пирофосфат(АТФ, АДФ).
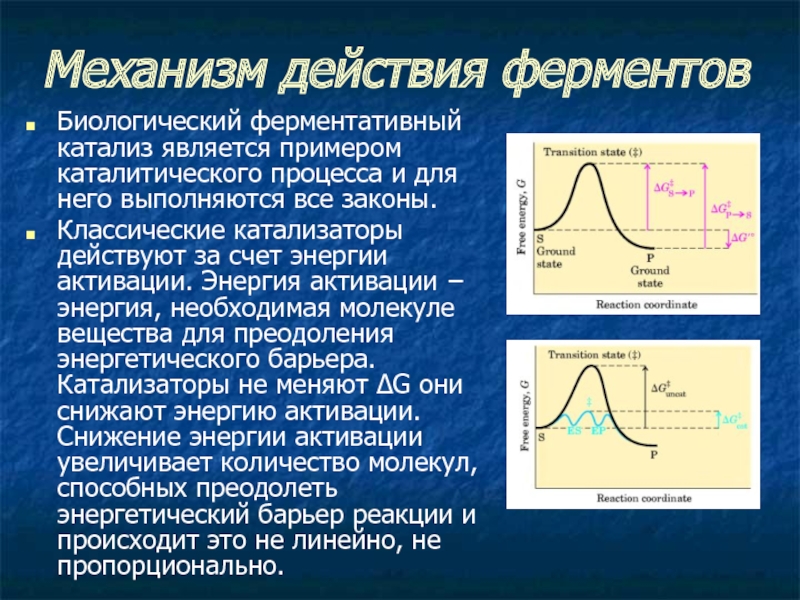
Слайд 5Механизм действия ферментов
Биологический ферментативный катализ является примером каталитического процесса и для
него выполняются все законы.
Классические катализаторы действуют за счет энергии активации. Энергия активации − энергия, необходимая молекуле вещества для преодоления энергетического барьера. Катализаторы не меняют ΔG они снижают энергию активации. Снижение энергии активации увеличивает количество молекул, способных преодолеть энергетический барьер реакции и происходит это не линейно, не пропорционально.
Классические катализаторы действуют за счет энергии активации. Энергия активации − энергия, необходимая молекуле вещества для преодоления энергетического барьера. Катализаторы не меняют ΔG они снижают энергию активации. Снижение энергии активации увеличивает количество молекул, способных преодолеть энергетический барьер реакции и происходит это не линейно, не пропорционально.
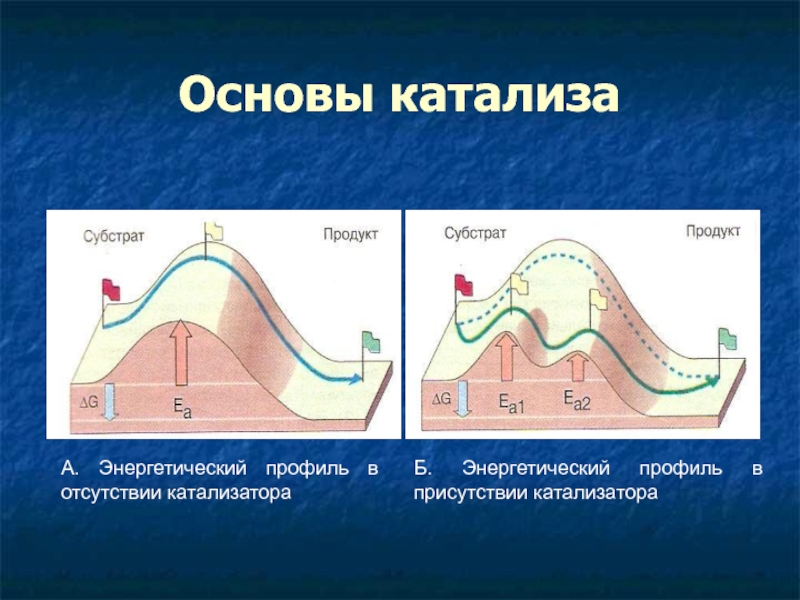
Слайд 6Основы катализа
А. Энергетический профиль в отсутствии катализатора
Б. Энергетический профиль в
присутствии катализатора
Слайд 7Снижение энергии активации достигается за счет:
1. ориентации субстратов.
2. Теория стерического взаимодействия
(взаимодействие ключ-замок). Фишер предположил, что активный центр фермента пространственно соответствует молекуле субстрата. За счет своей пространственной специфичности фермент и субстрат ориентируются специфично.
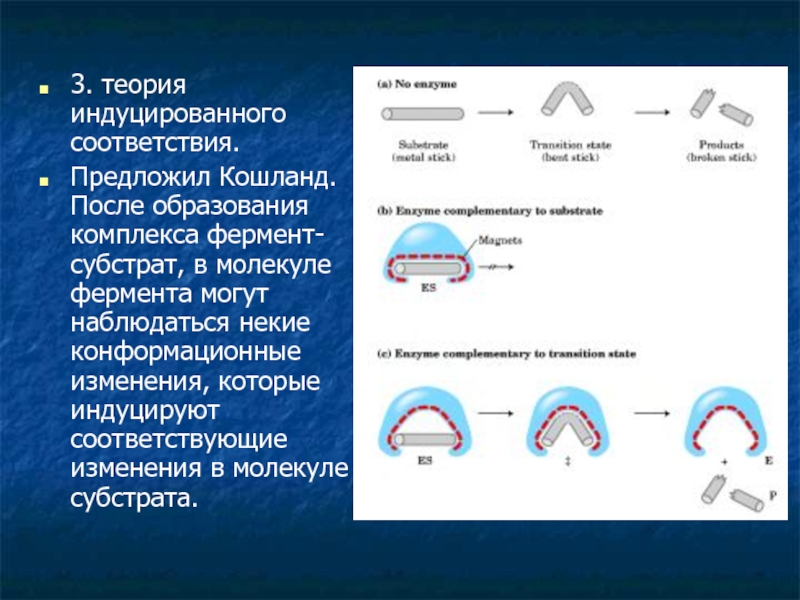
Слайд 83. теория индуцированного соответствия.
Предложил Кошланд. После образования комплекса фермент-субстрат, в молекуле
фермента могут наблюдаться некие конформационные изменения, которые индуцируют соответствующие изменения в молекуле субстрата.
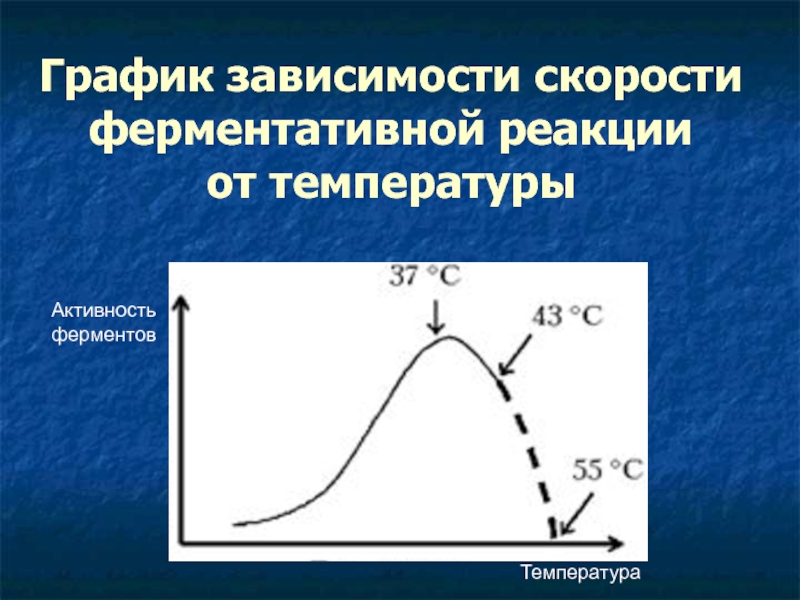
Слайд 9График зависимости скорости ферментативной реакции
от температуры
Температура
Активность ферментов
Слайд 14Факторы, влияющие на активность фермента
Концентрация субстрата.
В 1913г. Михаэлис и Ментен проедложили
уравнение
υ = υmax[S]/Km+[S]
υ = υmax[S]/Km+[S]
Слайд 15
Стадии ферментативного процесса
Е + S ES Е + P
Е - фермент
S
- субстрат
ЕS - фермент-субстратный комплекс
Р - продукт
k1
k2
k3
При условии, что: 1. [Еo] 〉〉 [S]
2. [ES]=const
Зависимость скорости реакции описывается
уравнением Михаэлиса-Ментен
ЕS - фермент-субстратный комплекс
Р - продукт
k1
k2
k3
При условии, что: 1. [Еo] 〉〉 [S]
2. [ES]=const
Зависимость скорости реакции описывается
уравнением Михаэлиса-Ментен
Слайд 16Km - константа Михаэлиса.
Лимитирующим фактором протекания реакции, является образование фермент-субстратного комплекса.
Km=
концентрации субстрата при которой скорость реакции равна ½ скорости максимальной.
Т.к. это концентрация, то она выражается моль/литр и тп.
Уравнение Михаэлиса-Ментен описывает односубстратные не аллостерические ферменты.
Т.к. это концентрация, то она выражается моль/литр и тп.
Уравнение Михаэлиса-Ментен описывает односубстратные не аллостерические ферменты.
Слайд 24IV. Влияние ингибиторов и активаторов.
Модулятор − вещество, способное изменять активность ферментов.
Активатор
− вещество, ускоряющее протекание ферментативных реакций. Механизм действия сходен с механизмом действия ингибиторов.
Ингибитор − вещество, снижающее скорость ферментативной реакции.
По механизму действия ингибирование бывает обратимое и необратимое.
Обратимое ингибирование:
Ингибитор − вещество, снижающее скорость ферментативной реакции.
По механизму действия ингибирование бывает обратимое и необратимое.
Обратимое ингибирование:
Слайд 25Конкурентное ингибирование
Ингибитор по своему строению похож на молекулу субстрата. Ингибитор и
субстрат конкурируют за активный центр. Конкурентное ингибирование можно снять за счет избыточного добавления субстрата. При конкурентном ингибировании υmax не меняется. Меняется лишь сродство фермента к субстрату.
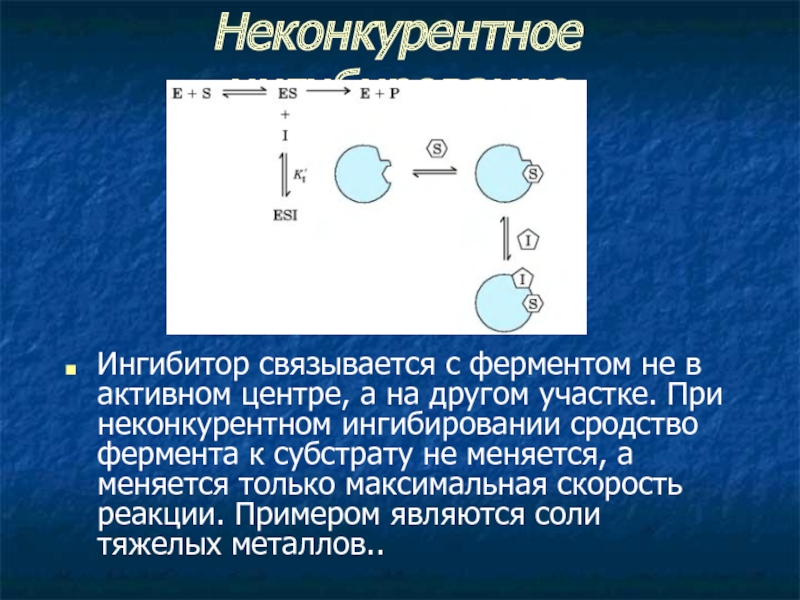
Слайд 26Неконкурентное ингибирование
Ингибитор связывается с ферментом не в активном центре, а на
другом участке. При неконкурентном ингибировании сродство фермента к субстрату не меняется, а меняется только максимальная скорость реакции. Примером являются соли тяжелых металлов..
Слайд 28бесконкурентное ингибирование
При это меняются максимальная скорость и сродство к субстрату бесконкурентное
ингибирование
Меняются максимальная скорость и сродство к субстрату.
Меняются максимальная скорость и сродство к субстрату.
Слайд 29Аллостерические ферменты.
не подчиняются уравнению Михаэлиса-Ментен. Это всегда олигомерные белки, т.е. белки
состоящие из нескольких субъединиц. Количество их может варьировать от 2 до 12.
Обязательным условием является наличие нескольких конформаций его субъединиц.
Для них характерно наличие как активных центров, так и дополнительных центров связывания с которыми связываются аллостерические модуляторы.
Обязательным условием является наличие нескольких конформаций его субъединиц.
Для них характерно наличие как активных центров, так и дополнительных центров связывания с которыми связываются аллостерические модуляторы.
Слайд 30
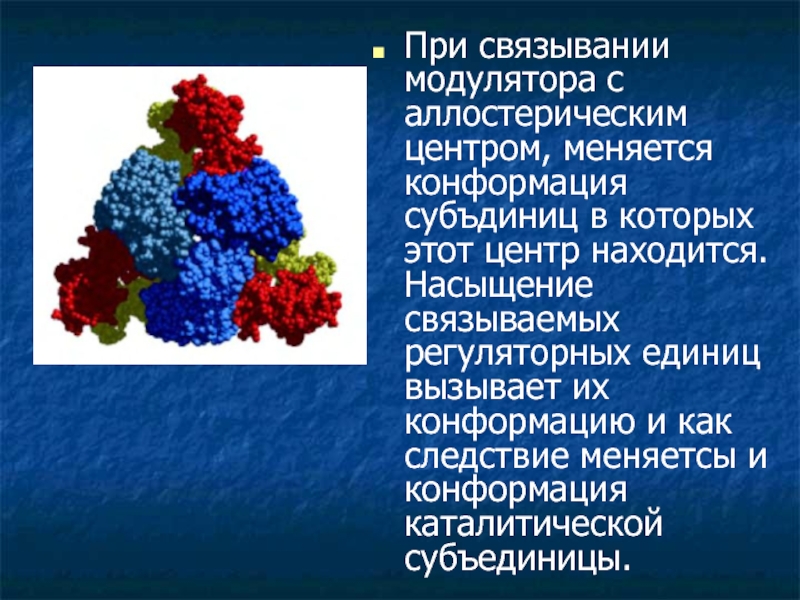
При связывании модулятора с аллостерическим центром, меняется конформация субъдиниц в которых
этот центр находится. Насыщение связываемых регуляторных единиц вызывает их конформацию и как следствие меняетсы и конформация каталитической субъединицы.
Слайд 31
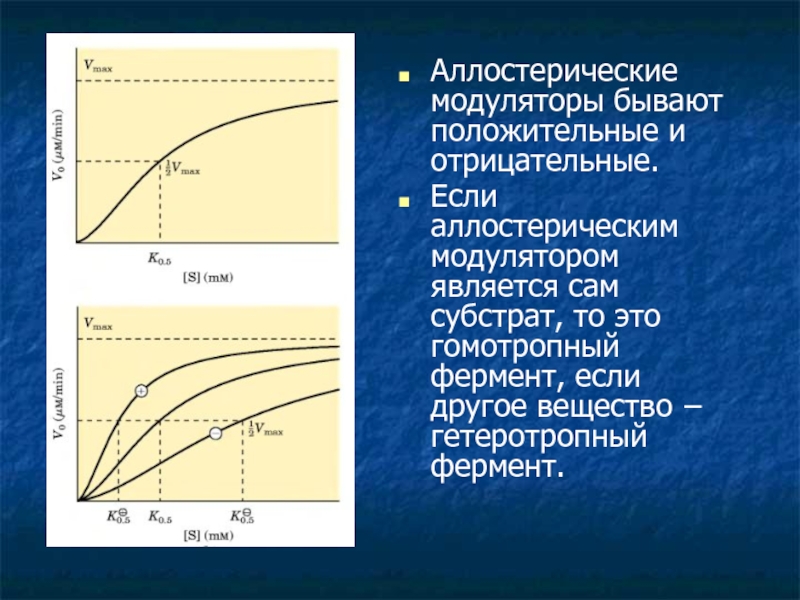
Аллостерические модуляторы бывают положительные и отрицательные.
Если аллостерическим модулятором является сам субстрат,
то это гомотропный фермент, если другое вещество − гетеротропный фермент.
Слайд 32Ковалентная модификация.
Ферменты, регулируемые с помощью ковалентной модификации, могут присоединять либо отщеплять
специальные функциональные группы, при этом переходя в более активное состояние. Чаще всего такой функциональной группой является остаток фосфорной кислоты, т.е. фермент фосфорилируется либо дефосфорилируется. В результате присоединения фосфатной группы меняется конформация и активность фермента. Фермент, осуществляющий фосфорилирование, является киназа.






![Факторы, влияющие на активность ферментаКонцентрация субстрата.В 1913г. Михаэлис и Ментен проедложили уравнениеυ = υmax[S]/Km+[S]](/img/tmb/5/422567/7e67f2d20cca5fa5ae2f4eb8cce2dcfa-800x.jpg)