- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Ферменты, их сходство и отличие от неорганических катализаторов. Коферменты презентация
Содержание
- 1. Ферменты, их сходство и отличие от неорганических катализаторов. Коферменты
- 2. ПЛАН ЛЕКЦИИ: 1. Химическая природа и
- 3. Ферменты – биокатализаторы белковой природы.
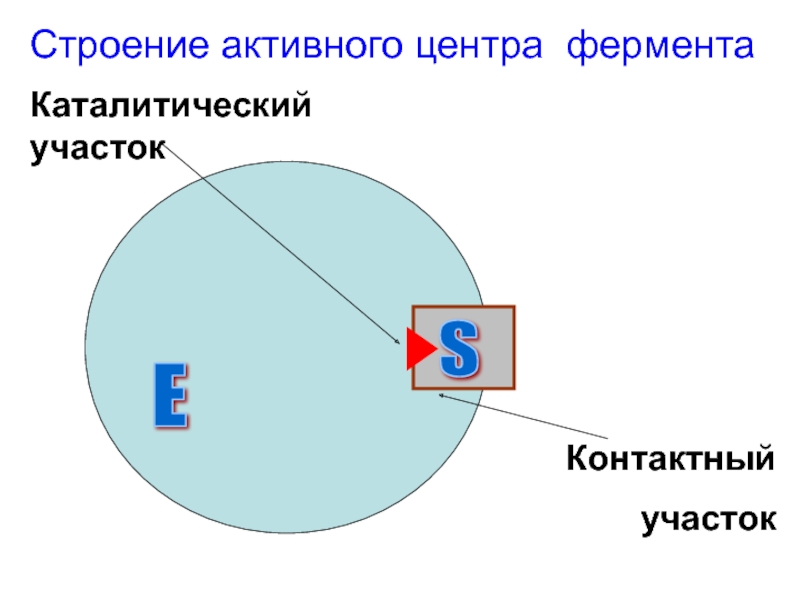
- 4. Строение активного центра фермента Е S Каталитический участок Контактный участок
- 5. ОБЩИЕ ЧЕРТЫ ФЕРМЕНТОВ И НЕБИОЛОГИЧЕСКИХ КАТАЛИЗАТОРОВ:
- 6. ОТЛИЧИТЕЛЬНЫЕ ПРИЗНАКИ ФЕРМЕНТОВ: 1 .Ферменты обладают более
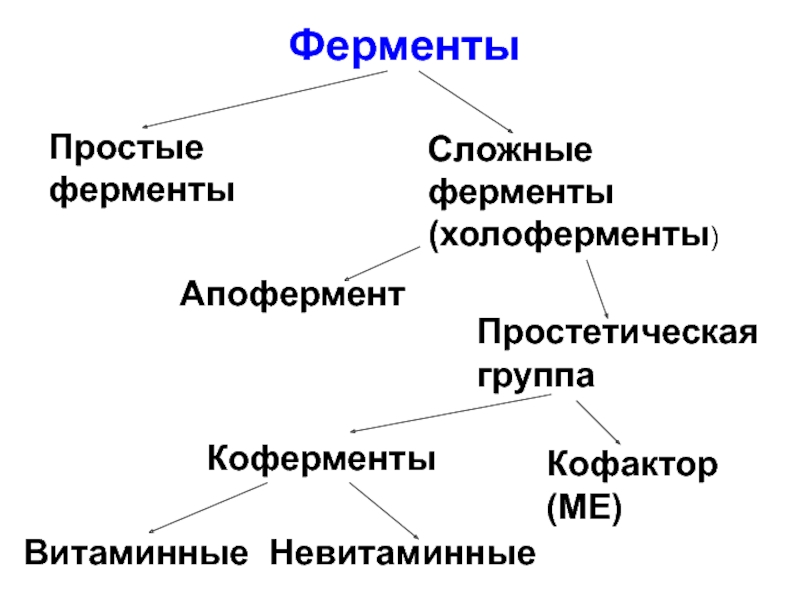
- 7. Ферменты Простые ферменты Сложные ферменты (холоферменты) Апофермент Простетическая группа Кофактор (МЕ) Витаминные Невитаминные Коферменты
- 8. Коферменты: Витаминные: тиаминовые ; флавиновые; пантотеновые;
- 9. Тиаминовые коферменты Производные витамина B1
- 10. Флавиновые коферменты Производные витамина B2
- 11. Пантотеновые коферменты Производные пантотеновой кислоты); Основной
- 12. Никотинамидные коферменты Производные витамина РР
- 14. Пиридоксиновые коферменты Производные витамина В6 (пиридоксин);
- 15. Номенклатура ферментов Тривиальная - пепсин
- 16. Шифр 1-номер класса
- 17. Классификация ферментов В основе лежит тип катализируемой
- 18. Оксидоредуктазы Катализируют окислительно - восстановительные реакции Подклассы: дегидрогеназы; оксидазы; оксигеназы.
- 21. Трансферазы ускоряют реакции транспорта групп атомов от
- 22. Реакция трансаминирования
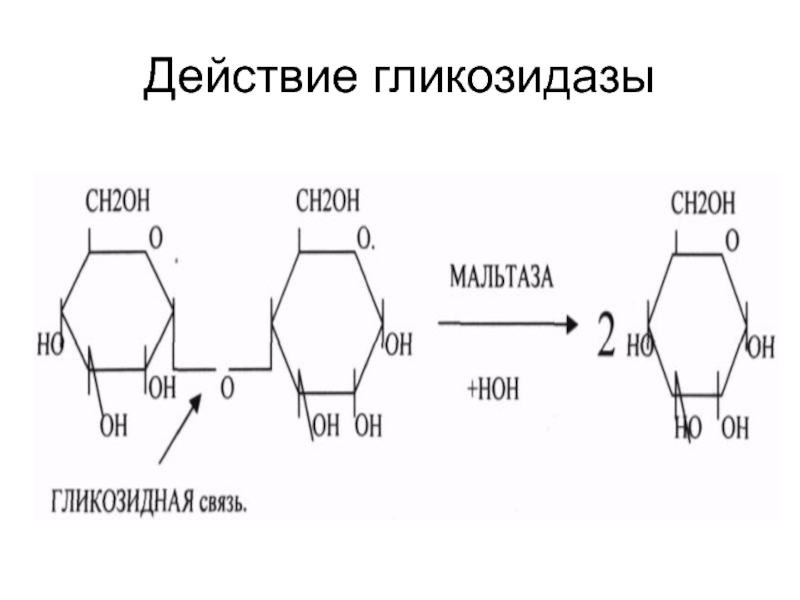
- 23. Гидролазы катализируют реакции разрыва связей в молекулах
- 24. Действие эстеразы:
- 25. Действие гликозидазы
- 26. Лиазы ускоряют отщепление негидролитическим путем групп: СООН, NH2, SH2; присоединение воды по двойной связи.
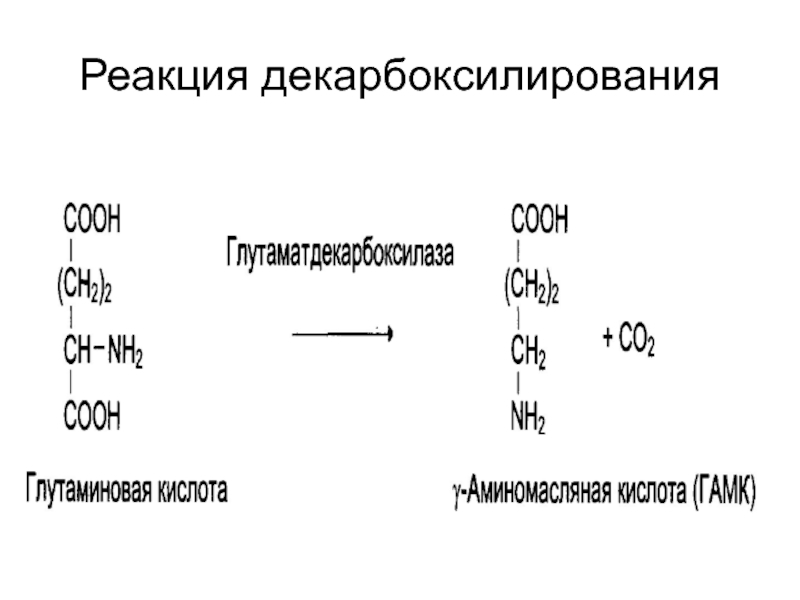
- 27. Реакция декарбоксилирования
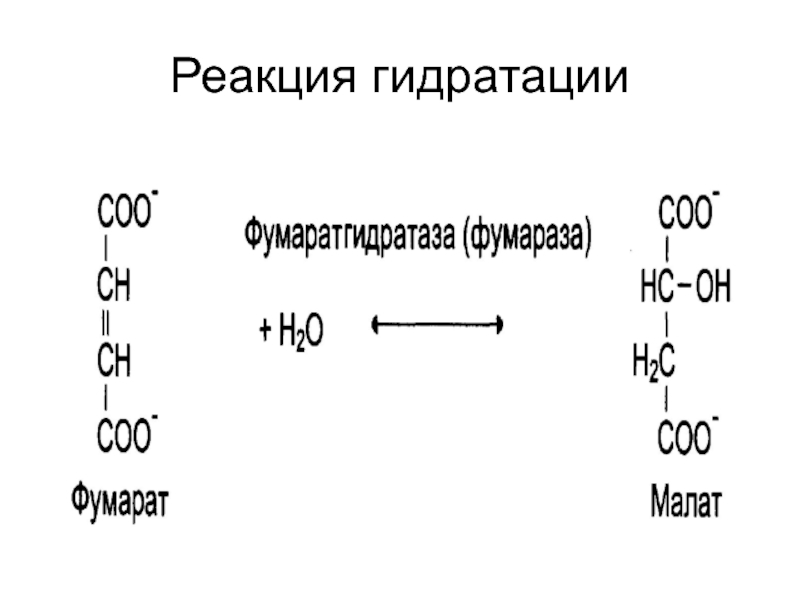
- 28. Реакция гидратации
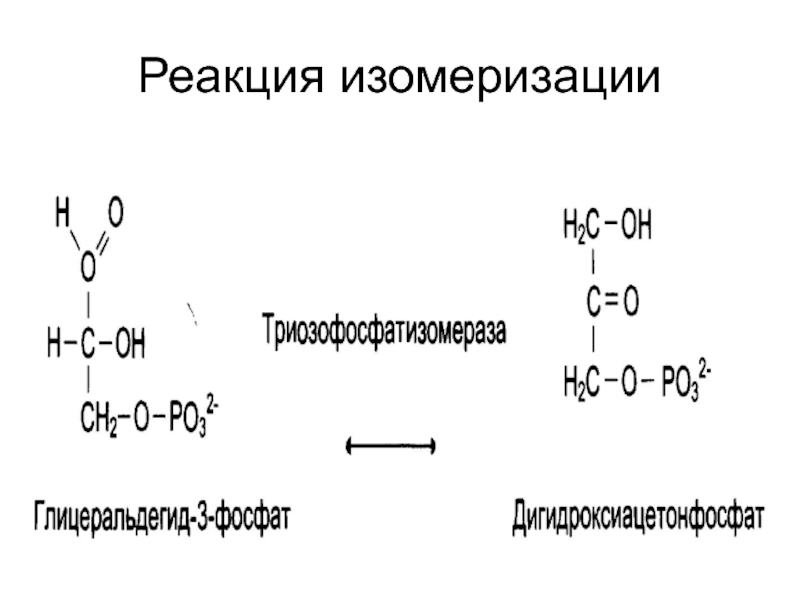
- 29. Изомеразы катализируют реакции изомеризации. Выделяют: «истинные изомеразы»; мутазы
- 30. Реакция изомеризации
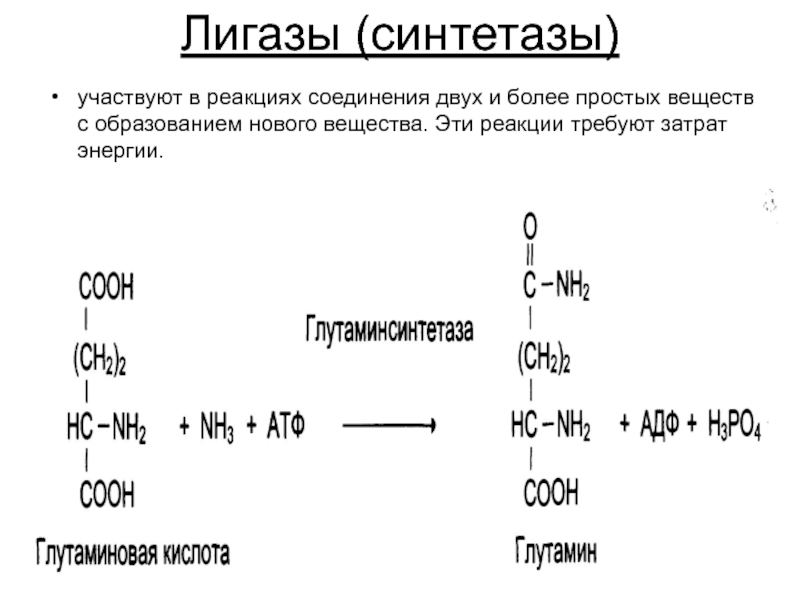
- 31. Лигазы (синтетазы) участвуют в реакциях соединения двух
- 32. Свойства ферментов: высокая каталитическая активность; специфичность действия;
- 33. Специфичность действия Субстратная абсолютная; групповая;
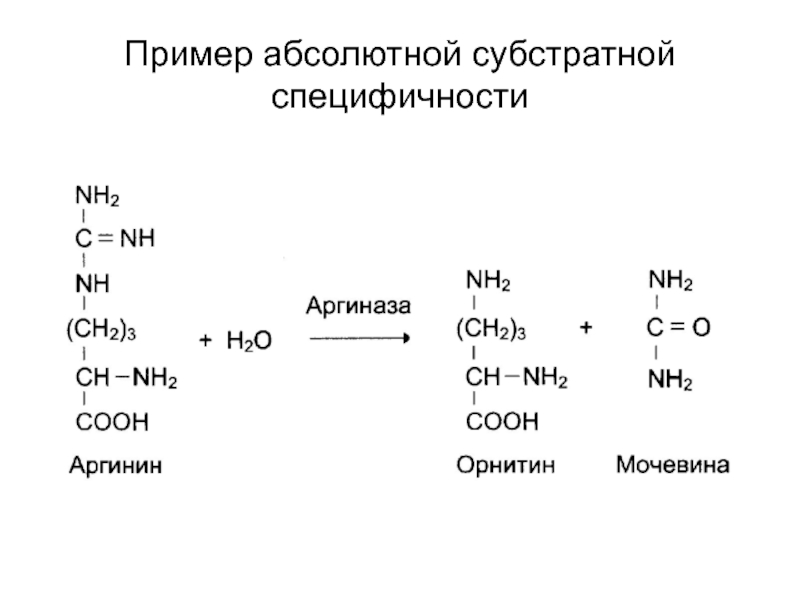
- 34. Пример абсолютной субстратной специфичности
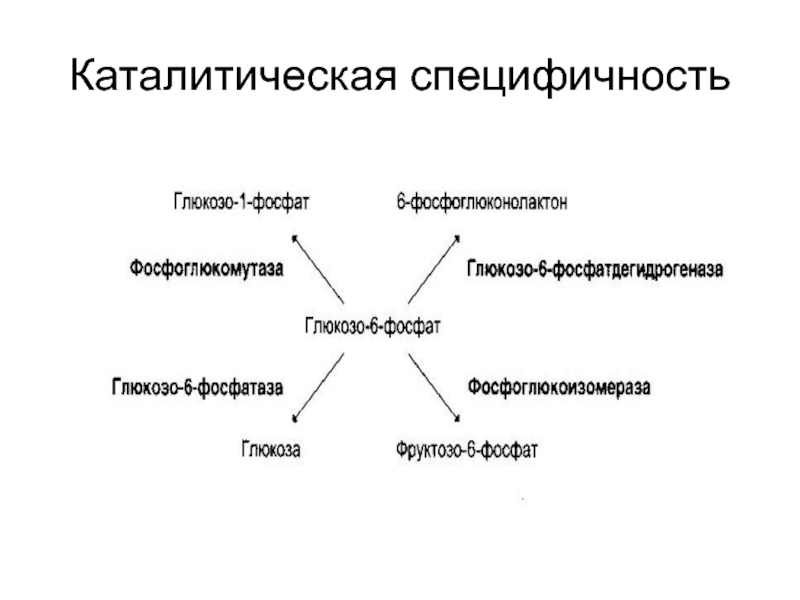
- 35. Каталитическая специфичность
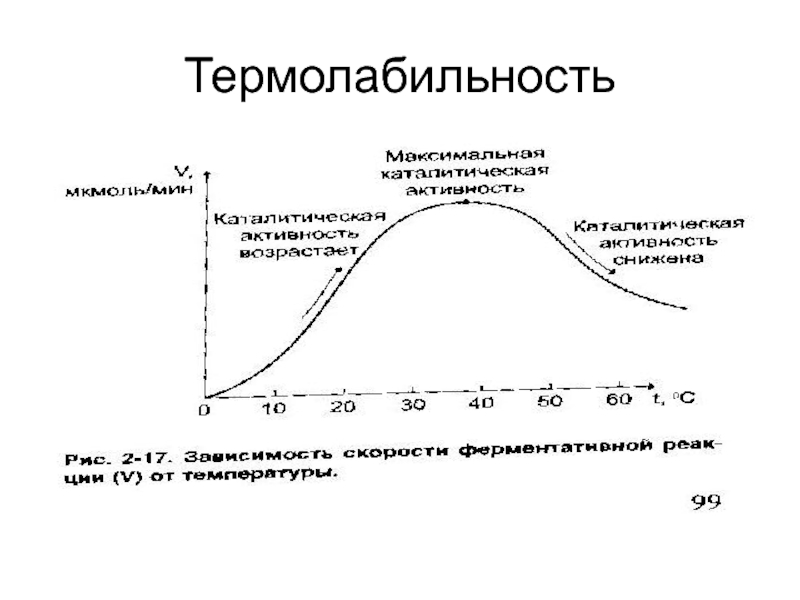
- 36. Термолабильность
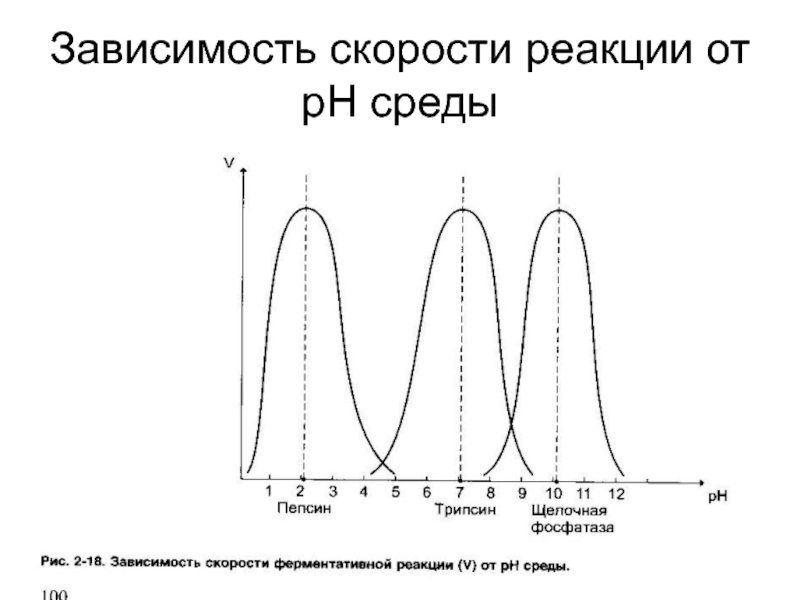
- 37. Зависимость скорости реакции от рН среды
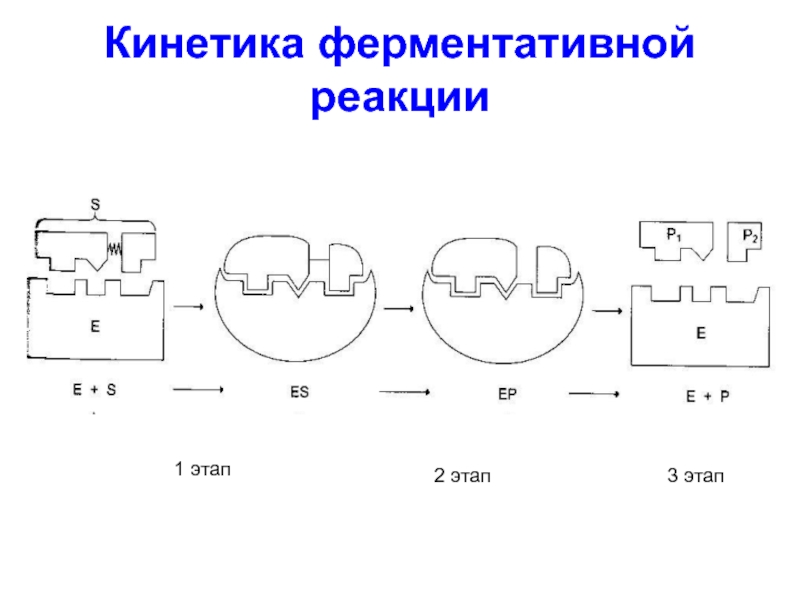
- 38. Кинетика ферментативной реакции 1 этап 3 этап 2 этап
- 39. Молекулярные эффекты: Эффект концентрирования; Эффект ориентации;
- 40. Ингибирование ферментативной активности снижение каталитической активности в
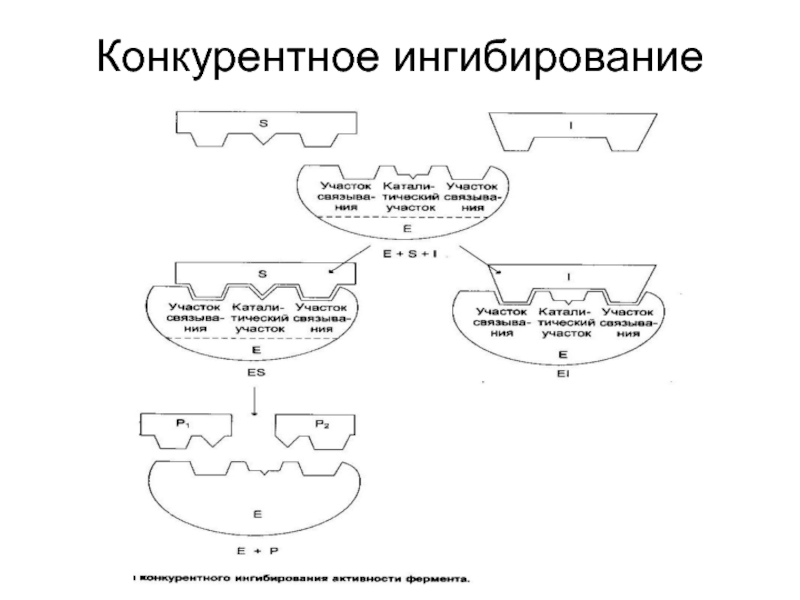
- 41. Конкурентное ингибирование
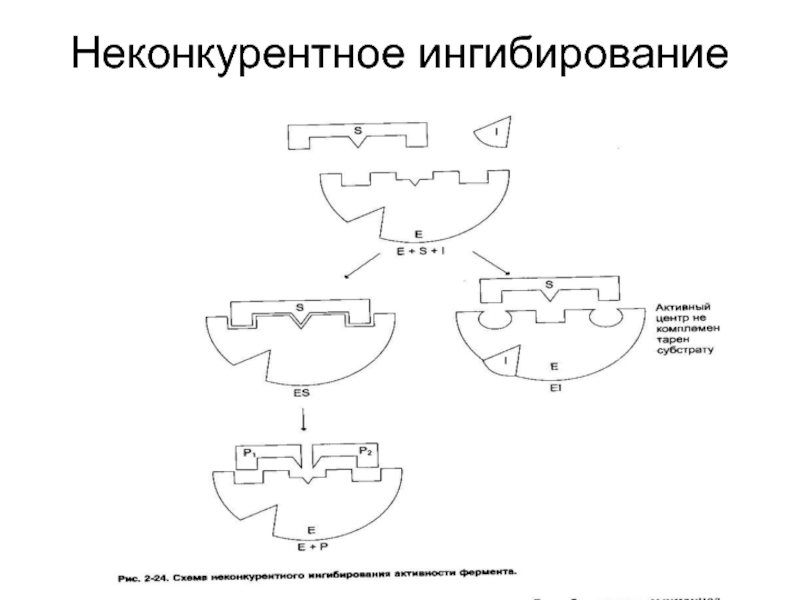
- 42. Неконкурентное ингибирование
- 43. Способы регуляции активности ферментов: Аллостерическая регуляция;
- 44. Аллостерическая регуляция
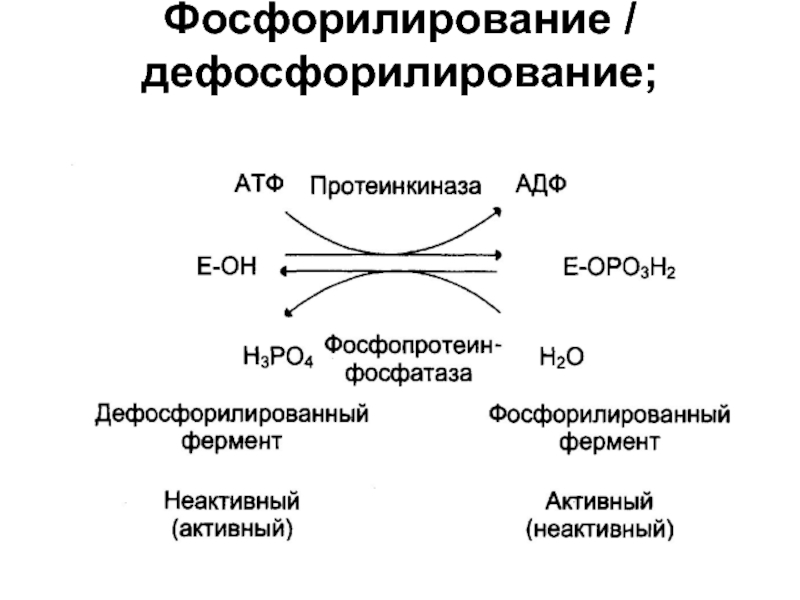
- 45. Фосфорилирование / дефосфорилирование;
Слайд 2ПЛАН ЛЕКЦИИ:
1. Химическая природа и структурная организация ферментов;
2. Сходства и отличия
ферментов и неорганических катализаторов;
3. Коферменты, классификация, функции;
4. Классификация и номенклатура ферментов;
5. Свойства ферментов;
6. Механизм действия ферментов;
7. Ингибирование ферментативной активности;
8. Регуляция активности ферментов.
3. Коферменты, классификация, функции;
4. Классификация и номенклатура ферментов;
5. Свойства ферментов;
6. Механизм действия ферментов;
7. Ингибирование ферментативной активности;
8. Регуляция активности ферментов.
Слайд 3Ферменты – биокатализаторы белковой природы.
Рибозимы - биокатализаторы, по химической природе РНК.
Рибозимы
катализируют разрыв фосфодиэфирных связей нуклеиновых кислот.
Слайд 5ОБЩИЕ ЧЕРТЫ ФЕРМЕНТОВ И НЕБИОЛОГИЧЕСКИХ КАТАЛИЗАТОРОВ:
Повышают скорость реакции;
В реакциях
не расходуются;
Для обратимых процессов и прямая, и обратная реакция катализируется одним и тем же ферментом.
Для обратимых процессов и прямая, и обратная реакция катализируется одним и тем же ферментом.
Слайд 6ОТЛИЧИТЕЛЬНЫЕ ПРИЗНАКИ ФЕРМЕНТОВ:
1 .Ферменты обладают более высокой эффективностью действия (повышают скорость
реакции в большее число раз, чем неорганические катализаторы).
2.Ферменты чувствительны к температуре (термолабильны)
3.Ферменты чувствительны к значениям рН среды.
4.Специфичность действия.
5.Ферменты - это катализаторы с регулируемой активностью.
2.Ферменты чувствительны к температуре (термолабильны)
3.Ферменты чувствительны к значениям рН среды.
4.Специфичность действия.
5.Ферменты - это катализаторы с регулируемой активностью.
Слайд 7Ферменты
Простые ферменты
Сложные ферменты (холоферменты)
Апофермент
Простетическая группа
Кофактор
(МЕ)
Витаминные
Невитаминные
Коферменты
Слайд 8Коферменты:
Витаминные:
тиаминовые ;
флавиновые;
пантотеновые;
никотинамидные;
пиридоксиновые.
Невитаминные:
нуклеотиды;
производные порфирина;
глутатион.
Слайд 9Тиаминовые коферменты
Производные витамина B1 (тиамина);
Участвуют в реакциях декарбоксилирования кетокислот (входят
в состав пируватдегидрогеназного и α-кетоглутаратдегидрогеназного комплексов);
Являются коферментами транскетолаз (распад глюкозы);
Основной представитель тиаминдифосфат (ТДФ).
Являются коферментами транскетолаз (распад глюкозы);
Основной представитель тиаминдифосфат (ТДФ).
Слайд 10Флавиновые коферменты
Производные витамина B2 (рибофлавина);
ФМН – флавинмононуклеотид;
ФАД – флавинадениндинуклеотид;
Могут быть
в окисленной и восстановленной формах;
Коферменты дегидрогеназ.
Коферменты дегидрогеназ.
Слайд 11Пантотеновые коферменты
Производные пантотеновой кислоты);
Основной представитель – кофермент А;
Участвует:
в переносе
кислотных остатков;
Синтезе холестерола и кетоновых тел;
Активации жирных кислот;
Обезвреживании ксенобиотиков.
Синтезе холестерола и кетоновых тел;
Активации жирных кислот;
Обезвреживании ксенобиотиков.
Слайд 12Никотинамидные коферменты
Производные витамина РР (никотинамид);
НАД (никотинамидадениндинуклеотид);
НАДФ (никотинамидадениндинуклеотидфосфат);
Коферменты могут быть в
окисленной и восстановленной формах;
НАД и НАДФ связаны с ферментами дегидрогеназами, которые в окислительно-восстановительных реакциях.
НАД и НАДФ связаны с ферментами дегидрогеназами, которые в окислительно-восстановительных реакциях.
Слайд 14Пиридоксиновые коферменты
Производные витамина В6 (пиридоксин);
Кофермент – пиридоксальфосфат;
Участвует в :
Реакциях переаминирования
(трансаминирование). Связан с ферментами аминотрансферазами;
Реакциях декарбоксилирования аминокислот.
Реакциях декарбоксилирования аминокислот.
Слайд 15Номенклатура ферментов
Тривиальная - пепсин
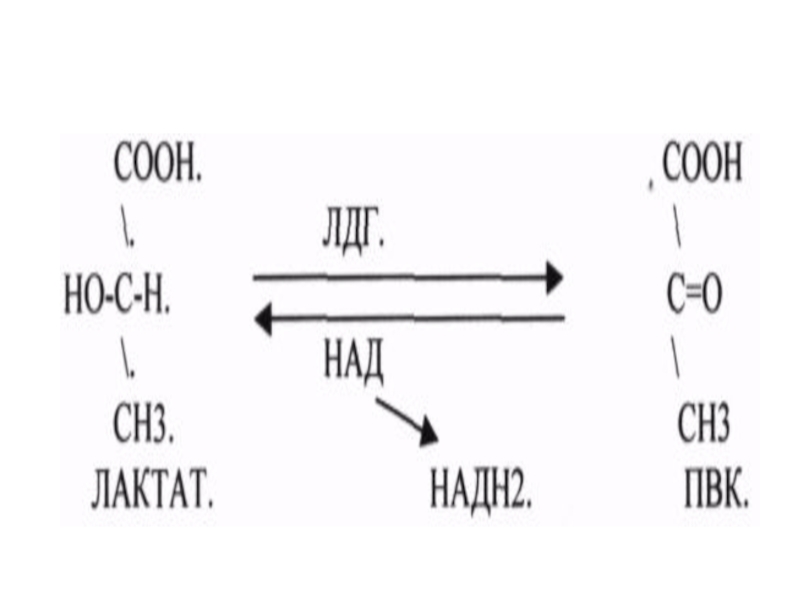
Рабочая - лактатдегидрогеназа
Систематическая - L-лактат:НАД
- оксидоредуктаза
Слайд 16Шифр
1-номер класса
2-номер подкласса
3-номер подподкласса
4-индивидуальный номер фермента в подподклассе
1.1.1.27 - ЛДГ
1.1.1.27 - ЛДГ
Слайд 17Классификация ферментов
В основе лежит тип катализируемой реакции
1. Оксидоредуктазы
2. Трансферазы
3. Гидролазы
4. Лиазы
5. Изомеразы
6. Синтетазы
4. Лиазы
5. Изомеразы
6. Синтетазы
Слайд 18Оксидоредуктазы
Катализируют окислительно - восстановительные реакции
Подклассы:
дегидрогеназы;
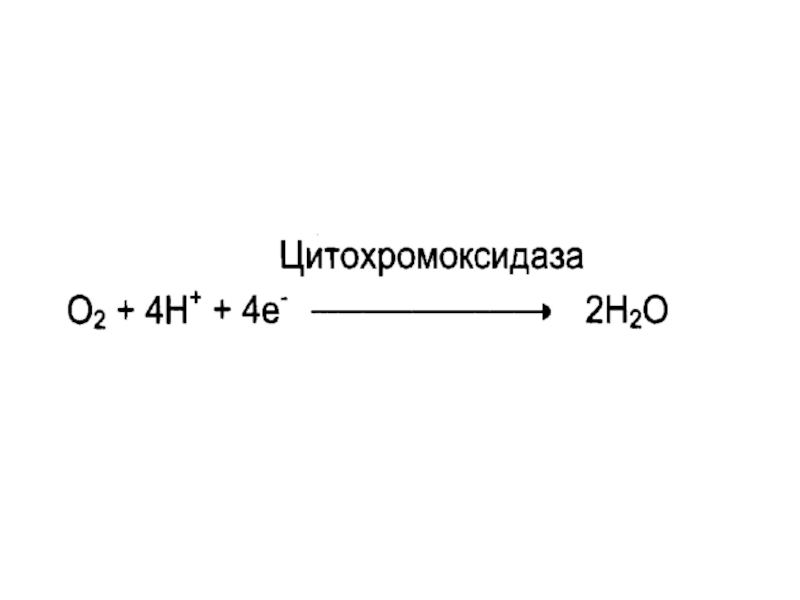
оксидазы;
оксигеназы.
Слайд 21Трансферазы
ускоряют реакции транспорта групп атомов от одного субстрата к другому.
Подклассы
(в зависимости от переносимых групп):
аминотрансферазы;
метилтрансферазы;
фосфотрансферазы (киназы);
ацилтрансферазы;
гликозилтрансферазы
аминотрансферазы;
метилтрансферазы;
фосфотрансферазы (киназы);
ацилтрансферазы;
гликозилтрансферазы
Слайд 23Гидролазы
катализируют реакции разрыва связей в молекулах субстратов при участии воды. При
этом элементы воды присоединяются к свободным единичным валентностям, образовавшимся после разрыва связей.
Подклассы:
эстеразы;
гликозидазы;
пептидазы;
фосфатазы.
Подклассы:
эстеразы;
гликозидазы;
пептидазы;
фосфатазы.
Слайд 26Лиазы
ускоряют отщепление негидролитическим путем групп: СООН, NH2, SH2;
присоединение воды по двойной
связи.
Слайд 31Лигазы (синтетазы)
участвуют в реакциях соединения двух и более простых веществ с
образованием нового вещества. Эти реакции требуют затрат энергии.
Слайд 32Свойства ферментов:
высокая каталитическая активность;
специфичность действия;
термолабильность;
чувствительность к изменению рН среды;
регулируемая активность.
Слайд 33Специфичность действия
Субстратная
абсолютная;
групповая;
стереоспецифичность.
Каталитическая
обеспечивается каталитическим участком;
происходит выбор пути превращения субстрата
Слайд 39Молекулярные эффекты:
Эффект концентрирования;
Эффект ориентации;
Эффект индуцированного
соответствия;
Эффект натяжения связей субстрата;
Эффект кислотно-основного катализа;
Эффект ковалентного катализа.
Эффект натяжения связей субстрата;
Эффект кислотно-основного катализа;
Эффект ковалентного катализа.
Слайд 40Ингибирование ферментативной активности
снижение каталитической активности в присутствии определенных веществ – ингибиторов.
Виды ингибирования:
По механизму (конкурентное, неконкурентное);
По обратимости (обратимое, необратимое);
По специфичности (специфическое, неспецифическое).
По механизму (конкурентное, неконкурентное);
По обратимости (обратимое, необратимое);
По специфичности (специфическое, неспецифическое).
Слайд 43Способы регуляции активности ферментов:
Аллостерическая регуляция;
Регуляция с помощью белок-белковых взаимодействий;
Фосфорилирование / дефосфорилирование;
Частичный
протеолиз.