теме:
«ФЕРМЕНТЫ - 1»
КРАСНОДАР
2009
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Ферменты-1 презентация
Содержание
- 1. Ферменты-1
- 2. Энергия активации катализируемой реакции Полное изменение свободной
- 3. Ферменты Одно-компонентные (только аминокислоты) Двухкомпонентые
- 4. Собственные свойства ферментов Высокая биологическая активность Ферментная
- 5. Строение активного центра фермента
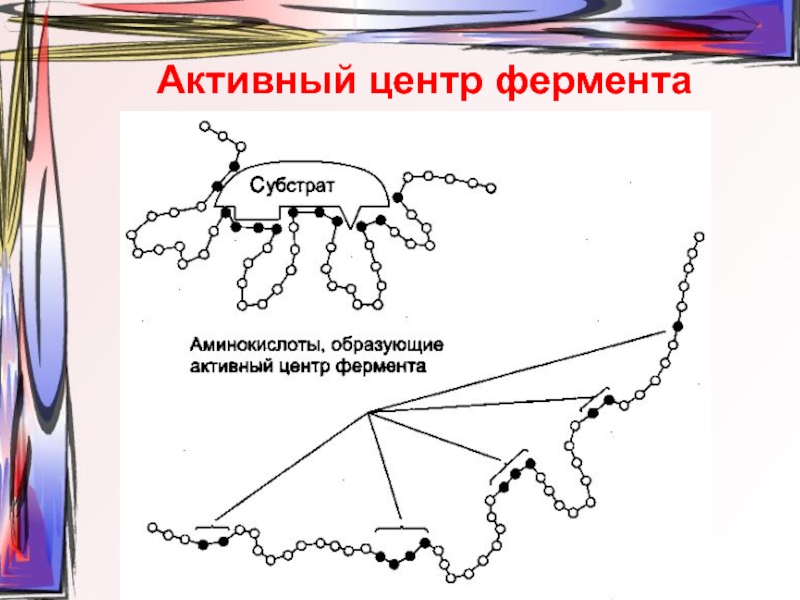
- 6. Активный центр фермента
- 7. Металлы, содержащиеся в ферментах
- 8. Каталитические центры ферментов Ко-А, глутатион, липоевая кислота
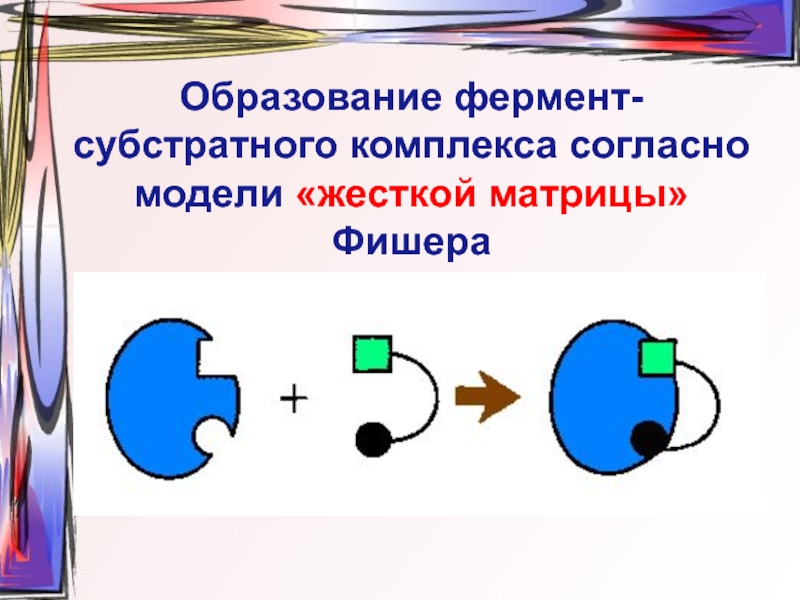
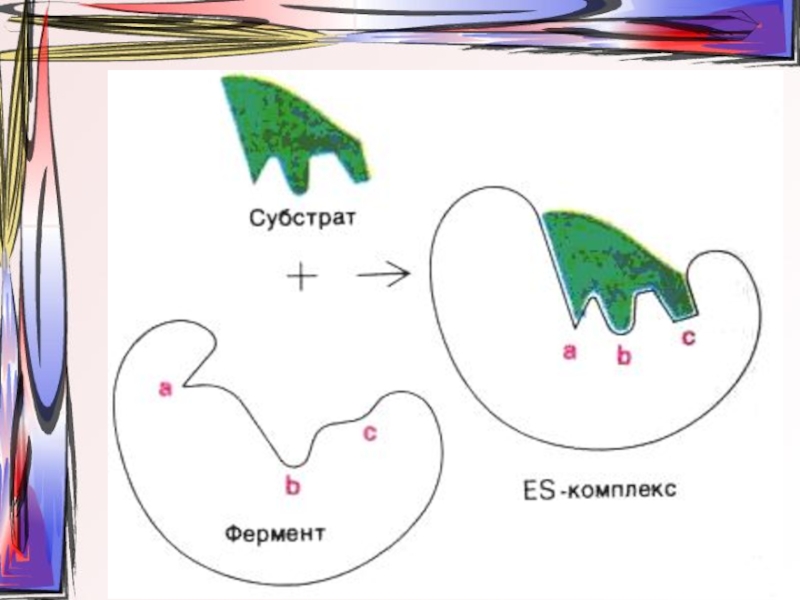
- 9. Образование фермент-субстратного комплекса согласно модели «жесткой матрицы» Фишера
- 11. Схематическое представление конформационных изменений в молекуле фермента
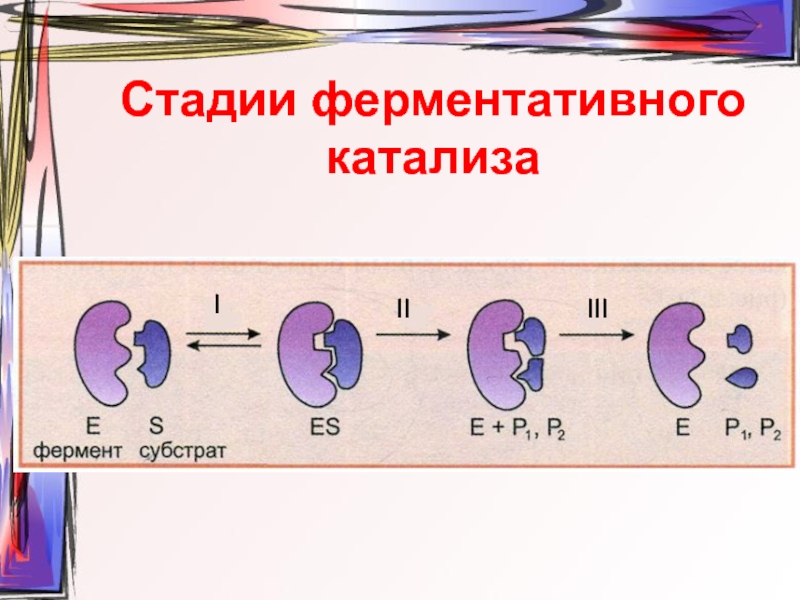
- 13. Общее уравнение ферментативной реакции:
- 14. Стадии ферментативного катализа I III II
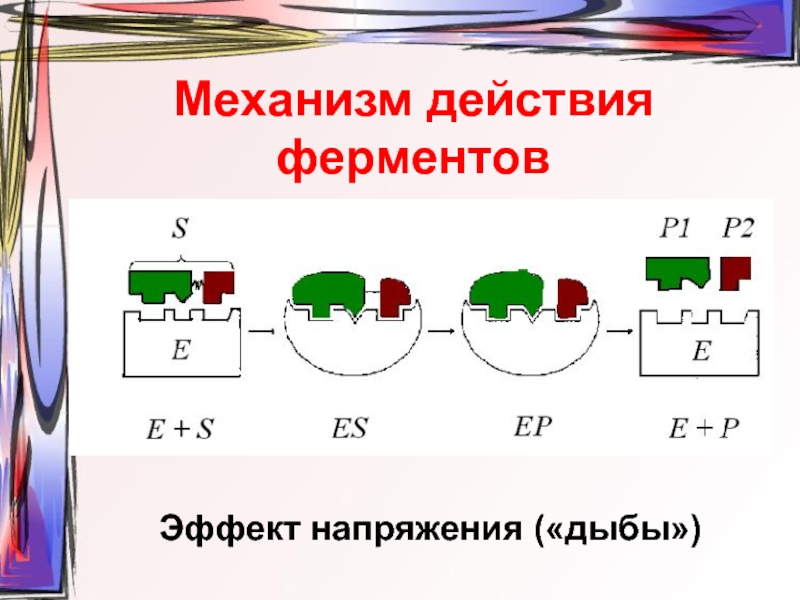
- 15. Механизм действия ферментов Эффект напряжения («дыбы»)
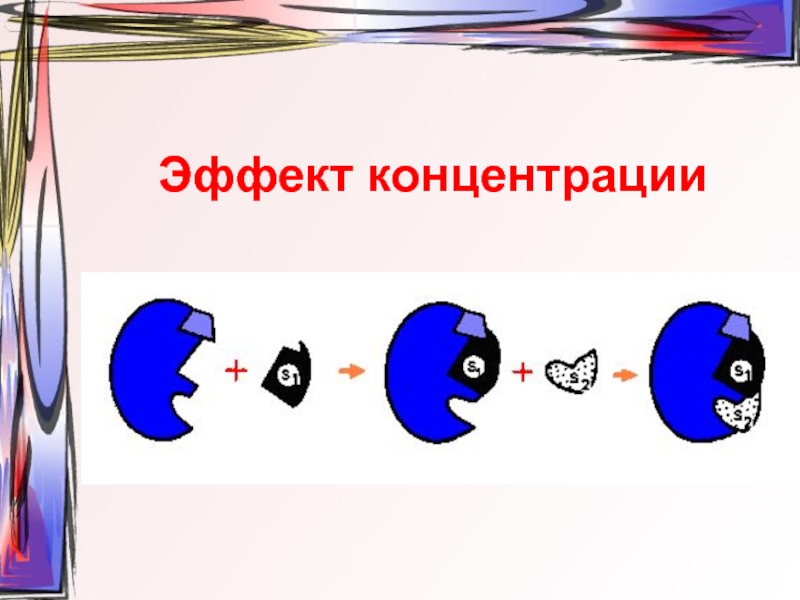
- 16. Эффект концентрации
- 17. Эффект ориентации неправильное
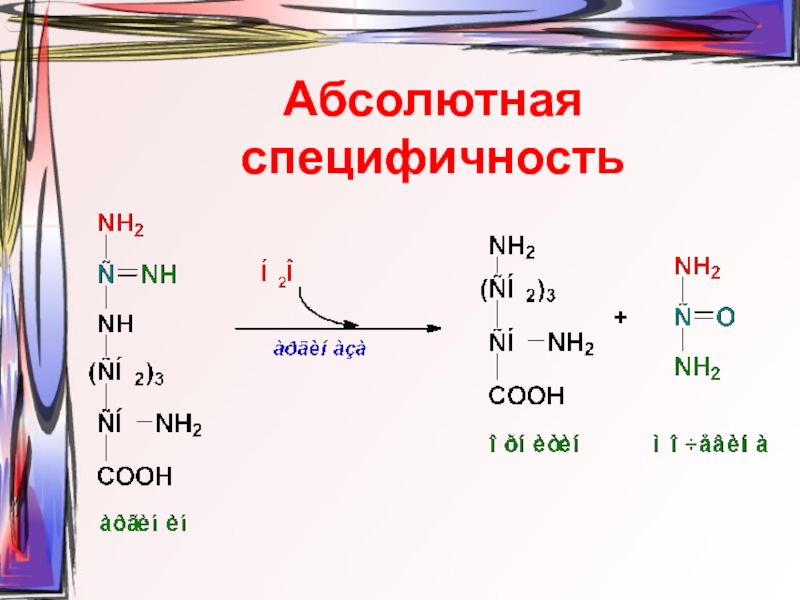
- 18. Абсолютная специфичность
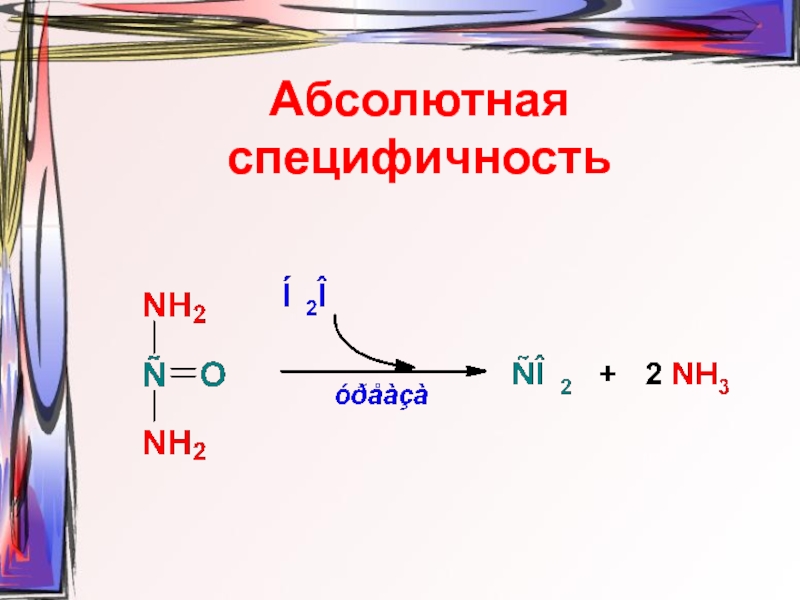
- 19. Абсолютная специфичность
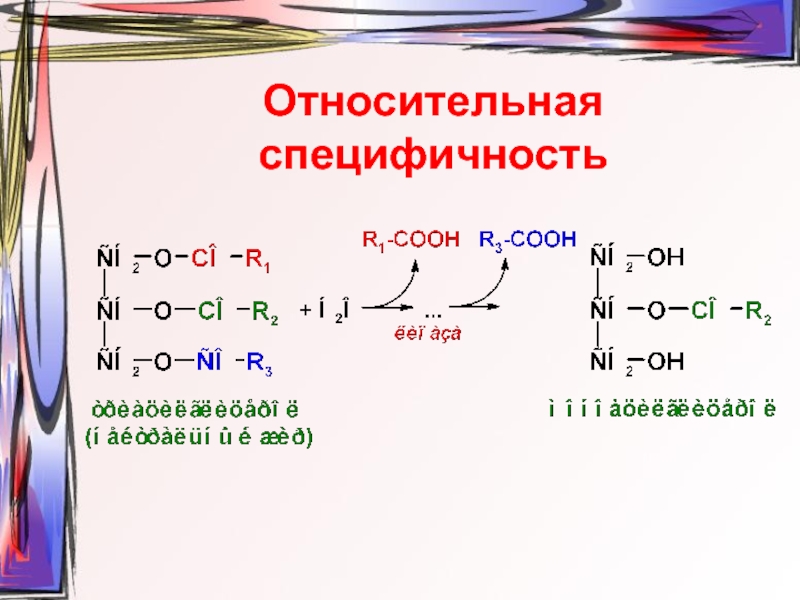
- 20. Относительная специфичность
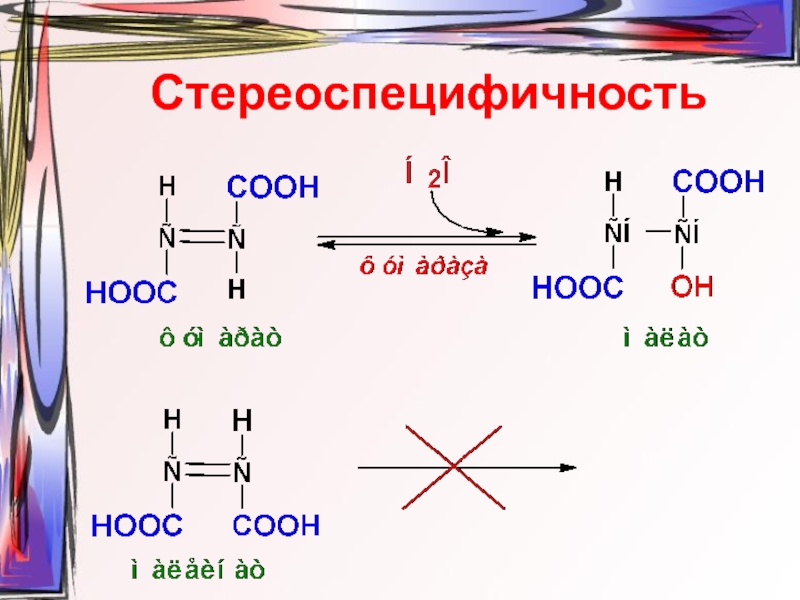
- 21. Стереоспецифичность
- 22. Общее уравнение ферментативной реакции:
- 23. Константа Михаэлиса
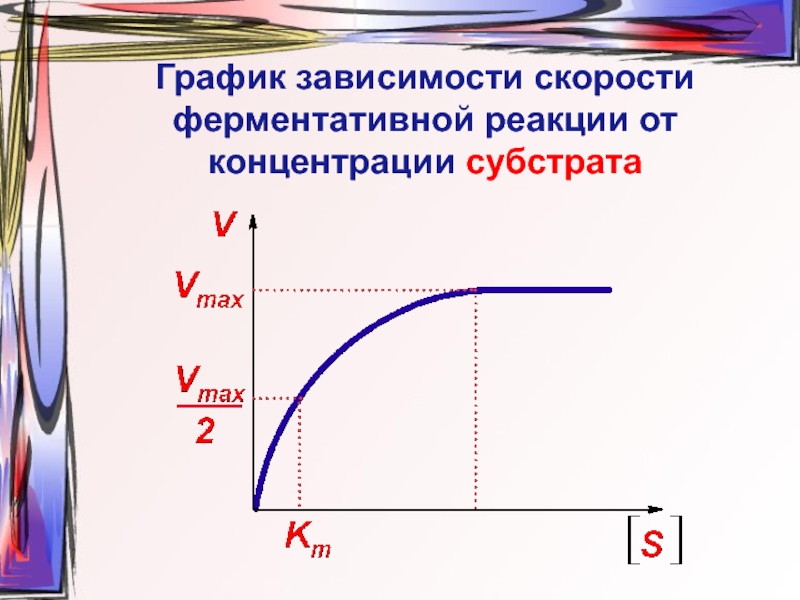
- 24. Зависимость скорости ферментативной реакции от концентрации субстрата
- 25. [S] >> Km; V = Vmax [S]
- 26. График зависимости скорости ферментативной реакции от концентрации субстрата
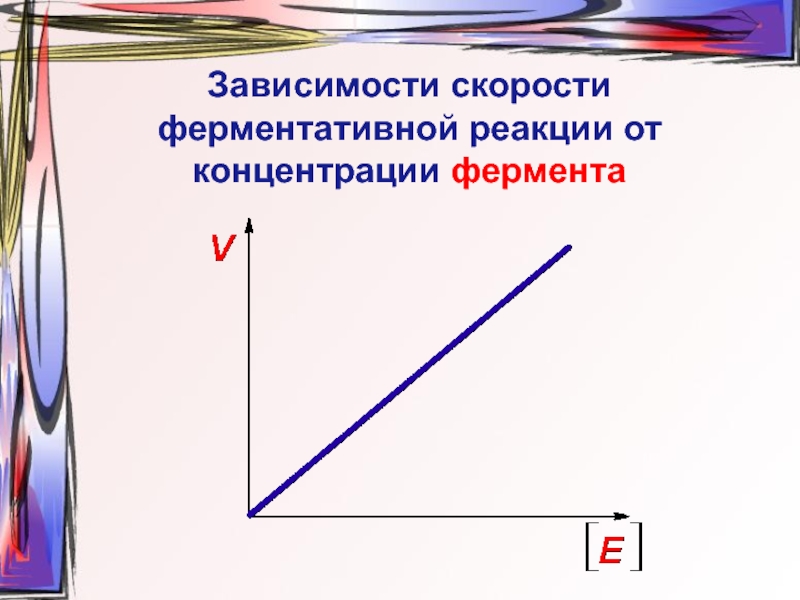
- 27. Зависимости скорости ферментативной реакции от концентрации фермента
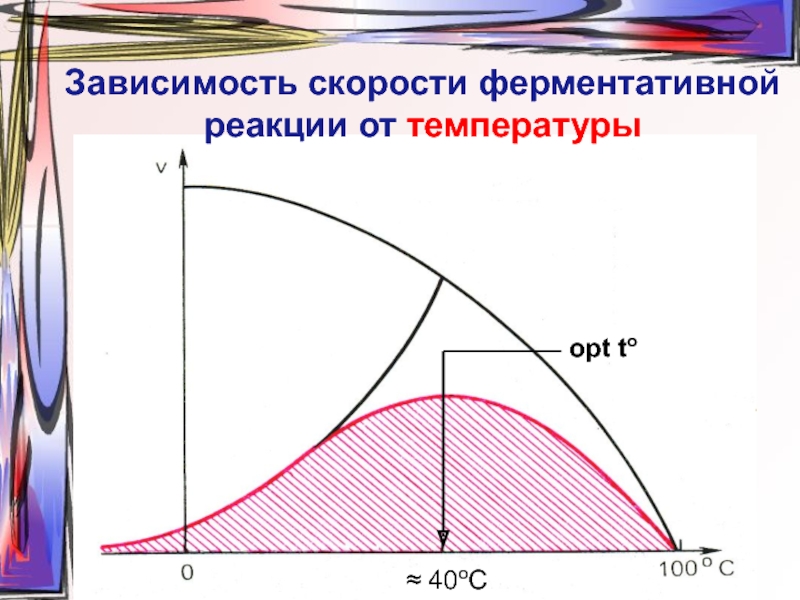
- 28. Зависимость скорости ферментативной реакции от температуры opt to ≈ 40oC
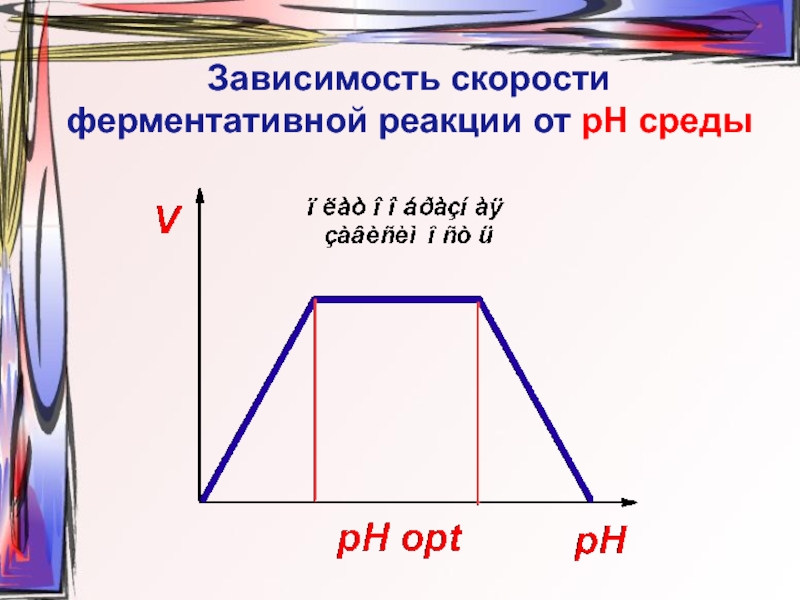
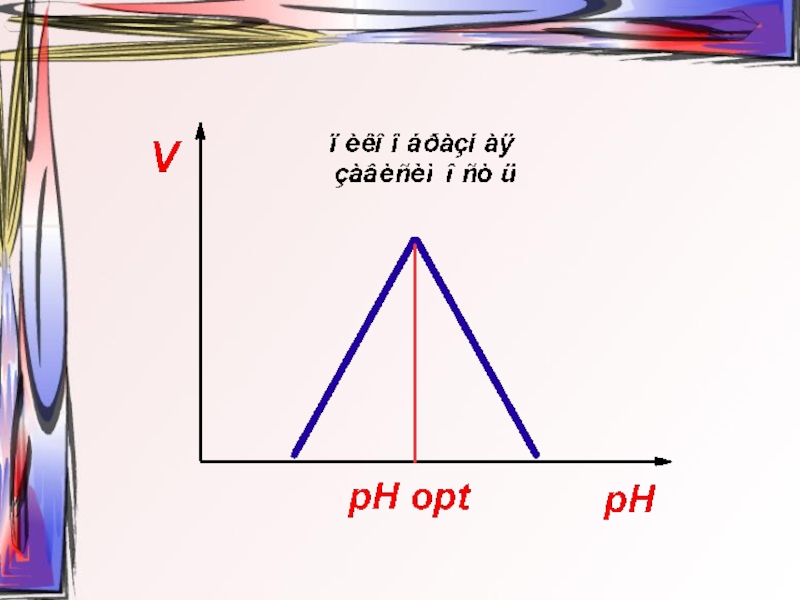
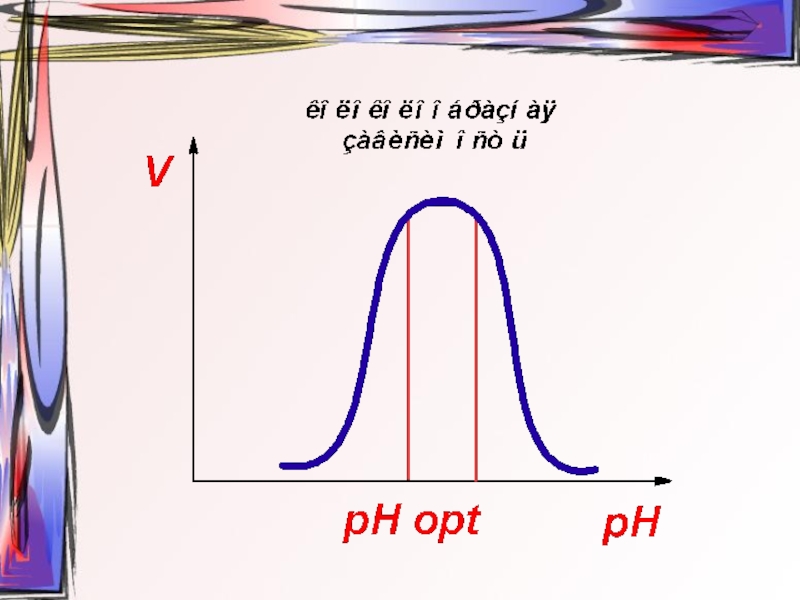
- 29. Зависимость скорости ферментативной реакции от рН среды
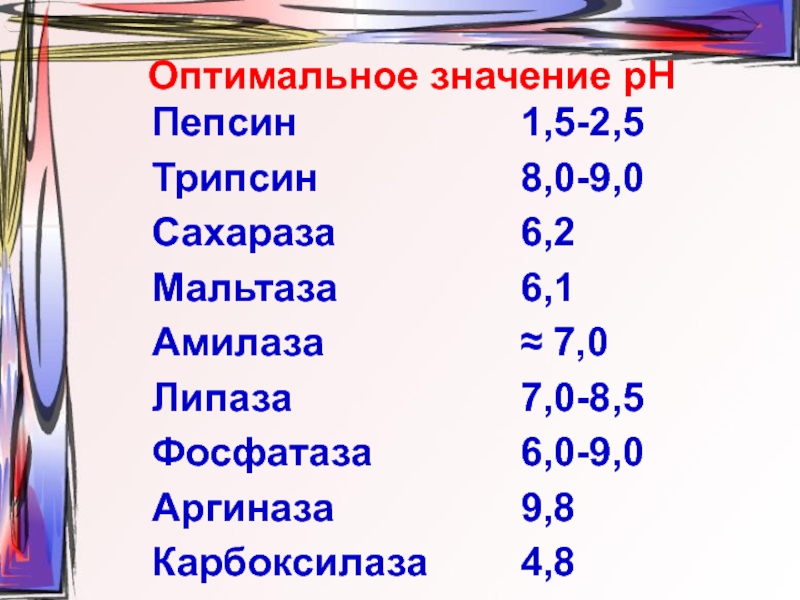
- 32. Оптимальное значение рН Пепсин Трипсин Сахараза Мальтаза
Слайд 1КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
КУБАНСКИЙ МЕДИЦИНСКИЙ ИНСТИТУТ
КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ
Лекция по
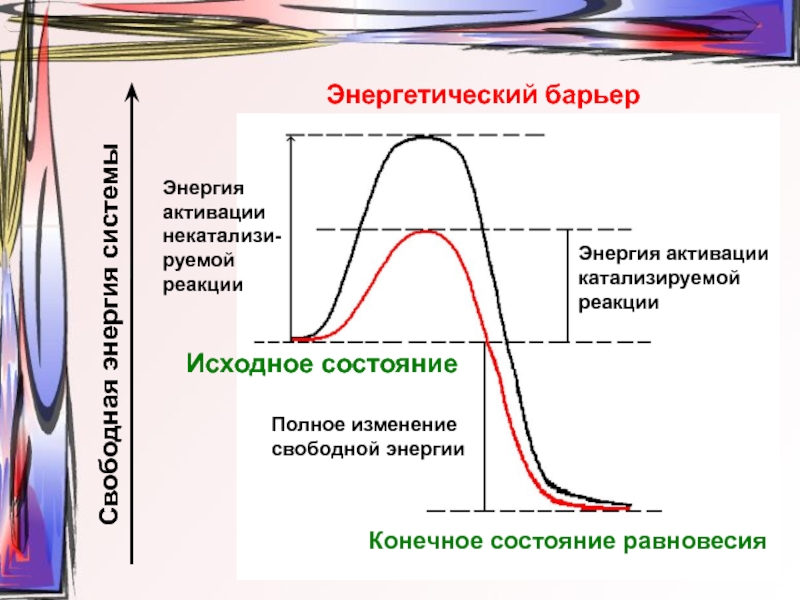
Слайд 2Энергия активации катализируемой реакции
Полное изменение свободной энергии
Энергия активации некатализи-руемой реакции
Исходное состояние
Конечное
состояние равновесия
Энергетический барьер
Свободная энергия системы
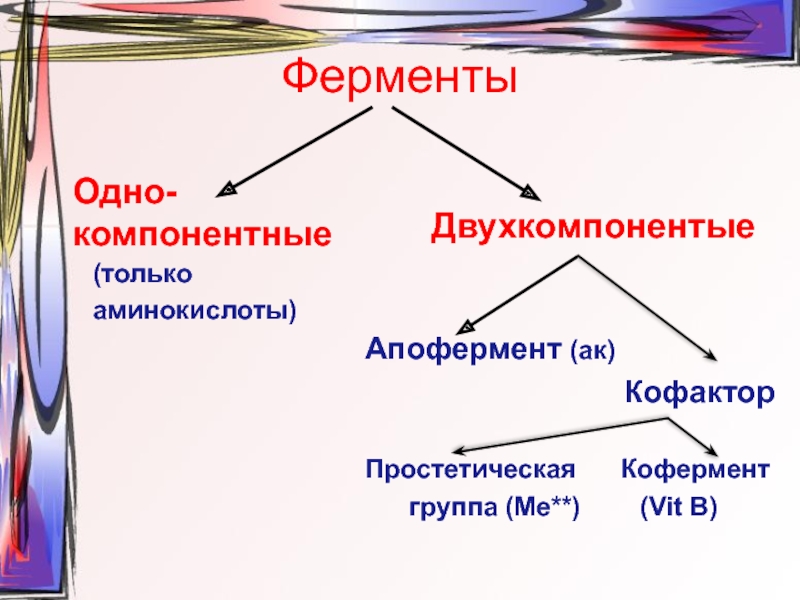
Слайд 3Ферменты
Одно-компонентные
(только
аминокислоты)
Двухкомпонентые
Апофермент (ак)
Кофактор
Простетическая Кофермент
группа (Ме**) (Vit В)
Простетическая Кофермент
группа (Ме**) (Vit В)
Слайд 4Собственные свойства ферментов
Высокая биологическая активность
Ферментная специфичность
действия
субстратная
Иная зависимость от факторов, влияющих на
скорость реакции
Наличие механизмов регуляции активности
Наличие механизмов регуляции активности
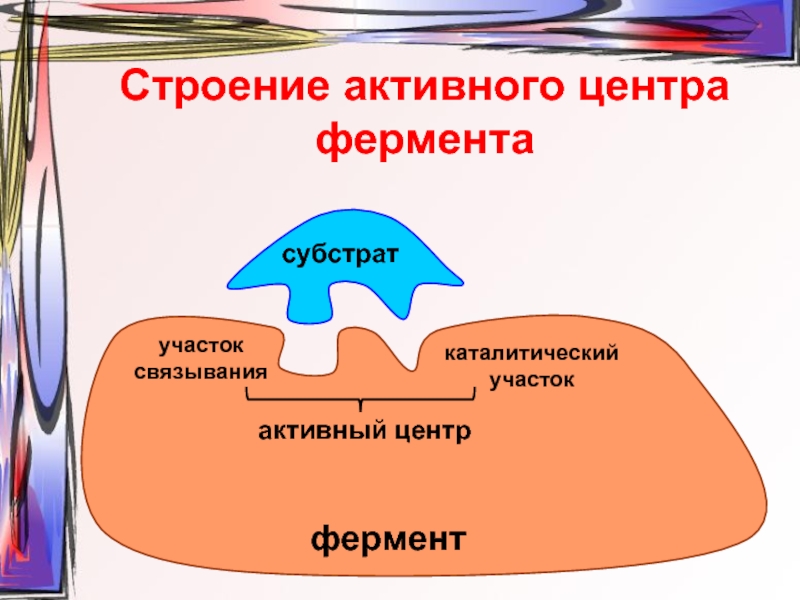
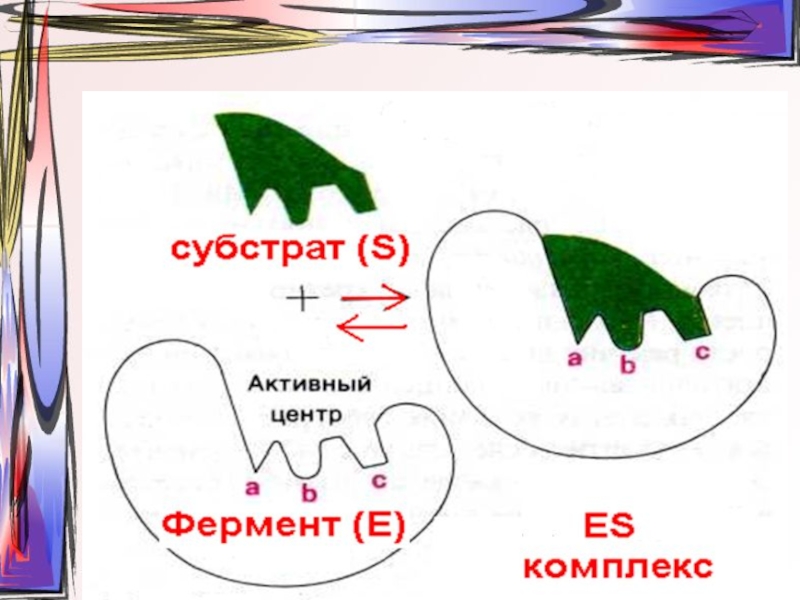
Слайд 5Строение активного центра фермента
субстрат
участок связывания
каталитический участок
активный центр
фермент
Слайд 8Каталитические центры ферментов
Ко-А, глутатион, липоевая кислота
пиридоксальфосфат
тетрагидрофолиевая кислота
флавины
биотин
тиаминпирофосфат
НАД+ и НАДФ+
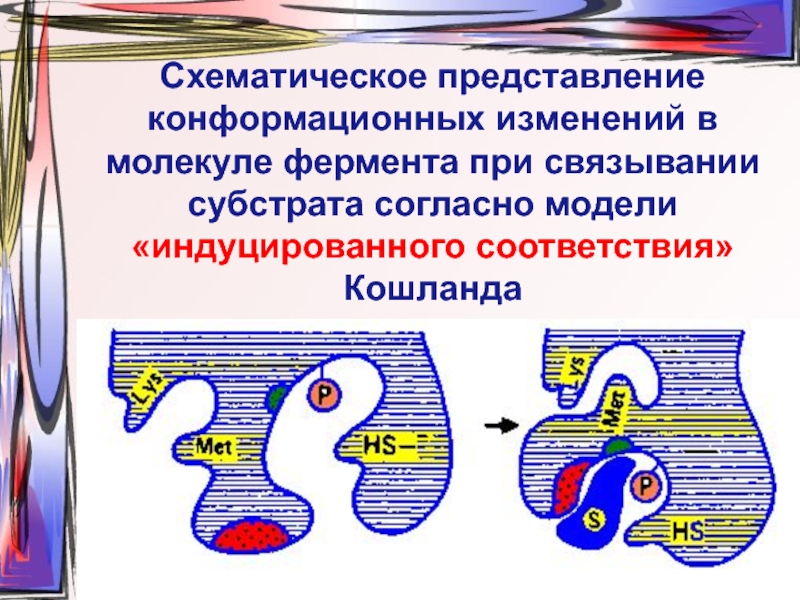
Слайд 11Схематическое представление конформационных изменений в молекуле фермента при связывании субстрата согласно
модели «индуцированного соответствия» Кошланда
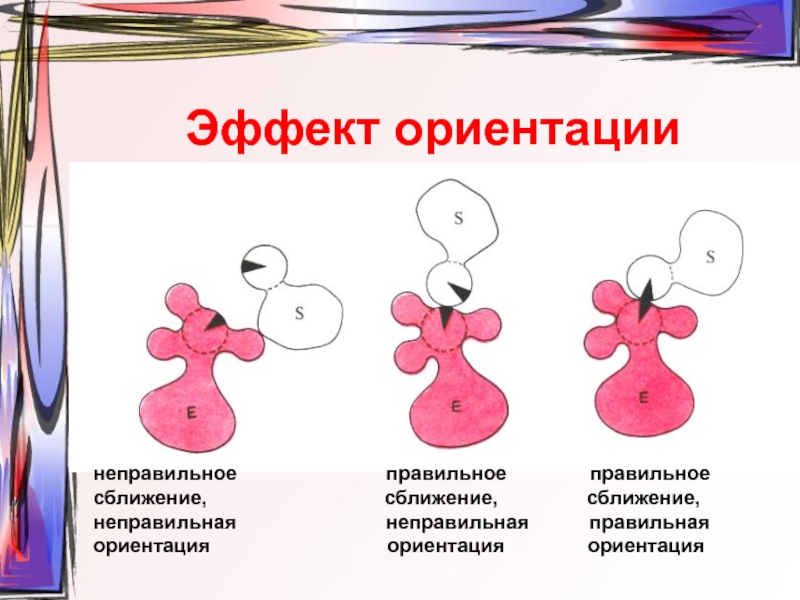
Слайд 17Эффект ориентации
неправильное
правильное правильное
сближение, сближение, сближение,
неправильная неправильная правильная
ориентация ориентация ориентация
сближение, сближение, сближение,
неправильная неправильная правильная
ориентация ориентация ориентация








![[S] >> Km; V = Vmax[S]](/img/tmb/4/355702/de3acc83114165533cf62851154e8a7b-800x.jpg)