* Лекция 8
© проф. Федоренко Борис Николаевич
* Лекция 2
© проф. Федоренко Борис Николаевич
* Лекция 2
проф. Федоренко Борис Николаевич
ФЕДОРЕНКО Борис Николаевич
доктор технических наук, профессор Московского государственного университета пищевых производств
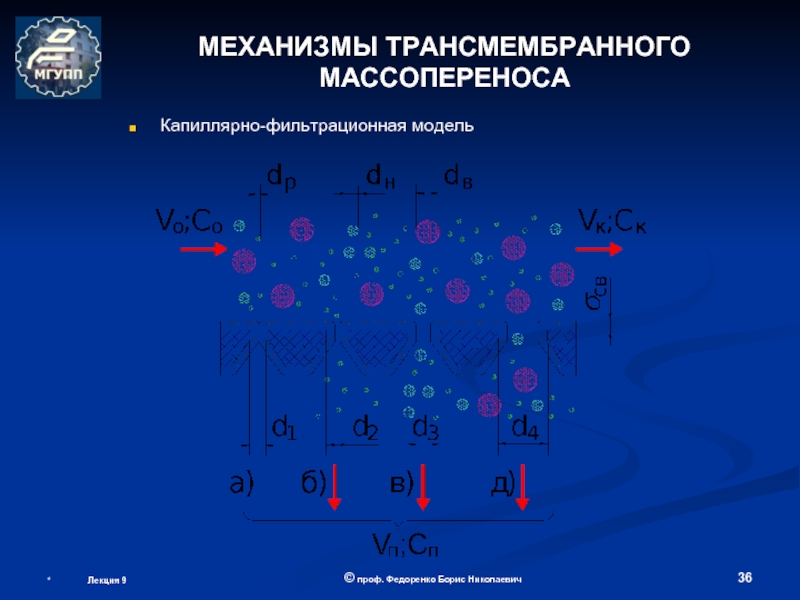
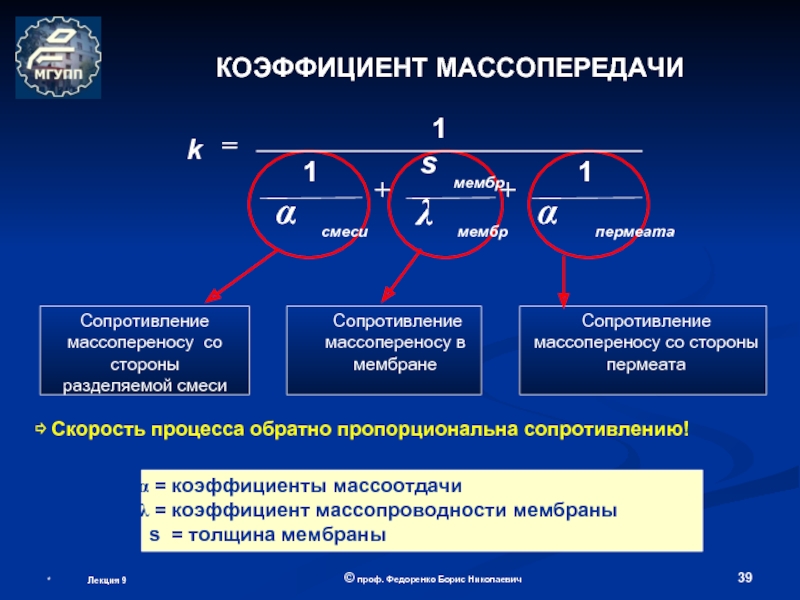
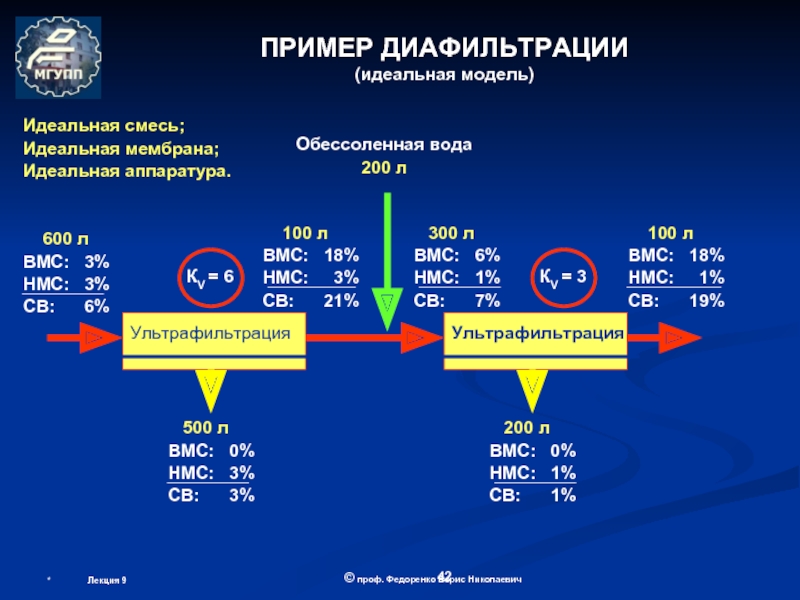
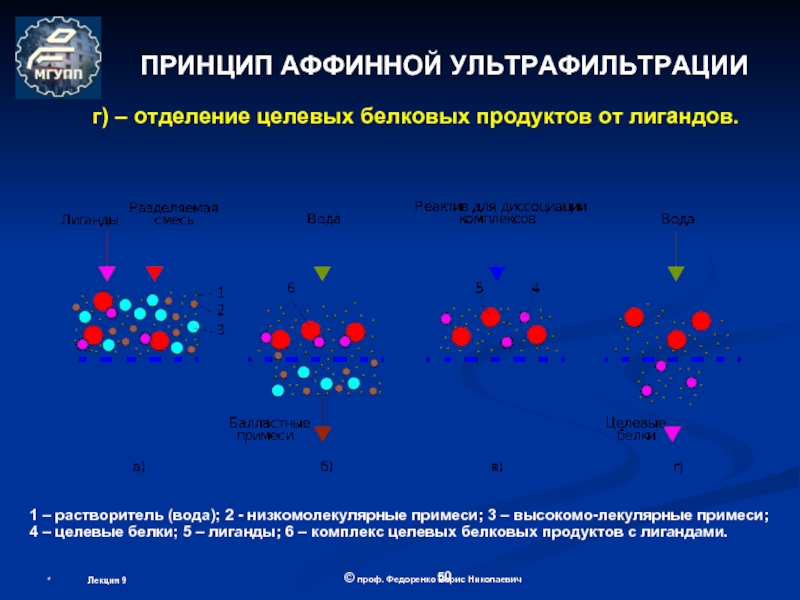
Лекция 6.
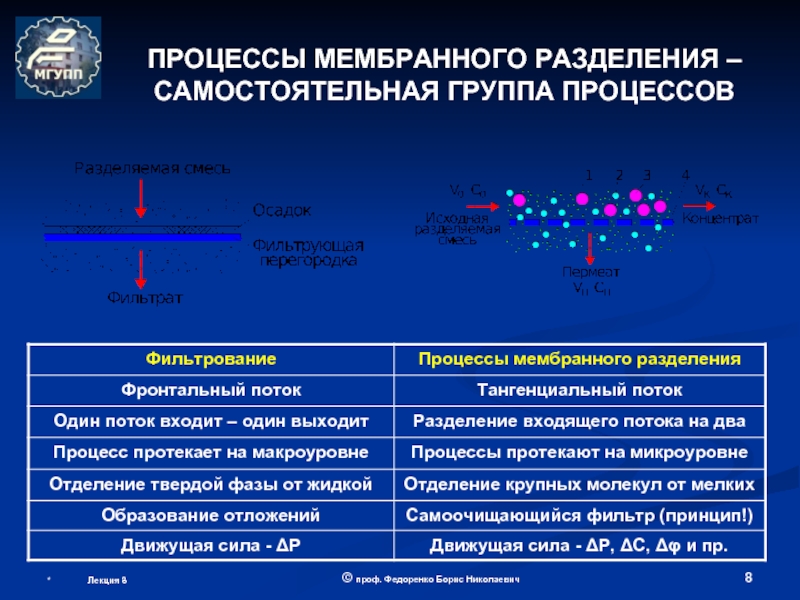
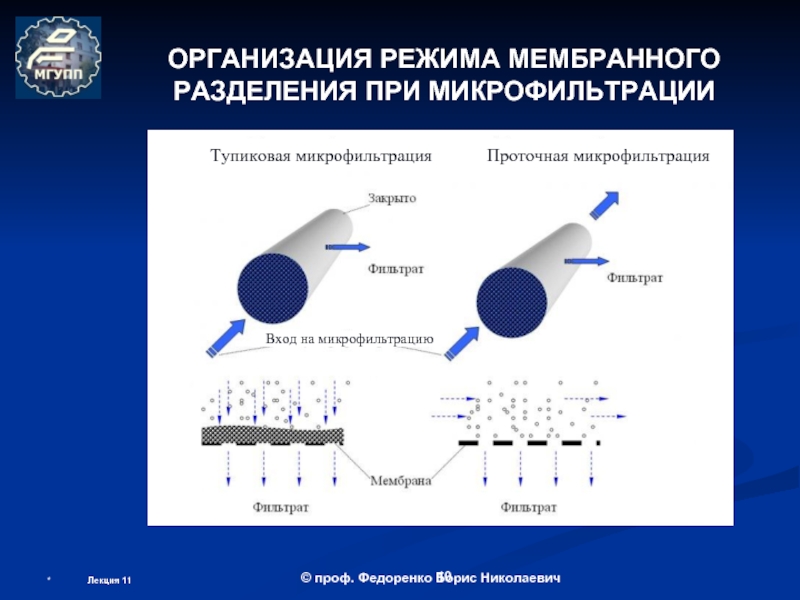
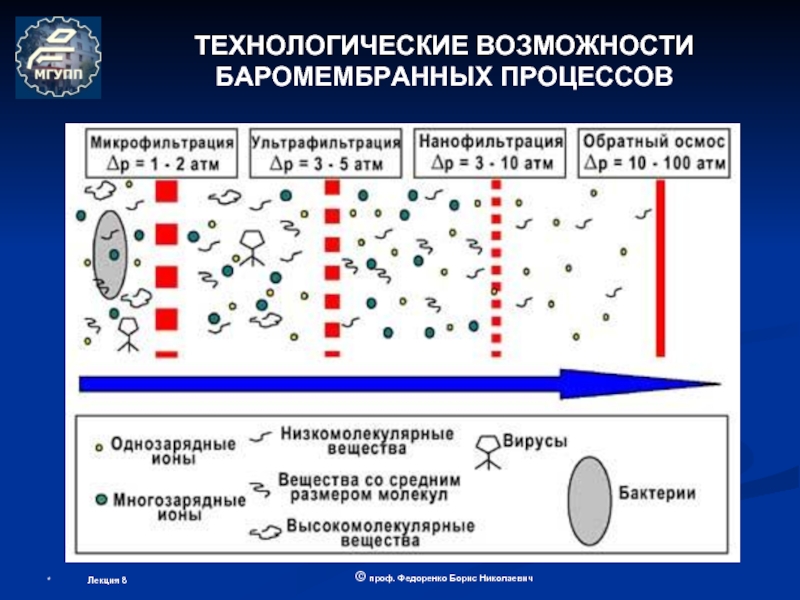
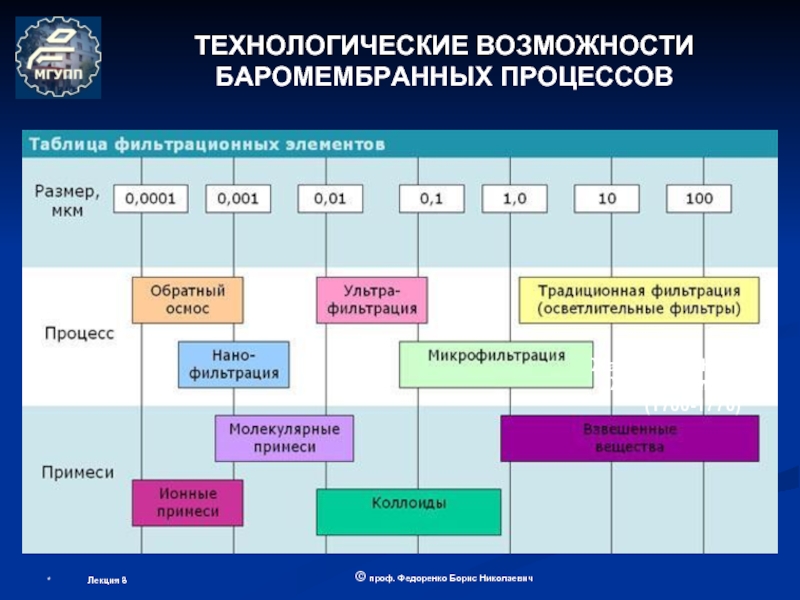
ОБОРУДОВАНИЕ МЕМБРАННОЙ БИОТЕХНОЛОГИИ
(теоретические основы мембранных процессов)
ТЕХНОЛОГИЧЕСКОЕ
ОБОРУДОВАНИЕ ОТРАСЛИ
(биотехнологические производства)