- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Бионеорганическая химия. Жидкие среды организма. (Лекция 2) презентация
Содержание
- 1. Бионеорганическая химия. Жидкие среды организма. (Лекция 2)
- 2. Структура водных растворов Самойлов О.Я. Вода Структурированная,
- 3. Положительная гидратация катиона Отрицательная гидратация катиона Зона
- 4. Структура водных растворов Гидрофобная гидратация Неполярные молекулы
- 5. Структура водных растворов Белки структурируются водой! Монослои
- 6. Структура водных растворов Вода свободная структурированная деструктурировнная
- 7. Высаливание и анестезия Увеличение
- 8. Осмос Осмос – самопроизвольная диффузия молекул растворителя
- 9. Натрий-калиевый насос Внеклеточная среда С(Na+) ≈ 140
- 10. Буферные системы организма
- 11. Буферные системы организма Сопряженность буферных систем карбоангидраза
- 12. Гетерогенные системы организма Плазма крови [Ca2+] =
- 13. Гетерогенные системы организма Растворение костной ткани Sкостной
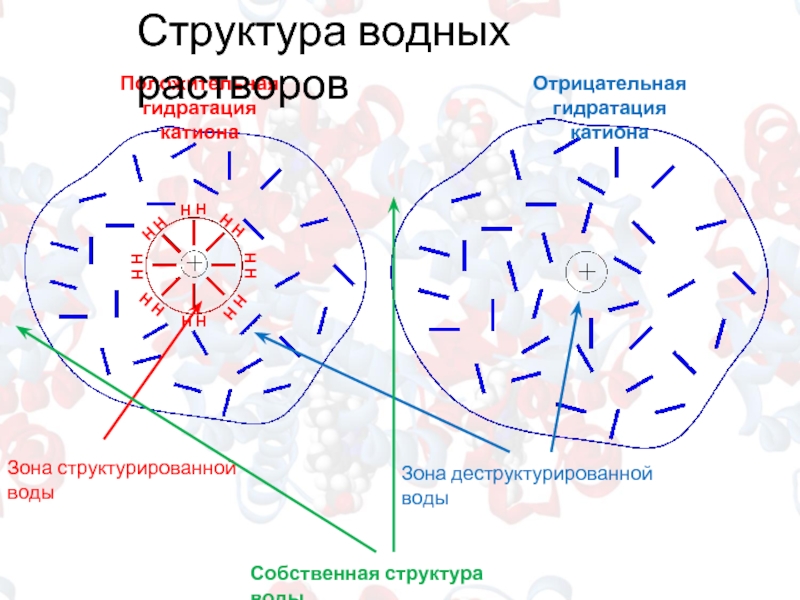
Слайд 2Структура водных растворов
Самойлов О.Я.
Вода
Структурированная,
Деструктурированная:
клатраты,
отдельные молекулы воды
≈60%
Раствор
электролита
Положительная гидратация
высокая поверхностная плотность заряда
(большой заряд, малый радиус ионов)
Na+, Mg2+, Cl-, CO32-
τ > 10-9 c
Отрицательная гидратация
Низкая поверхностная плотность заряда
(малый заряд, большой радиус ионов)
K+, NH4+, Br-, HPO42-
τ < 10-9 c
«свободная» вода
τ ≈ 10-9 c
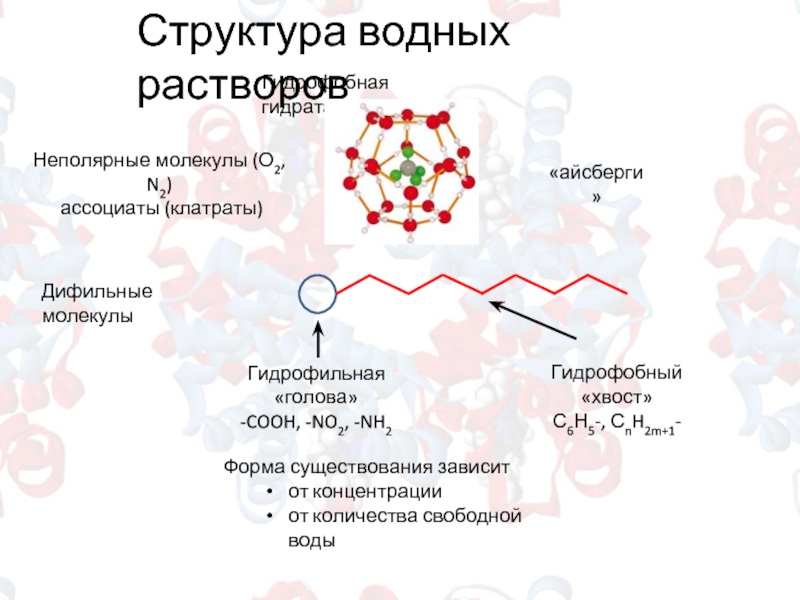
Слайд 3Положительная гидратация
катиона
Отрицательная гидратация
катиона
Зона структурированной воды
Зона деструктурированной воды
Собственная структура воды
Структура водных растворов
Слайд 4Структура водных растворов
Гидрофобная гидратация
Неполярные молекулы (О2, N2)
ассоциаты (клатраты)
«айсберги»
Дифильные молекулы
Гидрофильная «голова»
-COOH,
Гидрофобный «хвост»
С6Н5-, СnH2m+1-
Форма существования зависит
от концентрации
от количества свободной воды
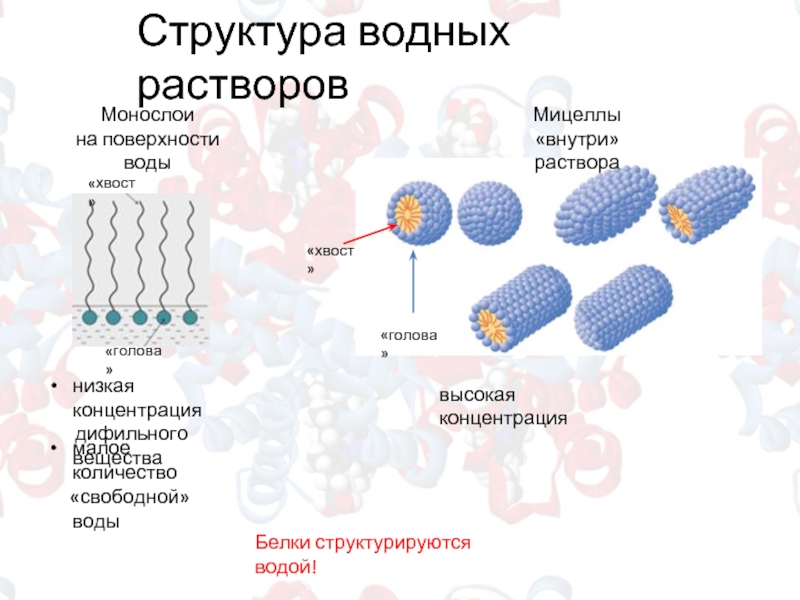
Слайд 5Структура водных растворов
Белки структурируются водой!
Монослои
на поверхности воды
Мицеллы
«внутри» раствора
низкая концентрация
малое количество
«свободной» воды
высокая концентрация
«голова»
«хвост»
«хвост»
«голова»
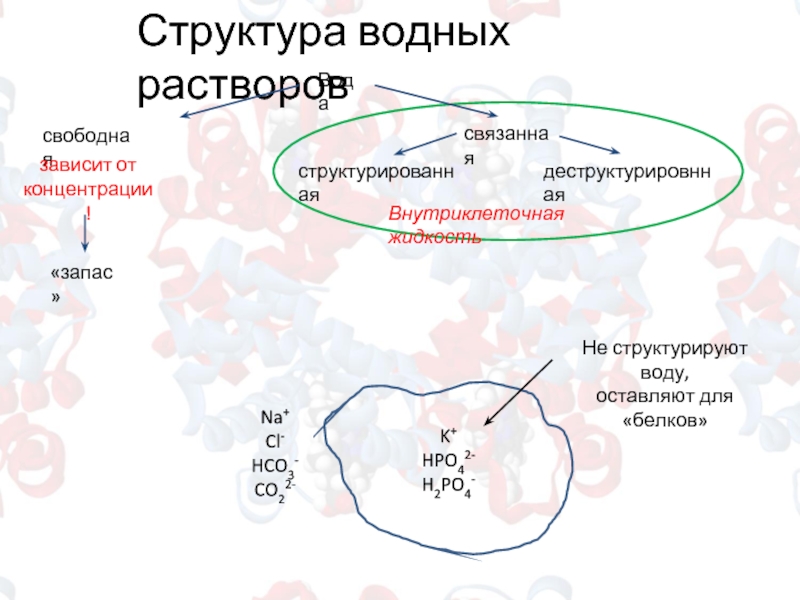
Слайд 6Структура водных растворов
Вода
свободная
структурированная
деструктурировнная
связанная
Внутриклеточная жидкость
«запас»
зависит от
концентрации!
K+
HPO42-
H2PO4-
Na+
Cl-
HCO3-
CO22-
Не структурируют воду,
оставляют для «белков»
Слайд 7
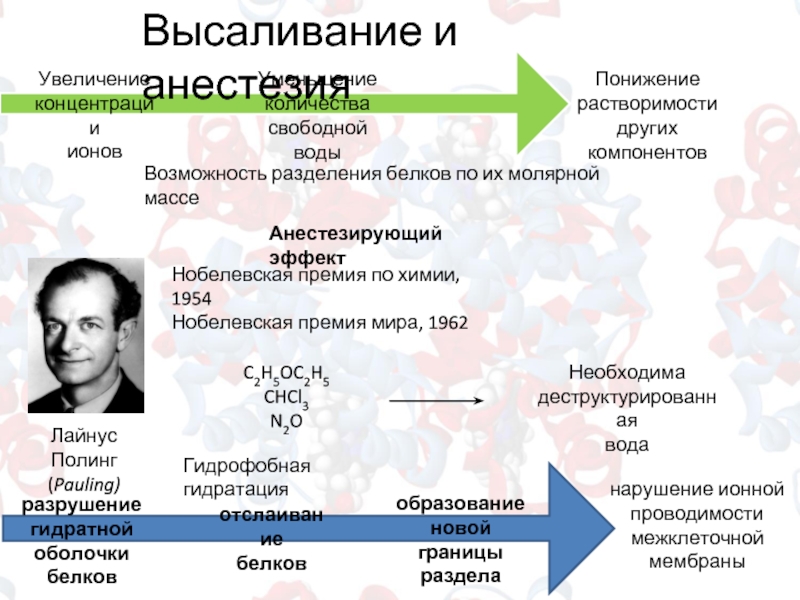
Высаливание и анестезия
Увеличение
концентрации
ионов
Уменьшение
количества
свободной воды
Понижение
растворимости
других компонентов
Возможность разделения белков
Анестезирующий эффект
Лайнус Полинг
(Pauling)
Нобелевская премия по химии, 1954
Нобелевская премия мира, 1962
C2H5OC2H5
CHCl3
N2O
Гидрофобная гидратация
Необходима
деструктурированная
вода
разрушение
гидратной
оболочки белков
отслаивание
белков
образование
новой границы
раздела
нарушение ионной
проводимости межклеточной мембраны
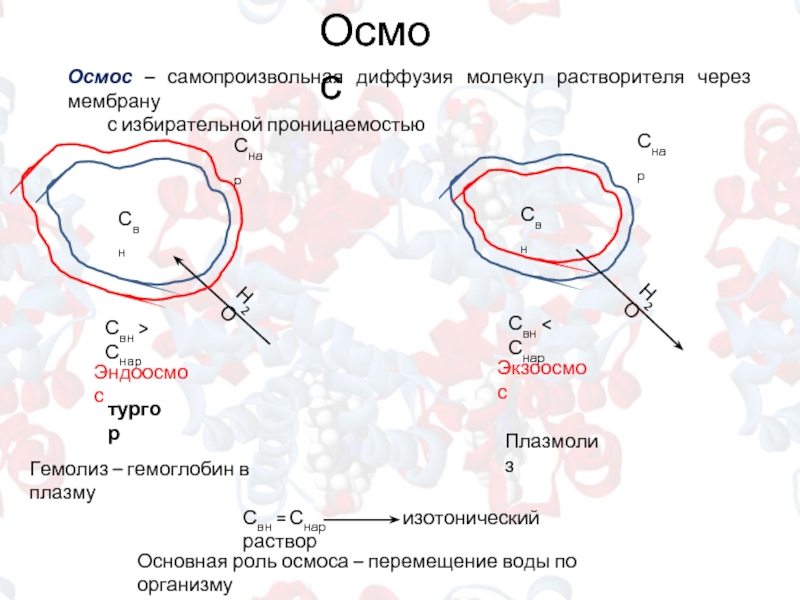
Слайд 8Осмос
Осмос – самопроизвольная диффузия молекул растворителя через мембрану
с избирательной проницаемостью
Свн
Снар
Свн
Н2О
Эндоосмос
Свн
Снар
Свн < Снар
Н2О
Экзоосмос
тургор
Гемолиз – гемоглобин в плазму
Плазмолиз
Свн = Снар изотонический раствор
Основная роль осмоса – перемещение воды по организму
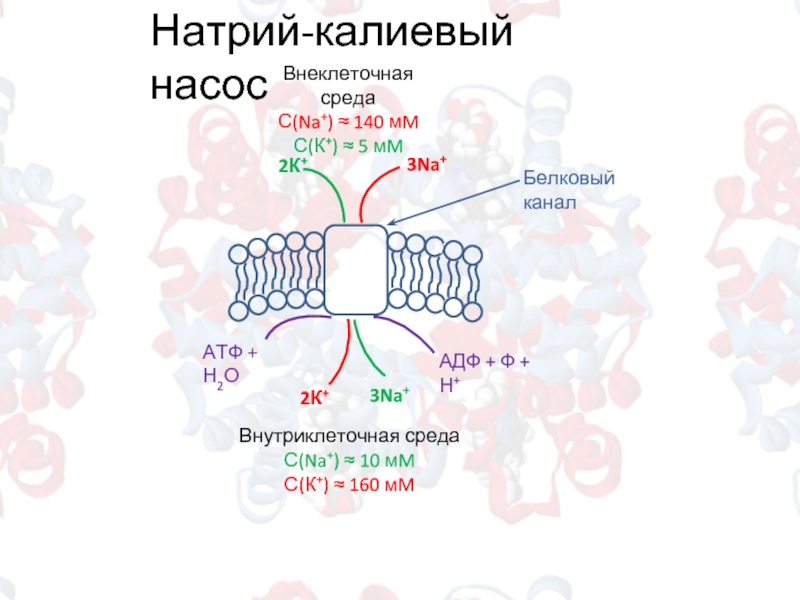
Слайд 9Натрий-калиевый насос
Внеклеточная среда
С(Na+) ≈ 140 мM
С(К+) ≈ 5 мM
Внутриклеточная среда
С(Na+) ≈
С(К+) ≈ 160 мM
м
м
2К+
3Na+
2К+
3Na+
АТФ + Н2О
АДФ + Ф + Н+
Белковый канал
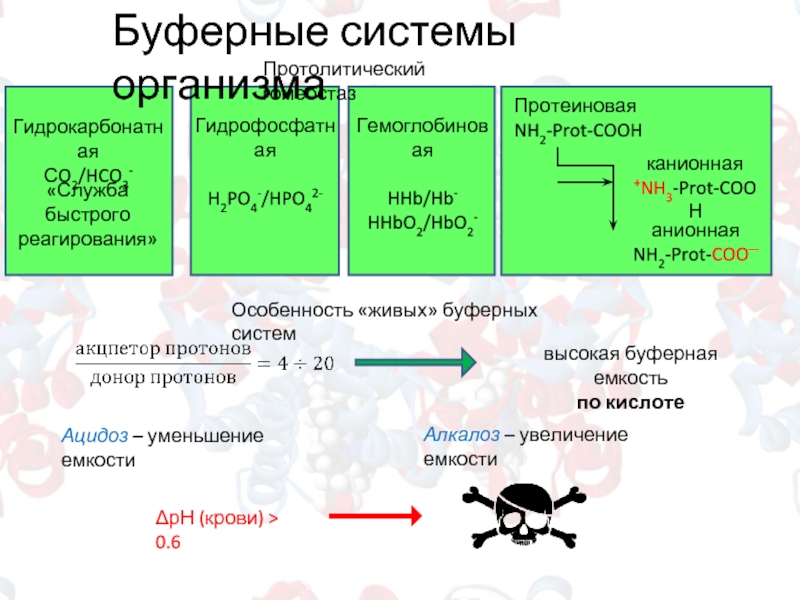
Слайд 10
Буферные системы организма
Гидрокарбонатная
СO2/HCO3-
«Служба быстрого
реагирования»
Гидрофосфатная
H2PO4-/HPO42-
Гемоглобиновая
HHb/Hb-
HHbO2/HbO2-
Протолитический гомеостаз
Протеиновая
NH2-Prot-COOH
анионная
NH2-Prot-COO─
канионная
+NH3-Prot-COOН
высокая буферная емкость
по кислоте
Особенность «живых»
Ацидоз – уменьшение емкости
Алкалоз – увеличение емкости
ΔрН (крови) > 0.6
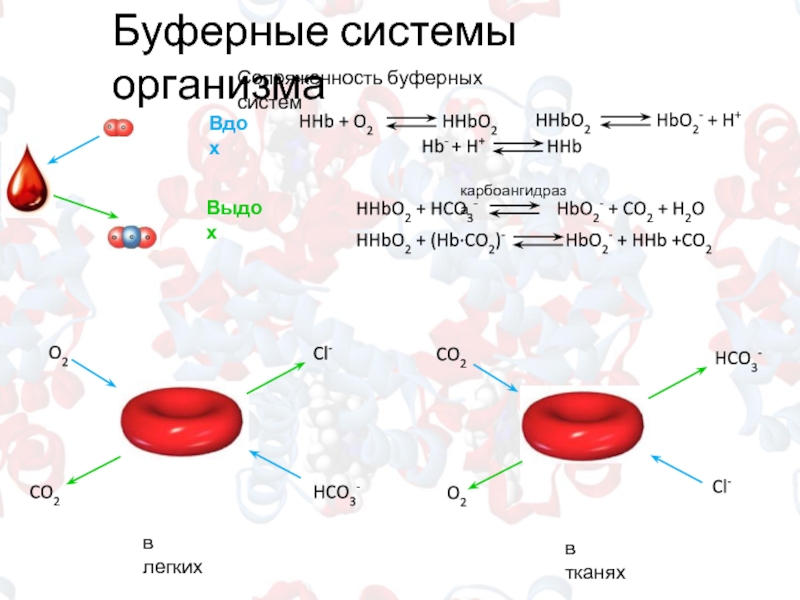
Слайд 11Буферные системы организма
Сопряженность буферных систем
карбоангидраза
Вдох
Выдох
O2
HCO3-
CO2
Cl-
CO2
Cl-
O2
HCO3-
в легких
в тканях
Слайд 12Гетерогенные системы организма
Плазма крови
[Ca2+] = 1,1∙10-3 M
[HPO42-] = 2,9∙10-4 M
ИП =
КS (CaHPO4) = 2,7∙10-7
Размер кристаллов - 10-9÷10-7 м коллоидное состояние
pH = 8,3
КS (Ca5(PO4)3OH) = 1,6∙10-58
гидроксиапатит
поверхность коллагена
Ca5(PO4)3F – зубная эмаль
Ca3(PO4)2
КS (Ca3(PO4)2) = 2∙10-29
резерв ионов кальция и фосфатов в организме
Слайд 13Гетерогенные системы организма
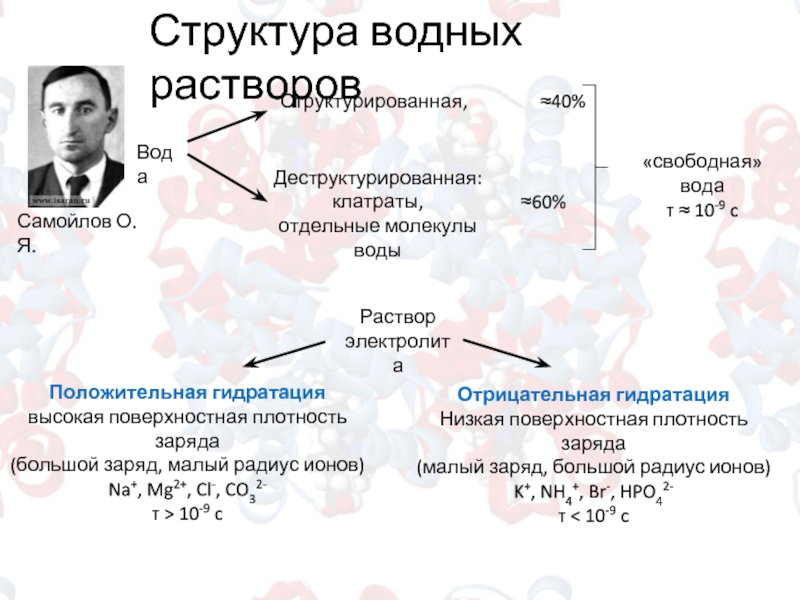
Растворение костной ткани
Sкостной ткани = 2000 км2
Костная ткань –
Образование камней
Фосфат кальция (щелочная среда)
Урат кальция (кислая среда)
Оксалат кальция

![Гетерогенные системы организмаПлазма крови[Ca2+] = 1,1∙10-3 M[HPO42-] = 2,9∙10-4 MИП = 3,2∙10-7 КS (CaHPO4) =](/img/tmb/3/215053/c7201d8ae3989a78f983f6b9dc3a7e0c-800x.jpg)