- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Бионеорганическая химия. Особенности биохимический процессов. (Лекция 1) презентация
Содержание
- 1. Бионеорганическая химия. Особенности биохимический процессов. (Лекция 1)
- 2. Неорганическая биохимия (в 2 томах) Ред. Эйхгорн
- 3. Что такое бионеорганическая химия Биохимия + неорганическая
- 4. Что такое бионеорганическая химия Задачи бионеорганической химии
- 5. Биоэнергетика Организм – открытая система
- 6. Биоэнергетика Принцип энергетического сопряжения «Источники» энергии АТФ креатинфосфат фосфоенолпируват
- 7. Биоэнергетика Химическое равновесие и стационарное состояние ΔG
- 8. Биоэнергетика │ΔGi │ ≤ 10 кДж Биохимические
- 9. Биоэнергетика Теорема Пригожина (1947) – стационарному состоянию
- 10. Ферментативный катализ Активный центр Аллостерический
- 11. Ферментативный катализ Особенности ферментативного катализа Размер. М(фермента)
- 12. Ферментативный катализ Высокая специфичность Модель индуцированной приспособляемости
- 13. Ферментативный катализ Уравнение Михаэлиса-Ментен Леонор Михаэлис (Michaelis) Мод Ментен (Menten)
- 14. Автоколебательные процессы Автокатализ – самоускорение реакции из-за
- 15. Реакция Белоусова-Жаботинского LA + Ce4+ ? ADCA
- 16. Автоколебательные процессы Биохимическая система – стационарное состояние,
Слайд 2Неорганическая биохимия (в 2 томах)
Ред. Эйхгорн Гюнтер, 1978
Основы химии живого
Слесарев В.И.,
Биометаллоорганическая химия
Ред. Жерар Жауен, 2010
Бионеорганическая химия
http://vk.com/club66508377
Вместо предисловия
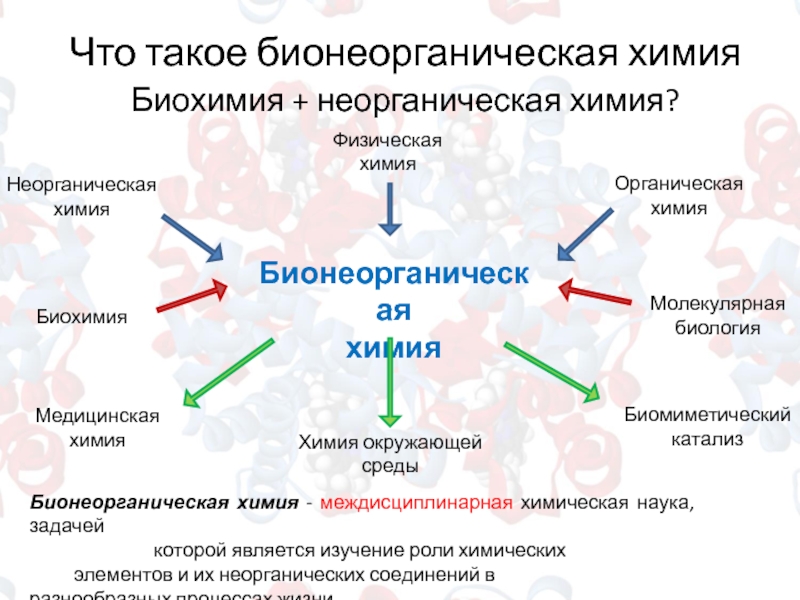
Слайд 3Что такое бионеорганическая химия
Биохимия + неорганическая химия?
Бионеорганическая
химия
Неорганическая
химия
Физическая
химия
Биохимия
Органическая
химия
Молекулярная
биология
Медицинская
химия
Биомиметический катализ
Химия
Бионеорганическая химия - междисциплинарная химическая наука, задачей
которой является изучение роли химических элементов и их неорганических соединений в разнообразных процессах жизни.
Слайд 4Что такое бионеорганическая химия
Задачи бионеорганической химии
Изучение роли металлов и их соединений
и окружающей среде
Изучение реакционной способности ионов металлов и их соединений
по отношению к биологическим субстратам
Моделирование металл-содержащих ферментов (металлопротеинов)
и процессов с их участием
Направленный синтез биологически активных соединений металлов
Создание фармакологических препаратов и биоматериалов
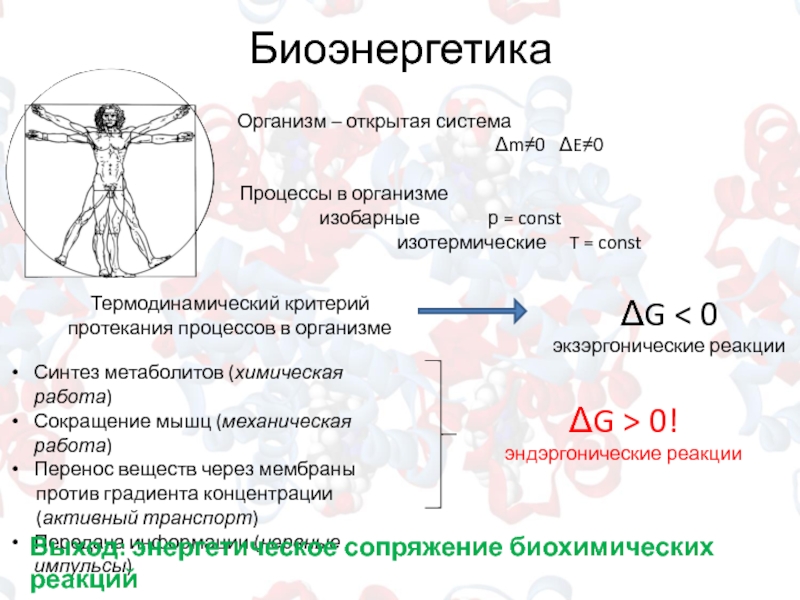
Слайд 5Биоэнергетика
Организм – открытая система
Процессы в организме
изобарные р = const
изотермические T = const
Синтез метаболитов (химическая работа)
Сокращение мышц (механическая работа)
Перенос веществ через мембраны
против градиента концентрации
(активный транспорт)
Передача информации (нервные импульсы)
ΔG > 0!
эндэргонические реакции
Выход: энергетическое сопряжение биохимических реакций
Слайд 6Биоэнергетика
Принцип энергетического сопряжения
«Источники» энергии
АТФ
креатинфосфат
фосфоенолпируват
Слайд 7Биоэнергетика
Химическое равновесие и стационарное состояние
ΔG = 0
Химическое равновесие
Процессы не протекают
Джозайя Гиббс
(Gibbs)
«Transactions
Якоб Вант-Гофф
(van't Hoff)
Нобелевская премия по химии, 1901
Изотерма Вант-Гоффа
Слайд 8Биоэнергетика
│ΔGi │ ≤ 10 кДж
Биохимические процессы – обратимы!
Стационарное состояние – v
постоянство термодинамических величин,
но их значения неравновесны
Сопряженные процессы
Слайд 9Биоэнергетика
Теорема Пригожина (1947) – стационарному состоянию системы в условиях,
Нобелевская премия по химии, 1977
Гомеостаз – относительное динамическое постоянство состава и свойств внутренней среды организма, обуславливающее устойчивость его физиологических функций
Пригожин И. Р.
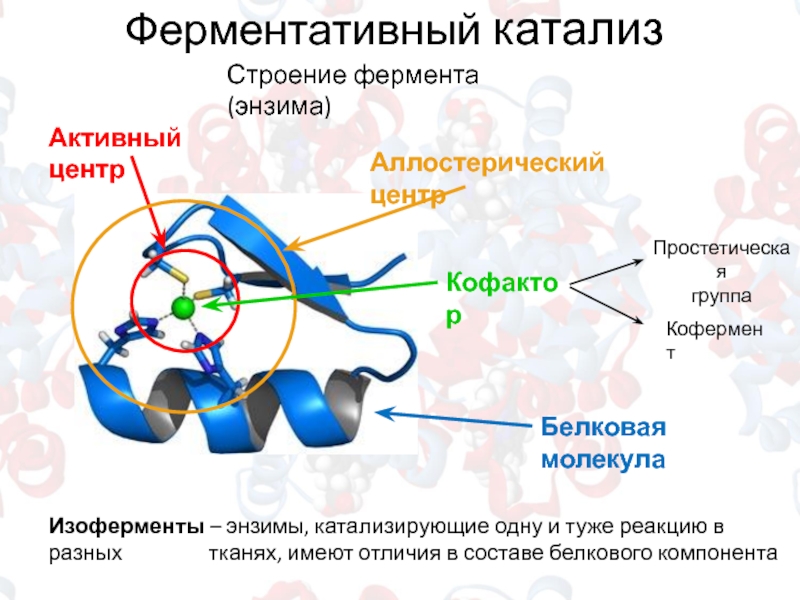
Слайд 10Ферментативный катализ
Активный центр
Аллостерический центр
Кофактор
Простетическая
группа
Кофермент
Строение фермента (энзима)
Белковая молекула
Изоферменты – энзимы, катализирующие
Слайд 11Ферментативный катализ
Особенности ферментативного катализа
Размер. М(фермента) = 105÷107 г/моль → коллоидные системы,
Высокая каталитическая эффективность. Скорость процессов возрастает в ~1010
Строго определенные условия: pH (изменение конформации, ионизация отдельных групп)
T (изменение конформации, вязкости)
Активаторы ферментов – Mg2+, Zn2+, K+
Ингибиторы ферментов – Pb2+, Cd2+, As3+, белки
Слайд 12Ферментативный катализ
Высокая специфичность
Модель индуцированной приспособляемости
Эмиль Фишер
(Fischer), 1890
Даниел Кошланд
(Koshland), 1958
химотрипсин
Модель «ключ-
Слайд 13Ферментативный катализ
Уравнение Михаэлиса-Ментен
Леонор Михаэлис
(Michaelis)
Мод Ментен
(Menten)
Слайд 14Автоколебательные процессы
Автокатализ – самоускорение реакции из-за каталитического действия промежуточного
Всегда есть автоингибирование!
Б.П. Белоусов
А.М. Жаботинский
Реакция Белоусова-Жаботинского
автокатализ
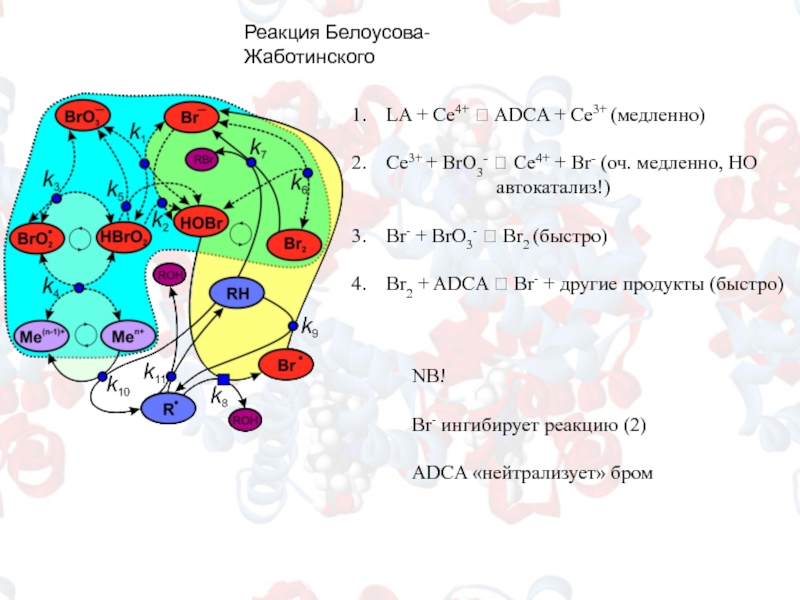
Слайд 15Реакция Белоусова-Жаботинского
LA + Ce4+ ? ADCA + Ce3+ (медленно)
Сe3+ + BrO3-
Br- + BrO3- ? Br2 (быстро)
Br2 + ADCA ? Br- + другие продукты (быстро)
NB!
Br- ингибирует реакцию (2)
ADCA «нейтрализует» бром
Слайд 16Автоколебательные процессы
Биохимическая система – стационарное состояние, [S]=const
I стадия: S →
автокатализ
Большинство биохимических процессов - сопряженные











![Автоколебательные процессыБиохимическая система – стационарное состояние, [S]=constI стадия: S → X II стадия: X + Y](/img/tmb/5/490130/32fe8122604e15714052f2ea5d526f6d-800x.jpg)





