(n–1)d 1→10.
- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Биогенные d-элементы презентация
Содержание
- 1. Биогенные d-элементы
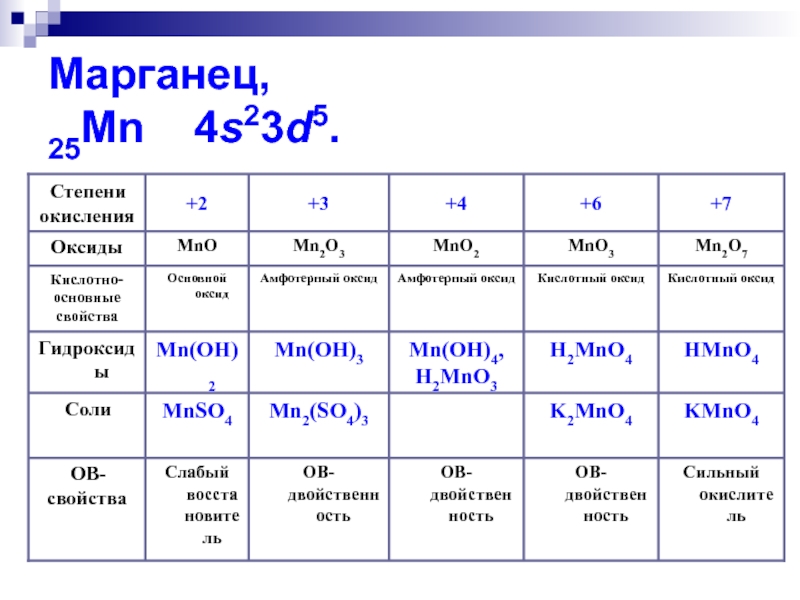
- 2. Марганец, 25Mn 4s23d5.
- 3. Основные и восстановительные свойства Mn2+ MnO+H2SO4+5H2O=[Mn(H2O)6]SO4
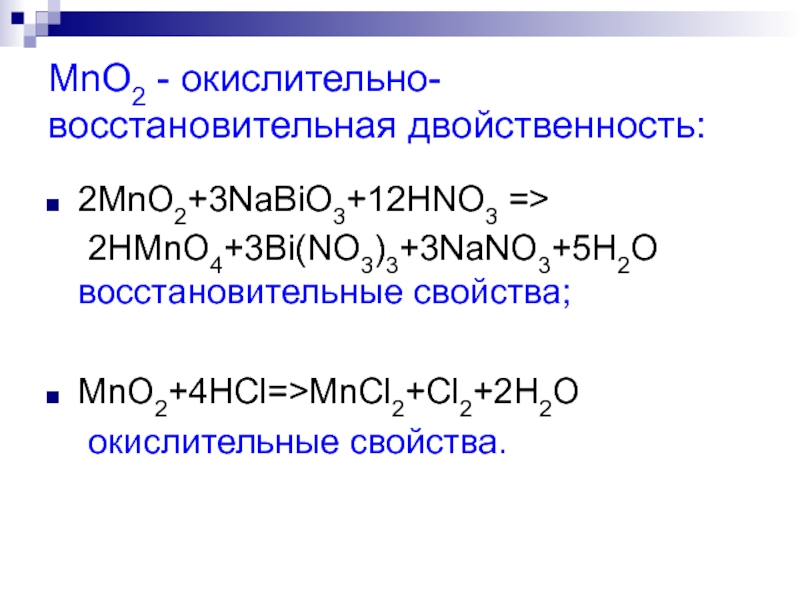
- 4. MnO2 - окислительно-восстановительная двойственность: 2MnO2+3NaВiO3+12HNO3 => 2HMnO4+3Вi(NO3)3+3NaNO3+5H2O восстановительные свойства; MnO2+4HCl=>MnCl2+Cl2+2H2O окислительные свойства.
- 5. KМnO4 - сильный окислитель при отравлениях
- 6. Зависимость ОВР от pH: в кислой среде
- 7. Mn in vivo В организме человека содержится
- 8. Биороль В составе фермента аргиназы марганец участвует
- 9. АРГ Mn2+
- 10. Биороль В составе фосфоглюкомутазы участвует в углеводном
- 11. Установлено влияние марганца на образование гемоглобина.
- 12. Избыток и недостаток: Суточная потребность 5-7мг. Марганец
- 13. Лекарственные препараты: MnCl2, MnSO4 в сочетании с
- 14. Железо 26Fe 4s23d6 с.о. +2
- 15. Химические превращения (Fe2+) Fe+2HCl=FeCl2+H2↑; FeCl2+2NaOH=Fe(OH)2↓+2NaCl;
- 16. Химические превращения (Fe3+) Fe(OH)3 проявляет амфотерные свойства,
- 17. Соли Fe3+ легко гидролизуются с образованием малорастворимых
- 18. Fe in vivo Содержание железа в организме
- 19. Биороль Транспортные биокомплексы: а) гемоглобин (Hb)
- 20. б) миоглобин (Mb) осуществляет обратимый перенос кислорода
- 21. в) трансферрин – железосодержащий белок, легко проходит
- 23. Ферментативные комплексы железа:
- 24. б) каталаза, активный центр которой содержит Fe+3,
- 25. Избыток и недостаток Суточная потребность железа составляет
- 26. При недостатке железа в организме (или большой
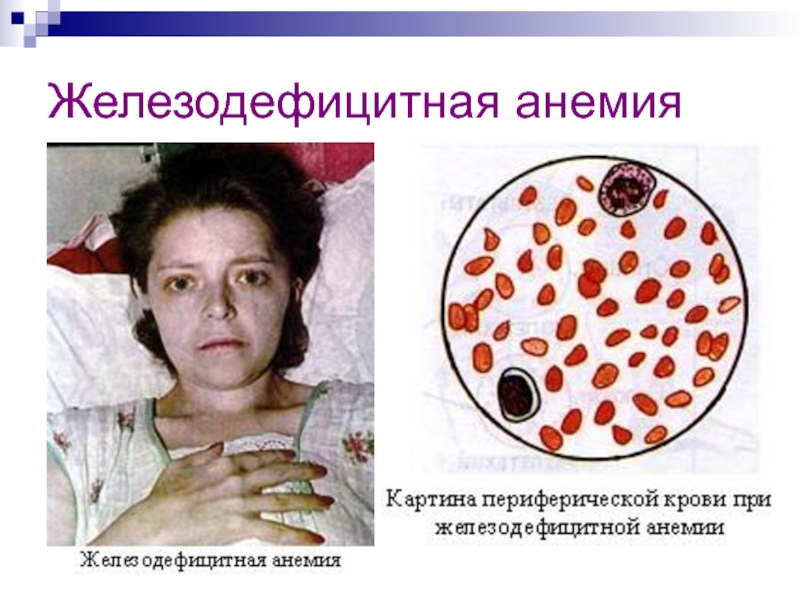
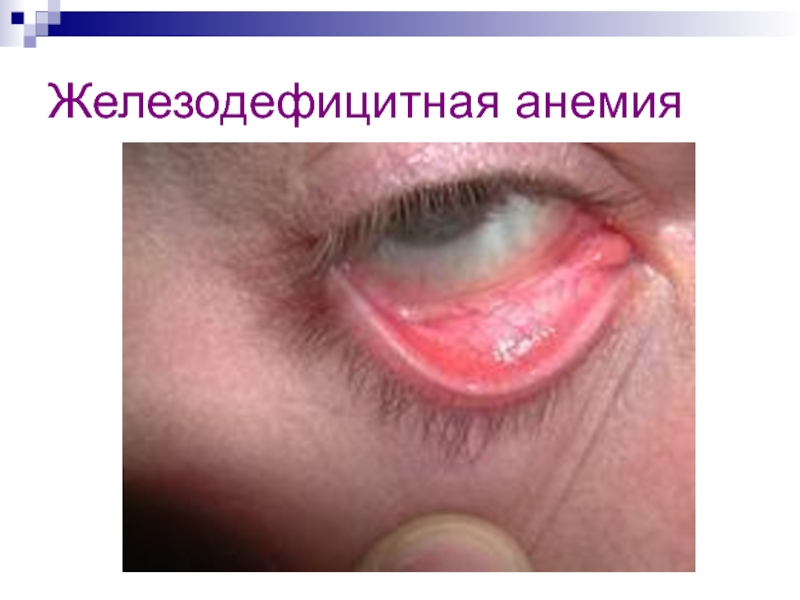
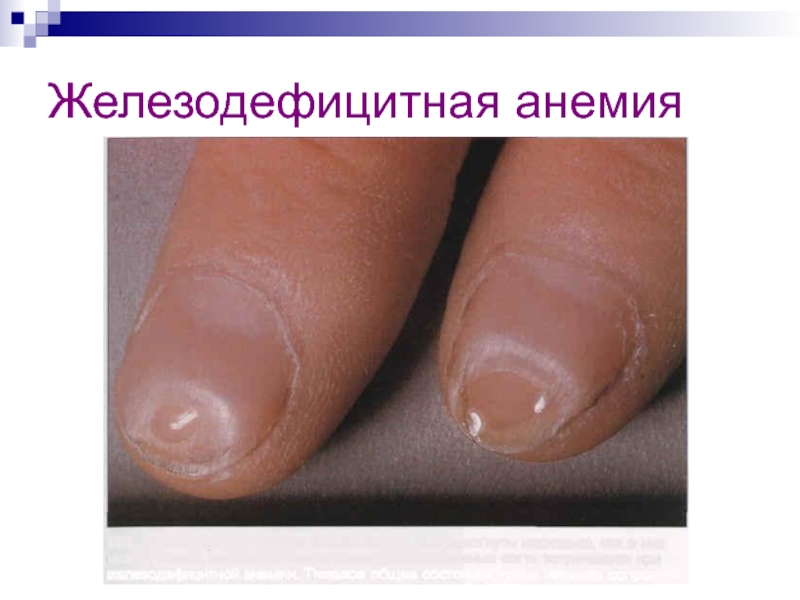
- 27. Железодефицитная анемия
- 28. Железодефицитная анемия
- 29. Железодефицитная анемия
- 30. Лекарственные препараты: FeCl2, FeSO4 ·7H2O,
- 31. FeCl3 (слабый окислитель) – применяют наружно как дезинфицирующее и кровоостанавливающее средство
- 32. Кобальт 27Co 4s2 3d7
- 33. Co in vivo Содержание в организме 1,2мг
- 34. Биороль Биороль кобальта связана с витамином В12,
- 35. Осуществляет перенос Н+, кобальт при этом восстанавливается:
- 36. Избыток и недостаток Суточная потребность составляет 0,3
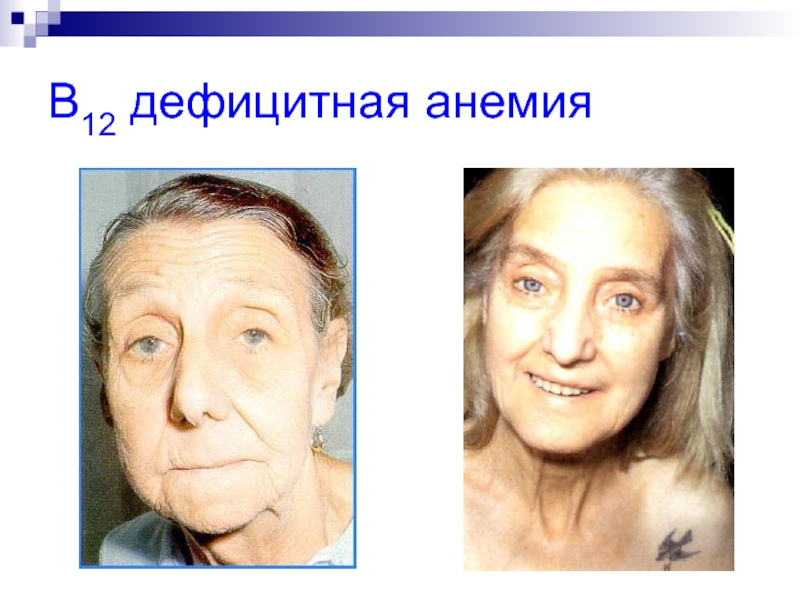
- 37. B12 дефицитная анемия
- 38. Лекарственные препараты: Витамин В12 – для лечения
- 39. Медь Электронная формула: 29Сu
- 40. Химические свойства 2Сu+O2=2CuO CuO+Cu=Cu2O Cu2O+2HCl=2CuCl↓ CuCl+2NH3=[Cu(NH3)2]Cl
- 41. CuO+H2SO4=CuSO4+H2O CuSO4+2NaOH=Cu(OH)2↓+2NaCl.
- 42. Химические свойства Cu(OH)2 обладает амфотерными свойствами, т.е.
- 43. Все соединения Cu ядовиты, даже сама металлическая
- 44. Cu in vivo В организме взрослого человека
- 45. Биороль В биохимических процессах медь участвует в
- 46. Медьсодержащие ферменты оксигеназы [ОКГ Сu+] активируют молекулу
- 47. Биороль Фермент супероксиддисмутаза
- 48. Фермент цитохромоксидаза [Fe2+ЦХОСu+], катализирует перенос электронов на
- 49. Биороль Медьсодержащий белок плазмы крови церулоплазмин [ЦП]:
- 50. б)восстановленная форма церулоплазмина [ЦПСu+] катализирует восстановление кислорода
- 51. в)осуществляет транспорт меди в органы, регулирует баланс
- 52. Избыток и недостаток Суточная потребность 4-5 мг.
- 53. Дефицит меди может привести к
- 54. Избыток меди возможен при нарушении
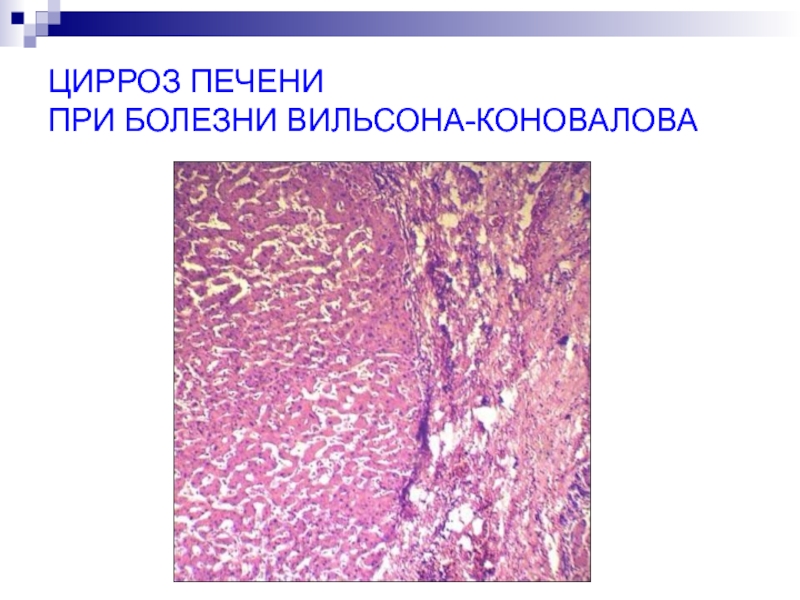
- 55. ЦИРРОЗ ПЕЧЕНИ ПРИ БОЛЕЗНИ ВИЛЬСОНА-КОНОВАЛОВА
- 56. Лекарственные препараты: CuSO4 - наружно как антисептик,
- 57. Цинк Электронная формула:
- 58. Химические свойства: 2Zn+O2=2ZnO ZnO+H2SO4=ZnSO4+H2O Качественная
- 59. Амфотерность Zn(OH)2 Zn(OH)2 является амфотерным
- 60. Zn in vivo В организме взрослого человека
- 61. Биороль Цинк входит в состав более
- 62. б) карбоксипептидаза КОПZn2+ участвует в гидролизе пептидной
- 63. Биороль Известное влияние цинк оказывает на углеводный
- 64. Участвует в формировании спиральной структуры РНК.
- 65. Избыток и недостаток Суточная потребность цинка около
- 66. Лекарственные препараты: ZnCl2 – вяжущее, прижигающее и
- 67. Токсическое действие Cd, Hg: Наиболее токсична метилртуть
- 68. Метилртуть накапливается в рыбе, а затем с
- 69. Постепенно концентрируясь, она вызывает необратимые разрушения в
- 70. Болезнь Минамата
- 71. Механизм токсического действия ртути и кадмия:
- 72. 2. У кадмия и особенно ртути ярко
- 73. Лекарственные препараты: HgСl2 – в концентрации 1
- 74. Спасибо за внимание!!!
Слайд 1БИОГЕННЫЕ
d-ЭЛЕМЕНТЫ
У атомов d-элементов заполняется электронами d-подуровень предвнешнего уровня: ns(1→2)
Слайд 3Основные и восстановительные свойства Mn2+
MnO+H2SO4+5H2O=[Mn(H2O)6]SO4
MnSO4+2NaOH=Mn(OH)2↓+Na2SO4
Mn(OH)2+O2+H2O→Mn(OH)4→MnO2↓+H2O
Качественная реакция на Mn2+ :
2Mn(NO3)2+5NaВiO3+16HNO3=
2HMnO4+5Вi(NO3)3+5NaNO3+7H2O
фиолетовое
окрашивание
Слайд 4MnO2 - окислительно-восстановительная двойственность:
2MnO2+3NaВiO3+12HNO3 =>
2HMnO4+3Вi(NO3)3+3NaNO3+5H2O восстановительные свойства;
MnO2+4HCl=>MnCl2+Cl2+2H2O
окислительные свойства.
Слайд 5KМnO4 - сильный окислитель
при отравлениях обезвреживание идет за счет окислительно-восстановительной
реакции:
2KMnO4+5H2O2+6CH3COOH =>
2Mn(CH3COO)2+2CH3COOK+5O2+8H2O
2KMnO4+5H2O2+6CH3COOH =>
2Mn(CH3COO)2+2CH3COOK+5O2+8H2O
Слайд 6Зависимость ОВР от pH:
в кислой среде ϕ0MnO4-/Mn2+ = 1,52В
2KMnO4+5K2SO3+3H2SO4=2MnSO4+6K2SO4+3H2O
в
нейтральной среде ϕ0MnO4-/MnO2 = 0,6В
2KMnO4+3K2SO3+H2O=2MnO2+3K2SO4+2KOH
в щелочной среде ϕ0MnO4-/MnO42- = 0,56В
2KMnO4+K2SO3+2KOH=2K2MnO4+K2SO4+H2O
2KMnO4+3K2SO3+H2O=2MnO2+3K2SO4+2KOH
в щелочной среде ϕ0MnO4-/MnO42- = 0,56В
2KMnO4+K2SO3+2KOH=2K2MnO4+K2SO4+H2O
Слайд 7Mn in vivo
В организме человека содержится около 12мг марганца, ω(Mn) =
10-5 %, микроэлемент.
Топография: кости (43%), мышцы, печень, ногти, поджелудочная железа, мозг, лёгкие, селезёнка.
Топография: кости (43%), мышцы, печень, ногти, поджелудочная железа, мозг, лёгкие, селезёнка.
Слайд 8Биороль
В составе фермента аргиназы марганец участвует в цикле мочевинообразования. На последнем
этапе синтеза мочевины аргиназа катализирует расщепление аргинина на мочевину и орнитин.
Слайд 10Биороль
В составе фосфоглюкомутазы участвует в углеводном обмене.
фосфоглюкомутаза
Глюкоза – 1 – фосфат Глюкоза – 6 – фосфат
В составе фермента холинэстеразы участвует в процессе свертывания крови.
Ионы Mn+2 стабилизируют конформацию нуклеиновых кислот, подобно Mg+2 , образуют соединительные мостики.
Участвует в синтезе витаминов В и С.
Глюкоза – 1 – фосфат Глюкоза – 6 – фосфат
В составе фермента холинэстеразы участвует в процессе свертывания крови.
Ионы Mn+2 стабилизируют конформацию нуклеиновых кислот, подобно Mg+2 , образуют соединительные мостики.
Участвует в синтезе витаминов В и С.
Слайд 11Установлено влияние марганца на образование гемоглобина.
Mn+2, подобно Mg+2, в составе активных
форм АТФ и АДФ участвует в аккумуляции и переносе энергии в организме.
[АТФ Мn]2– +H2O→ [АДФ Мn]– +H2PO4-+ ∆H
Марганец способствует усвоению фосфора и кальция и влияет на образование костей, минеральный обмен, рост, размножение.
[АТФ Мn]2– +H2O→ [АДФ Мn]– +H2PO4-+ ∆H
Марганец способствует усвоению фосфора и кальция и влияет на образование костей, минеральный обмен, рост, размножение.
Слайд 12Избыток и недостаток:
Суточная потребность 5-7мг. Марганец содержится в печени, красной свекле,
томатах, моркови, сое, горохе, картофеле.
Дефицит марганца вызывает снижение тонуса, замедление роста, нарушение в структуре нуклеиновых кислот.
Избыток марганца приводит к марганцевому рахиту из-за вытеснения кальция из костей.
Дефицит марганца вызывает снижение тонуса, замедление роста, нарушение в структуре нуклеиновых кислот.
Избыток марганца приводит к марганцевому рахиту из-за вытеснения кальция из костей.
Слайд 13Лекарственные препараты:
MnCl2, MnSO4 в сочетании с солями железа, меди, кобальта используют
для лечения анемии и при больших кровопотерях.
KMnO4 – наружное антисептическое средство; 0,01-5% для промывания ран; 5% как кровоостанавливающее.
KMnO4 – наружное антисептическое средство; 0,01-5% для промывания ран; 5% как кровоостанавливающее.
Слайд 15Химические превращения (Fe2+)
Fe+2HCl=FeCl2+H2↑;
FeCl2+2NaOH=Fe(OH)2↓+2NaCl;
Fe(OH)2 проявляет основные и восстановительные свойства:
Fe(OH)2+H2SO4=FeSO4+2H2O;
Fe(OH)2+O2+H2О→Fe(OH)3.
Fe(OH)2 разлагается при нагревании
с образованием соответствующего FeO:
Fe(OH)2→FeO+H2O.
Fe(OH)2→FeO+H2O.
Слайд 16Химические превращения (Fe3+)
Fe(OH)3 проявляет амфотерные свойства, т.е. реагирует и с кислотами,
и с основаниями:
Fe(OH)3+3HCl=FeCl3+3H2O;
Fe(OH)3+3NaOH=Na3[Fe(OH)6].
Fe(OH)3+3HCl=FeCl3+3H2O;
Fe(OH)3+3NaOH=Na3[Fe(OH)6].
Слайд 17Соли Fe3+ легко гидролизуются с образованием малорастворимых основных солей, поэтому для
перорального приема назначают препараты Fe2+:
FeCl3+H2O→Fe(OH)Cl2↓+HCl;
FeCl3+H2O→Fe(OH)Cl2↓+HCl;
Слайд 18Fe in vivo
Содержание железа в организме около 5г, ω(Fe) ≈ 10-2
%, микроэлемент.
Топография: большая часть железа сосредоточена в гемоглобине (~70%), в печени (~5%), селезёнке, костном мозге, почках, плазме крови.
Топография: большая часть железа сосредоточена в гемоглобине (~70%), в печени (~5%), селезёнке, костном мозге, почках, плазме крови.
Слайд 19Биороль
Транспортные биокомплексы:
а) гемоглобин (Hb) обратимо связывает кислород и переносит его от
лёгких к тканям:
[HbFe+2] + O2 [HbFe+2O2];
дезоксигемоглобин оксигемоглобин
[HbFe+2] + O2 [HbFe+2O2];
дезоксигемоглобин оксигемоглобин
Слайд 20б) миоглобин (Mb) осуществляет обратимый перенос кислорода в мышцах:
[MbFe+2] +
O2 [MbFe+2O2];
дезоксиформа оксиформа
дезоксиформа оксиформа
Слайд 21в) трансферрин – железосодержащий белок, легко проходит через клеточную мембрану и
доставляет Fe+3 от ферритина в костный мозг для синтеза гемоглобина.
Слайд 22
Ферритин – является аккумуляторным биокластером,
в его полости депонируется Fe+3, которое организм использует по мере необходимости.
Слайд 23 Ферментативные комплексы железа:
а) цитохромы(ЦХ) катализируют перенос электронов
в дыхательной цепи за счёт изменения степени окисления железа:
[ЦХ ∙ Fe+3] + ē [ЦХ ∙ Fe+2]
[ЦХ ∙ Fe+3] + ē [ЦХ ∙ Fe+2]
Слайд 24б) каталаза, активный центр которой содержит Fe+3, ускоряет процесс разложения токсичного
пероксида водорода:
каталаза
2Н2О2 2Н2О + О2
каталаза
2Н2О2 2Н2О + О2
Слайд 25Избыток и недостаток
Суточная потребность железа составляет 1мг, но из пищи усваивается
только 10-20%, поэтому должно поступать 10мг (мужчины), 20мг (женщины).
Железо содержится в печени, рыбе, изюме, гранатах, лесной землянике.
Железо содержится в печени, рыбе, изюме, гранатах, лесной землянике.
Слайд 26При недостатке железа в организме (или большой его потере) развивается железодефицитная
анемия (малокровие).
У беременных женщин невынашиваемость, недоразвитость плода, патологические роды. У детей- нарушение психики, отсутствие внимания, повышение заболеваемости.
У беременных женщин невынашиваемость, недоразвитость плода, патологические роды. У детей- нарушение психики, отсутствие внимания, повышение заболеваемости.
Слайд 30Лекарственные препараты:
FeCl2, FeSO4 ·7H2O,
“феррамид” (комплекс Fe
с никотиновой кислотой),
аскорбинат железа (II),
лактат железа (II),
“ферроплекс” (FeSO4 с аскорбиновой кислотой),
глицерофосфат железа (III)
применяются для лечения анемии.
аскорбинат железа (II),
лактат железа (II),
“ферроплекс” (FeSO4 с аскорбиновой кислотой),
глицерофосфат железа (III)
применяются для лечения анемии.
Слайд 31 FeCl3 (слабый окислитель) – применяют наружно как дезинфицирующее и
кровоостанавливающее средство
Слайд 33Co in vivo
Содержание в организме 1,2мг кобальта, микроэлемент.
Топография: мышцы (43%), кости
(14%), печень.
Слайд 34Биороль
Биороль кобальта связана с витамином В12, который является порфириновым комплексом Со+³
и в организме выполняет две основные функции:
В реакциях метилирования переносит СН3 – группы (синтез холина, лецитина, тимина, метионина, ДНК)
В реакциях метилирования переносит СН3 – группы (синтез холина, лецитина, тимина, метионина, ДНК)
Слайд 35Осуществляет перенос Н+, кобальт при этом восстанавливается:
+ē
HR · Со+3 R· Со+2+ H+
Кобальт в составе витамина В12, выполняя указанные функции, влияет на минеральный, углеводный, белковый и жировой обмен, а также участвует в кроветворении (синергизм с железом).
HR · Со+3 R· Со+2+ H+
Кобальт в составе витамина В12, выполняя указанные функции, влияет на минеральный, углеводный, белковый и жировой обмен, а также участвует в кроветворении (синергизм с железом).
-ē
Слайд 36Избыток и недостаток
Суточная потребность составляет 0,3 мг кобальта. Витамин В12 содержится
в мясе, печени, почках, рыбе, молоке, яйце.
Недостаток витамина В12 в организме вызывает злокачественную анемию.
Недостаток витамина В12 в организме вызывает злокачественную анемию.
Слайд 38Лекарственные препараты:
Витамин В12 – для лечения анемии, нервных заболеваний
Коамид (комплекс кобальта
с никотиновой кислотой) – для лечения анемии
Изотоп радиоактивного кобальта 60Со –
для лечения злокачественных опухолей.
Изотоп радиоактивного кобальта 60Со –
для лечения злокачественных опухолей.
Слайд 42Химические свойства
Cu(OH)2 обладает амфотерными свойствами, т.е. реагирует и с кислотами, и
с основаниями, образует комплексные соединения с координационным числом 4.
Cu(OH)2+2HCl=CuCl2+2H2O
Cu(OH)2+2NaOH = Na2[Cu(OH)4]
Cu(OH)2+4NH3 = [Cu(NH3)4](OH)2.
Cu(OH)2+2HCl=CuCl2+2H2O
Cu(OH)2+2NaOH = Na2[Cu(OH)4]
Cu(OH)2+4NH3 = [Cu(NH3)4](OH)2.
Слайд 43Все соединения Cu ядовиты, даже сама металлическая Cu, т.к. на ее
поверхности образуется ядовитый зеленый налет гидроксокарбоната меди:
2Cu+O2+CO2+H2O = (CuOH)2CO3.
2Cu+O2+CO2+H2O = (CuOH)2CO3.
Слайд 44Cu in vivo
В организме взрослого человека содержится около 100 мг меди,
микроэлемент.
Топография: печень, головной мозг, кровь.
Топография: печень, головной мозг, кровь.
Слайд 45Биороль
В биохимических процессах медь участвует в виде комплексов Сu+ и Сu2+
с биолигандами.
Известно около 25 медьсодержащих белков и ферментов.
Известно около 25 медьсодержащих белков и ферментов.
Слайд 46Медьсодержащие ферменты оксигеназы [ОКГ Сu+] активируют молекулу кислорода в процессе окисления
органических соединений:
O
[ОКГ Сu+] + О2 → [ОКГ Сu2+ ]
O
O
[ОКГ Сu2+ ] + RCH2OH → RCOOH + [ОКГ Сu+] + H2O
O
O
[ОКГ Сu+] + О2 → [ОКГ Сu2+ ]
O
O
[ОКГ Сu2+ ] + RCH2OH → RCOOH + [ОКГ Сu+] + H2O
O
Слайд 47Биороль
Фермент супероксиддисмутаза
[СОД Сu2+] ускоряет реакцию разложения токсичного
супероксид-иона ·О2-
[СОД Сu2+] +·О2- → [СОД Сu+] + О2
[СОД Сu+] + ·О2- + 2H+ →[СОД Сu2+] + Н2О2
[СОД Сu2+] +·О2- → [СОД Сu+] + О2
[СОД Сu+] + ·О2- + 2H+ →[СОД Сu2+] + Н2О2
Слайд 48Фермент цитохромоксидаза [Fe2+ЦХОСu+], катализирует перенос электронов на кислород на конечном этапе
тканевого дыхания:
2[Fe2+ЦХОСu+] + О2 + 4H+ →2[Fe3+ЦХОСu2+] + 2H2O
2[Fe2+ЦХОСu+] + О2 + 4H+ →2[Fe3+ЦХОСu2+] + 2H2O
Слайд 49Биороль
Медьсодержащий белок плазмы крови церулоплазмин [ЦП]:
а)катализирует окисление Fe+2 в Fe+3 в
процессе кроветворения:
Fe+2 + [ЦПСu2+] → Fe+3 + [ЦПСu+]
Fe+2 + [ЦПСu2+] → Fe+3 + [ЦПСu+]
Слайд 50б)восстановленная форма церулоплазмина [ЦПСu+]
катализирует восстановление кислорода в воду:
О2+4[ЦПСu+] +4H+ →
2H2O + 4 [ЦПСu2+]
Слайд 51в)осуществляет транспорт меди в органы, регулирует баланс меди и обеспечивает выведение
её избытка из организма:
[ЦПСu2+]→[органы Сu2+]+ [ЦП]
Медь вместе с железом участвует в кроветворении, способствует синтезу гемоглобина, образованию новых эритроцитов.
[ЦПСu2+]→[органы Сu2+]+ [ЦП]
Медь вместе с железом участвует в кроветворении, способствует синтезу гемоглобина, образованию новых эритроцитов.
Слайд 52Избыток и недостаток
Суточная потребность 4-5 мг.
Медь содержится в
печени телят и ягнят, белых грибах, черной смородине, абрикосах, устрицах.
Слайд 53 Дефицит меди может привести к разрушению эритроцитов (медная анемия),
а также нарушению остеогенеза с изменениями в скелете (экзотическая атаксия) и др.
Слайд 54 Избыток меди возможен при нарушении синтеза церулоплазмина. Медь накапливается
в печени, нервных клетках, разрушая их (болезнь Вильсона-Коновалова)
Слайд 56Лекарственные препараты:
CuSO4 - наружно как антисептик, вяжущее, прижигающие
CuSO4 - в микродозах
для лечения анемии.
Cu2O и CuO - в стоматологии в составе фосфатных бактерицидных цементов как пломбировочный материал.
Cu2O и CuO - в стоматологии в составе фосфатных бактерицидных цементов как пломбировочный материал.
Слайд 58Химические свойства:
2Zn+O2=2ZnO
ZnO+H2SO4=ZnSO4+H2O
Качественная реакция на ион Zn2+ - образование белого осадка сульфида
цинка ZnS:
ZnSO4+H2S=ZnS↓+Н2SO4
ZnSO4+4NH3=[Zn(NH3)4]SO4
ZnSO4+2NaOH=Zn(OH)2↓+Na2SO4.
ZnSO4+H2S=ZnS↓+Н2SO4
ZnSO4+4NH3=[Zn(NH3)4]SO4
ZnSO4+2NaOH=Zn(OH)2↓+Na2SO4.
Слайд 59Амфотерность Zn(OH)2
Zn(OH)2 является амфотерным гидроксидом, реагирует и с кислотами,
и с основаниями:
Zn(OH)2+2HCl=ZnCl2+2H2O
Zn(OH)2+2NaOH=Na2[Zn(OH)4].
Zn(OH)2+2HCl=ZnCl2+2H2O
Zn(OH)2+2NaOH=Na2[Zn(OH)4].
Слайд 60Zn in vivo
В организме взрослого человека содержится 1,4 – 2,3 г
цинка, микроэлемент.
Топография: мышцы (65%), кости (20%), кровь (9%), печень, половые железы, поджелудочная железа, сетчатая оболочка глаз.
Топография: мышцы (65%), кости (20%), кровь (9%), печень, половые железы, поджелудочная железа, сетчатая оболочка глаз.
Слайд 61Биороль
Цинк входит в состав более
40 металлоферментов:
а) карбоангидраза в эритроцитах катализирует
обратимую гидратацию СО2, тем самым влияет на процесс дыхания и газообмена организма:
карбоангидраза
СО2 + Н2О Н2СО3 ;
карбоангидраза
СО2 + Н2О Н2СО3 ;
Слайд 62б) карбоксипептидаза КОПZn2+ участвует в гидролизе пептидной связи белков:
КОП Zn2+
R1CO-NH R2 + H2O R1COOH + R2-N H2
в) дипептидазы катализируют реакции гидролиза дипептидов.
R1CO-NH R2 + H2O R1COOH + R2-N H2
в) дипептидазы катализируют реакции гидролиза дипептидов.
Слайд 63Биороль
Известное влияние цинк оказывает на углеводный обмен, входит в состав активной
формы инсулина.
Активирует биосинтез витаминов В и С.
Стимулирует фагоцитарную активность лейкоцитов.
Активирует биосинтез витаминов В и С.
Стимулирует фагоцитарную активность лейкоцитов.
Слайд 64Участвует в формировании спиральной структуры РНК.
Цинк влияет на рост, половое развитие,
размножение, способствует делению клеток, в том числе раковых. Концентрация Zn2+ в атипичных клетках возрастает, это можно использовать для диагностики рака на ранних стадиях.
Слайд 65Избыток и недостаток
Суточная потребность цинка около 20 мг компенсируется продуктами, которые
употребляют в пищу. Наиболее богаты цинком мясо, печень, молоко, яйцо.
Дефицит цинка при недоедании или алкоголизме приводит к отставанию в росте, половом созревании, к поражению кожных покровов.
Дефицит цинка при недоедании или алкоголизме приводит к отставанию в росте, половом созревании, к поражению кожных покровов.
Слайд 66Лекарственные препараты:
ZnCl2 – вяжущее, прижигающее и антисептическое действие – для лечения
воспаления слизистых.
ZnSO4 – 0,25 %-ный раствор в качестве глазных капель.
ZnO, ZnSO4 – в стоматологии в качестве временного пломбировочного материала.
ZnO – в дерматологии в виде мазей, присыпок, как вяжущее и противовоспалительное средство.
ZnSO4 – 0,25 %-ный раствор в качестве глазных капель.
ZnO, ZnSO4 – в стоматологии в качестве временного пломбировочного материала.
ZnO – в дерматологии в виде мазей, присыпок, как вяжущее и противовоспалительное средство.
Слайд 67Токсическое действие Cd, Hg:
Наиболее токсична метилртуть (CH3Hg+). Она образуется в водоемах
из неорганических соединений ртути под действием ферментов микроорганизмов:
Hg2+ + CH‾3→ CH3Hg+
карбанион метилртуть
Hg2+ + CH‾3→ CH3Hg+
карбанион метилртуть
Слайд 68 Метилртуть накапливается в рыбе, а затем с пищей попадает в организм
человека, растворяется в липидах мембран и проникает в клетки. Накапливается в почках, мозге, эритроцитах, проникает через плаценту в плод и нарушает структуру ДНК и РНК.
Слайд 69Постепенно концентрируясь, она вызывает необратимые разрушения в организме и смерть.
Отравление
метилртутью вызывает болезнь Минамата
(нервно-психические расстройства, нарушение координации движения).
(нервно-психические расстройства, нарушение координации движения).
Слайд 71Механизм токсического действия ртути и кадмия:
1. Ионы Cd2+ и Hg2+ могут
замещать Ca2+ в соединениях, т.к. имеют близкие радиусы.
Нарушение фосфорно-кальциевого обмена является причиной патологических изменений в костной ткани.
Cd2+, замещая Ca2+, вызывает болезнь итай-итай («страдание»), кости становятся хрупкими и ломаются при кашле, наблюдается искривление позвоночника у детей.
Нарушение фосфорно-кальциевого обмена является причиной патологических изменений в костной ткани.
Cd2+, замещая Ca2+, вызывает болезнь итай-итай («страдание»), кости становятся хрупкими и ломаются при кашле, наблюдается искривление позвоночника у детей.
Слайд 722. У кадмия и особенно ртути ярко выражено химическое сродство к
SH – группам. Блокирование SH – групп, приводящее к подавлению активности ферментов и денатурации белков, идет по схеме:
SH S
R + Hg2+ R Hg + 2 H+
SH S
Антидоты: тетацин-кальций, унитиол, тиосульфат натрия.
SH S
R + Hg2+ R Hg + 2 H+
SH S
Антидоты: тетацин-кальций, унитиол, тиосульфат натрия.
Слайд 73Лекарственные препараты:
HgСl2 – в концентрации 1 : 1000 для дезинфекции и
как антисептик.
HgО – в составе мазей для лечения глазных и кожных заболеваний.
HgS - для лечения венерических и кожных заболеваний.
HgNH2Cl – в дерматологии
Hg2Сl2 - как слабительное в ветеринарии.
HgО – в составе мазей для лечения глазных и кожных заболеваний.
HgS - для лечения венерических и кожных заболеваний.
HgNH2Cl – в дерматологии
Hg2Сl2 - как слабительное в ветеринарии.

![Основные и восстановительные свойства Mn2+ MnO+H2SO4+5H2O=[Mn(H2O)6]SO4MnSO4+2NaOH=Mn(OH)2↓+Na2SO4Mn(OH)2+O2+H2O→Mn(OH)4→MnO2↓+H2O Качественная реакция на Mn2+ :2Mn(NO3)2+5NaВiO3+16HNO3= 2HMnO4+5Вi(NO3)3+5NaNO3+7H2O фиолетовое окрашивание](/img/tmb/5/492576/f49e9092715d2b6f5f7a3235dfc2154d-800x.jpg)











![Химические превращения (Fe3+)Fe(OH)3 проявляет амфотерные свойства, т.е. реагирует и с кислотами, и с основаниями:Fe(OH)3+3HCl=FeCl3+3H2O;Fe(OH)3+3NaOH=Na3[Fe(OH)6].](/img/tmb/5/492576/572a78fb724e98ff88558a891ac2d4fe-800x.jpg)



![б) миоглобин (Mb) осуществляет обратимый перенос кислорода в мышцах: [MbFe+2] + O2 [MbFe+2O2]; дезоксиформа оксиформа](/img/tmb/5/492576/eef6f2f40f6eba4f789b71a87a4406dd-800x.jpg)















![Химические свойства2Сu+O2=2CuOCuO+Cu=Cu2OCu2O+2HCl=2CuCl↓CuCl+2NH3=[Cu(NH3)2]Cl](/img/tmb/5/492576/1cee93935f6cb321c3748805fd522129-800x.jpg)





![Медьсодержащие ферменты оксигеназы [ОКГ Сu+] активируют молекулу кислорода в процессе окисления органических соединений: O[ОКГ](/img/tmb/5/492576/136648920ac591bb5009638e15bc2dda-800x.jpg)
![БиорольФермент супероксиддисмутаза [СОД Сu2+] ускоряет реакцию разложения токсичного супероксид-иона ·О2- [СОД Сu2+] +·О2- →](/img/tmb/5/492576/77beaf1a3b4e46014ca23d050c961f15-800x.jpg)
![Фермент цитохромоксидаза [Fe2+ЦХОСu+], катализирует перенос электронов на кислород на конечном этапе тканевого дыхания: 2[Fe2+ЦХОСu+] +](/img/tmb/5/492576/27209d657e0f8a7b088f0cc24f2d44b0-800x.jpg)
![Биороль Медьсодержащий белок плазмы крови церулоплазмин [ЦП]: а)катализирует окисление Fe+2 в Fe+3 в процессе кроветворения:Fe+2 + [ЦПСu2+]](/img/tmb/5/492576/9a6a406dd47e4fabd0032bb6dc125415-800x.jpg)
![б)восстановленная форма церулоплазмина [ЦПСu+] катализирует восстановление кислорода в воду:О2+4[ЦПСu+] +4H+ → 2H2O + 4 [ЦПСu2+]](/img/tmb/5/492576/3e9e424f8333df0d9322a42946977db9-800x.jpg)






![Химические свойства:2Zn+O2=2ZnOZnO+H2SO4=ZnSO4+H2OКачественная реакция на ион Zn2+ - образование белого осадка сульфида цинка ZnS: ZnSO4+H2S=ZnS↓+Н2SO4ZnSO4+4NH3=[Zn(NH3)4]SO4ZnSO4+2NaOH=Zn(OH)2↓+Na2SO4.](/img/tmb/5/492576/91d78c62f3aaf672085af1fe4bd3bc73-800x.jpg)
![Амфотерность Zn(OH)2Zn(OH)2 является амфотерным гидроксидом, реагирует и с кислотами, и с основаниями: Zn(OH)2+2HCl=ZnCl2+2H2OZn(OH)2+2NaOH=Na2[Zn(OH)4].](/img/tmb/5/492576/49cef4b8fc993f4e094e2b28caa88fa5-800x.jpg)