- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Биофизические основы патологии клетки. Свободные радикалы и болезни человека презентация
Содержание
- 1. Биофизические основы патологии клетки. Свободные радикалы и болезни человека
- 2. Перекисное Окисление Липидов
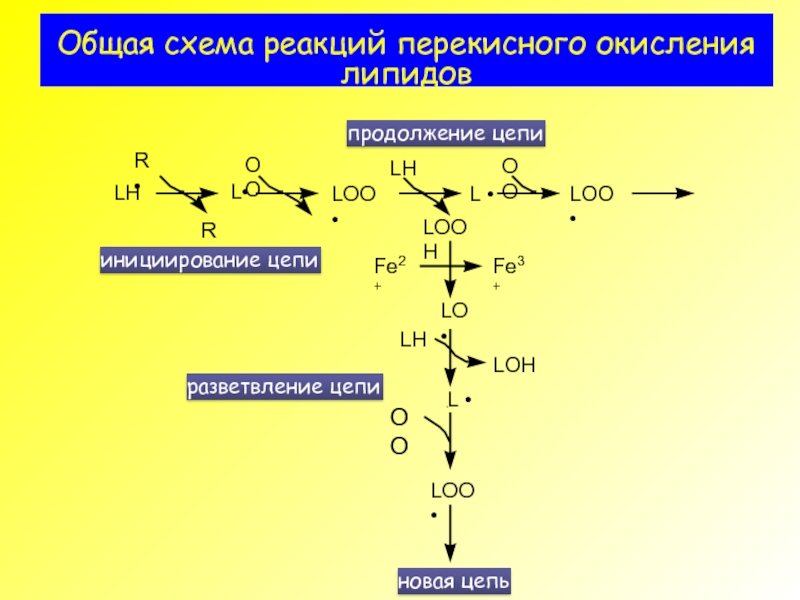
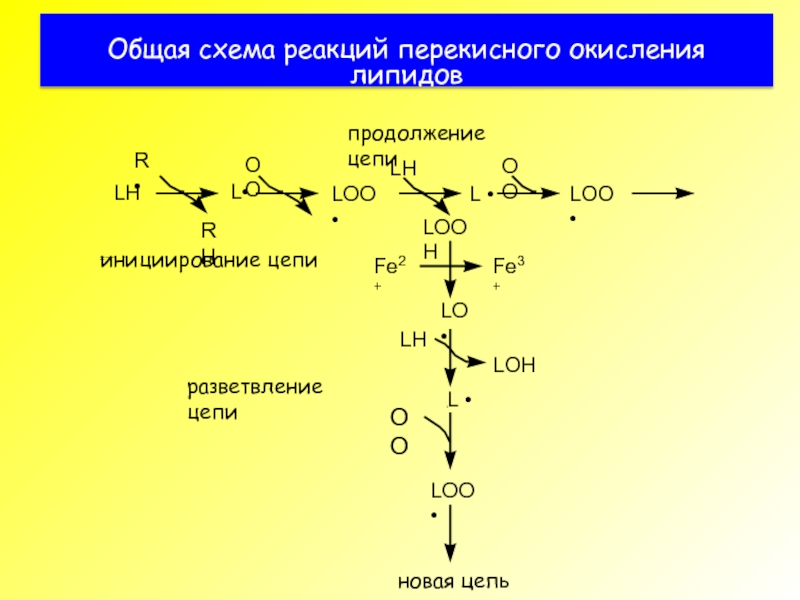
- 3. Общая схема реакций перекисного окисления липидов
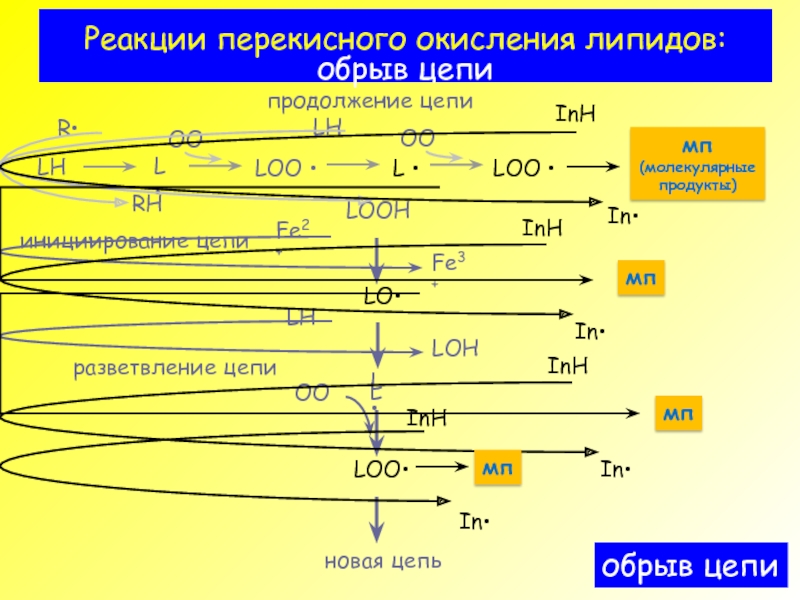
- 4. Реакции перекисного окисления липидов: обрыв цепи
- 5. Уравнения реакций цепного окисления липидов
- 6. Анализ кинетики ПОЛ
- 7. Уравнения реакций цепного окисления липидов
- 8. Уравнения реакций цепного окисления липидов
- 9. Кинетика перекисного окисления липидов БВ
- 10. Упрощение схемы химических реакций Правило 1: Скорость
- 11. Уравнения реакций цепного окисления липидов
- 12. Скорость нескольких последовательных реакций равна скорости самой
- 13. Уравнения реакций цепного окисления липидов
- 14. Уравнения реакций цепного окисления липидов
- 15. Скорость нескольких параллельных реакций в основном определяется
- 16. Уравнения реакций цепного окисления липидов
- 17. Уравнения реакций цепного окисления липидов
- 18. Пример 4: Вместо четырех реакций обрыва цепи
- 19. Упрощенная схема реакций перекисного окисления липидов из
- 20. Пример 2: Скорость реакции обрыва цепей определяется
- 21. Уравнения реакций цепного окисления липидов
- 22. Уравнения реакций цепного окисления липидов
- 23. Упрощенная схема реакций перекисного окисления липидов из
- 24. Дифференциальные уравнения кинеткики в системе трех реакций
- 25. Стационарное приближение Боденштейна – Семенова
- 26. Триггерная функция Fe2+ 1 2 3 4 5 6
- 27. Триггерная функция Fe2+ При γ = 0
- 28. Железо как про- и антиоксидант
- 29. Кинетика перекисного окисления липидов БВ
- 30. Хемилюминесценция при перекисном окислении липидов
- 31. Общая схема реакций перекисного окисления липидов
- 32. Уравнения реакций цепного окисления липидов
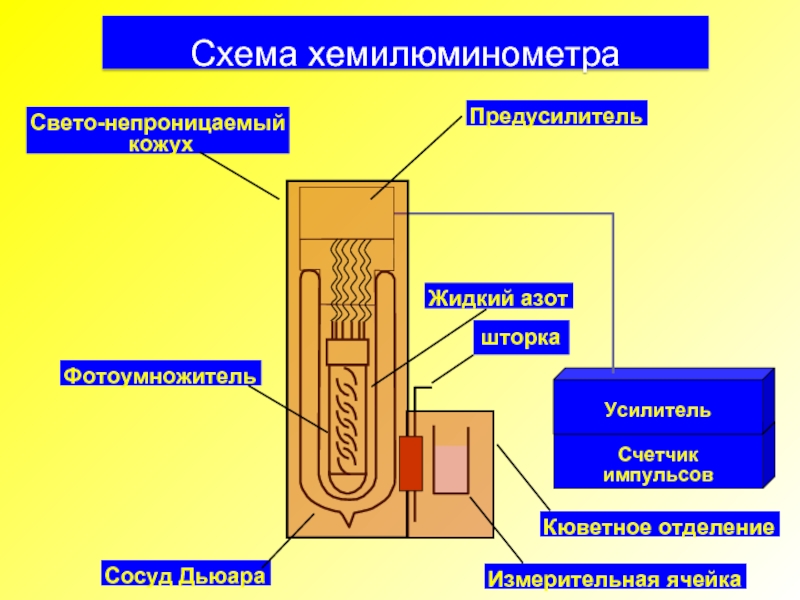
- 33. Схема хемилюминометра
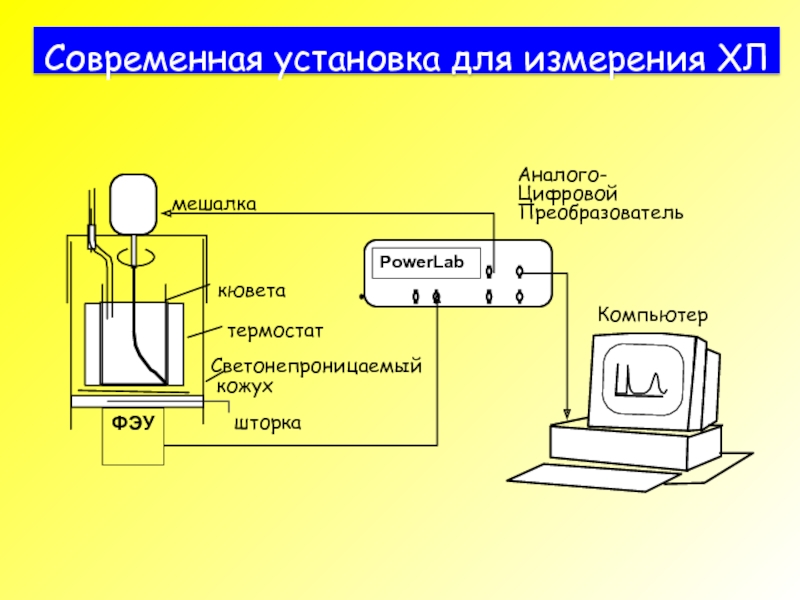
- 34. Современная установка для измерения ХЛ
- 35. Кинетика перекисного окисления липидов Владимиров, А., Т.Б.
- 36. Кинетика перекисного окисления липидов БВ
- 37. Эксперимент для изучения роли кислорода в ПОЛ
- 38. Хемилюминесценция при ПОЛ, индуцированном ионами Fe2+
- 39. Реакции ПОЛ, протекающие в присутствии и в
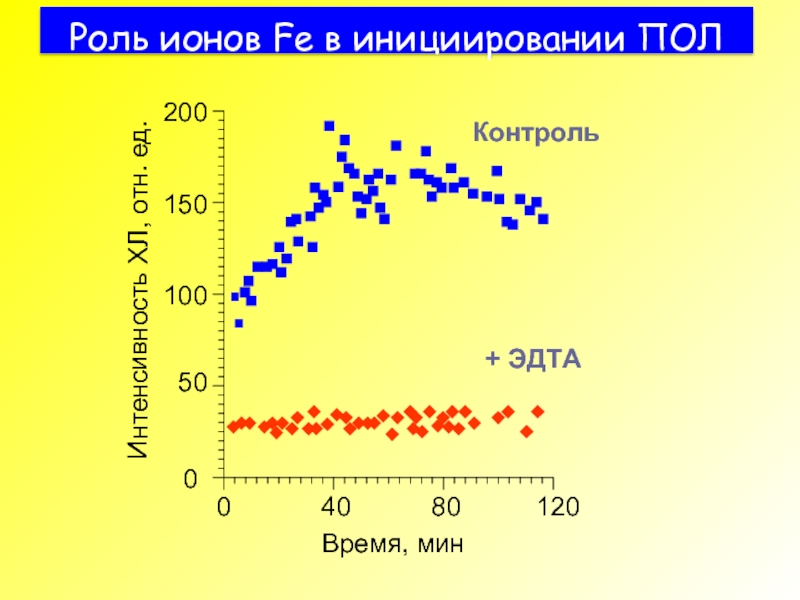
- 40. Роль ионов Fe в инициировании ПОЛ
- 41. Кинетика ХЛ (быстрая вспышка) при различных [Fe2+]
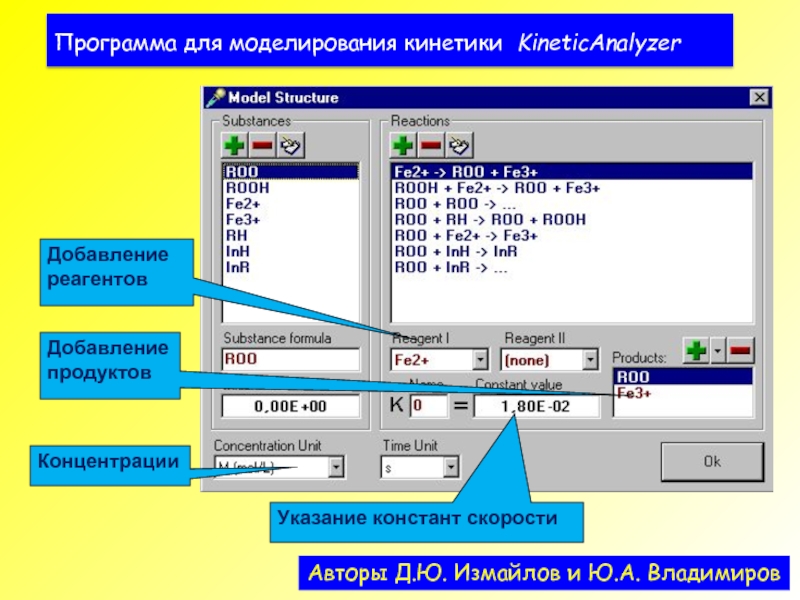
- 42. Программа для моделирования кинетики KineticAnalyzer Авторы Д.Ю. Измайлов и Ю.А. Владимиров
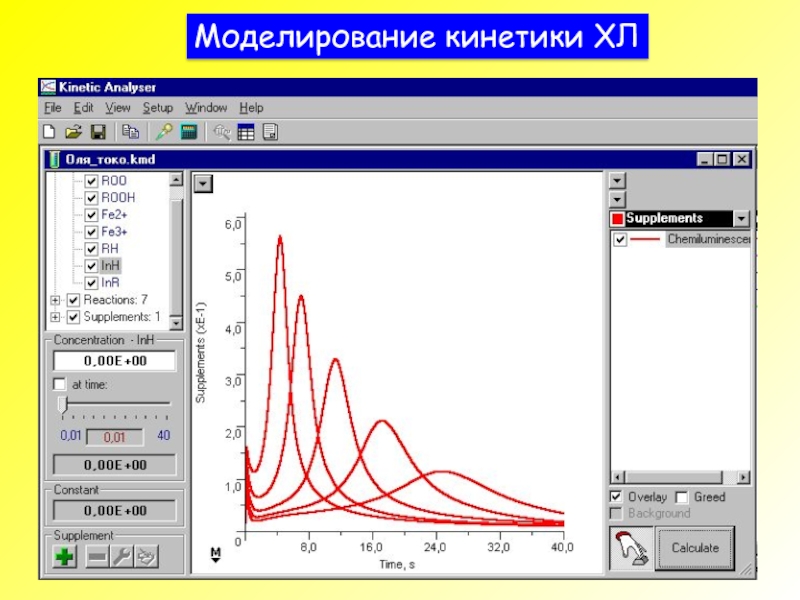
- 43. Моделирование кинетики ХЛ
- 44. Сравнение кинетики ХЛ (медленная вспышка) и ее
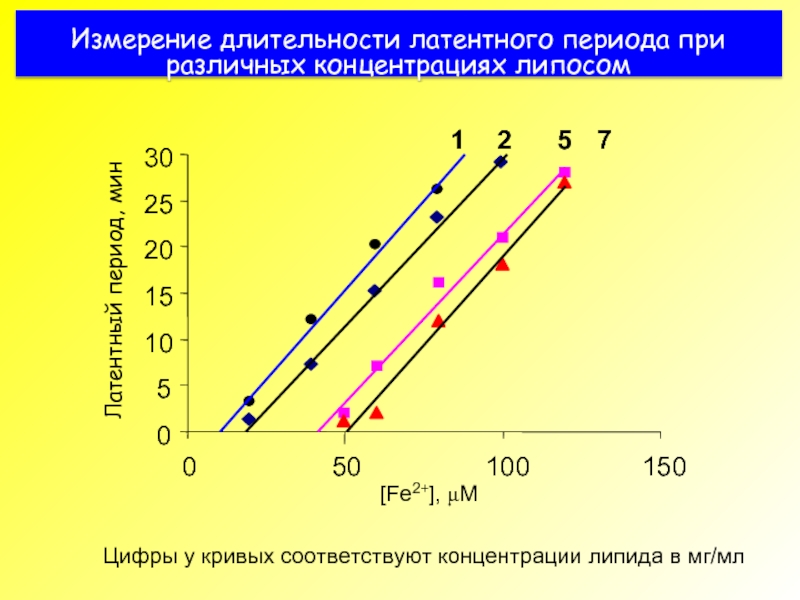
- 45. Измерение длительности латентного периода при различных концентрациях липосом
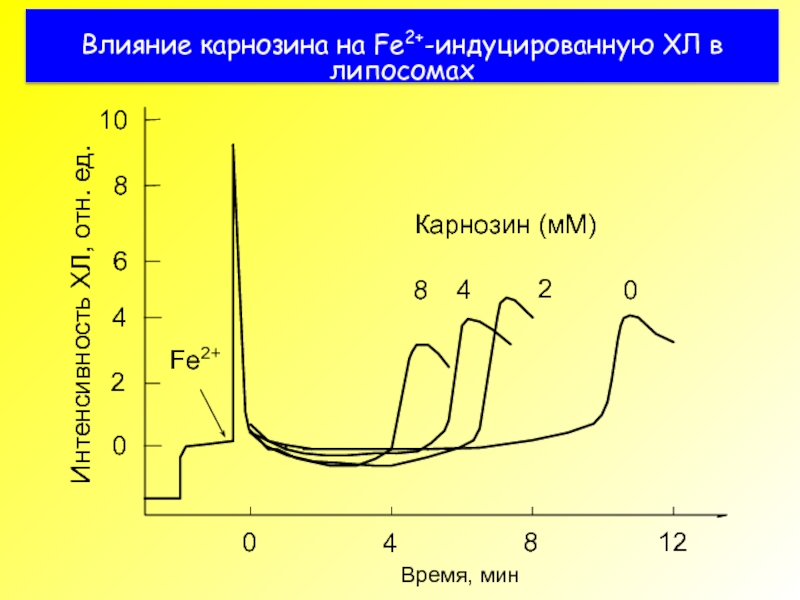
- 46. Влияние карнозина на Fe2+-индуцированную ХЛ в липосомах
- 47. Вопросы к зачету: Кинетика реакций цепного окисления
Слайд 1Свободные радикалы и болезни человека
Ю.А. Владимиров, А.Н. Осипов
2018
Биофизические основы патологии клетки
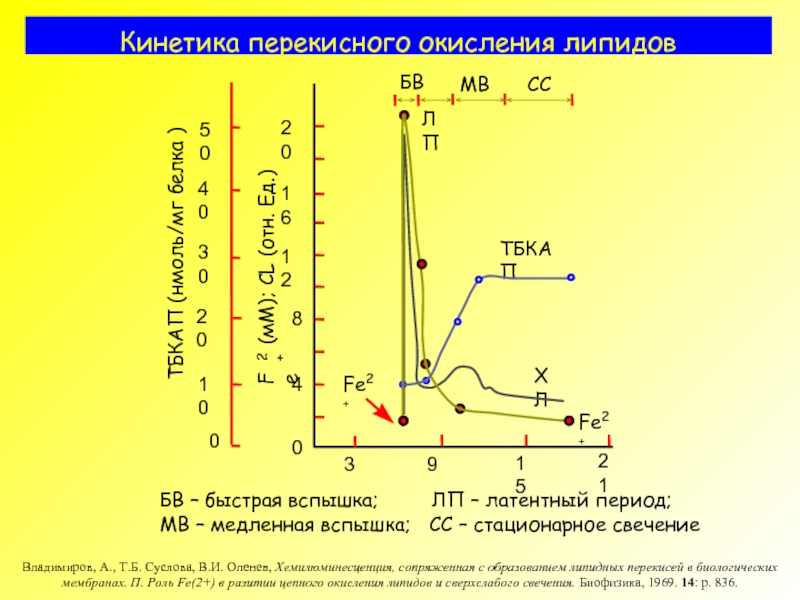
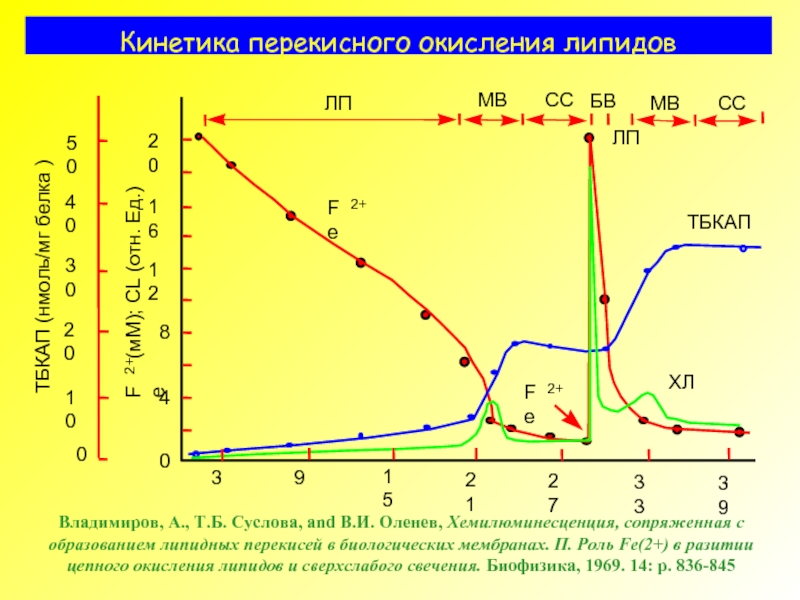
Слайд 9Кинетика перекисного окисления липидов
БВ – быстрая вспышка;
МВ – медленная вспышка; СС – стационарное свечение
Владимиров, А., Т.Б. Суслова, В.И. Оленев, Хемилюминесценция, сопряженная с образованием липидных перекисей в биологических мембранах. П. Роль Fe(2+) в разитии цепного окисления липидов и сверхслабого свечения. Биофизика, 1969. 14: p. 836.
Fe2+
Слайд 10Упрощение схемы химических реакций
Правило 1: Скорость нескольких последовательных реакций равна скорости
Правило 2: Скорость нескольких параллельных реакций в наибольшей мере определяется скоростью самой быстрой из них.
Иногда можно пренебречь остальными реакциями при расчетах.
Для упрощения системы химических реакций используют два правила химической кинетики:
Слайд 12Скорость нескольких последовательных реакций равна скорости самой медленной из них
Пример 1:
2) O2 + L· → LOO· v2 = k2 [O2]L·]
3) LH + LOO· → L· + LOOH v3 = k3 [LH][LOO·]
Пишем одну:
L· + O2 (+ LH) → LOOH + LOO· v2+3 ≈ v2 [O2][L·]
Пример 2: Вместо двух реакций разветвления цепи:
4) Fe2+ + LOOH → Fe3+ + LO· + OH¯ v4 = k4 [Fe2+] LOOH]
5) LO· + LH → LOH + L· v5 = k5 [LO·][LH]
Пишем одну:
Fe2+ + LOOH (+ LH) → Fe3+ + L· v4+5 ≈ k4 [Fe2+] LOOH]
Примечание:
На кинетику процесса в целом не влияют те продукты, которые не участвуют в дальнейших реакциях. Поэтому на схеме реакций мы можем их не указывать.
Слайд 15Скорость нескольких параллельных реакций в основном определяется самой быстрой из них
Пример
1) LH + HO· → L· + HOH v1 = k1 [LH][HO·]
4) Fe2+ + LOOH → Fe3+ + LO· + OH¯ v4 = k4 [Fe2+] LOOH]
При наличии Fe2+ скорость последней реакции гораздо выше, чем первой (т.к. концентрация HO· обычно бывает очень низкой). Поэтому основная масса радикалов образуется в реакции обрыва цепей:
Fe2+ + LOOH → Fe3+ + LO· + OH¯ v1+4 ≈ k4 [Fe2+] LOOH]
Слайд 18Пример 4: Вместо четырех реакций обрыва цепи оставим две, идущие в
Скорость нескольких параллельных реакций в наибольшей мере определяется скоростью самой быстрой из них.
6) LOO· + LOO· → МП + hν (k6)
9) L· + Fe2+ + H+ → Fe3+ + LH (k9)
Слайд 19Упрощенная схема реакций перекисного окисления липидов из 5 реакций
O2 + е-
L· + O2 (+ LH) → LOOH + L· (k2) Fe2+ + LOOH + LH → Fe3+ + LOH + OH¯ + L· (kp) LOO· + LOO· → L=O + LOH + фотон (k6)
Fe2+ + L· + H+ → Fe3+ + LH (k9)
Слайд 20Пример 2: Скорость реакции обрыва цепей определяется двумя параллельно идущими реакциями:
Fe2+
При наличии Fe2+ скорость первой реакции гораздо выше, чем второй. Поэтому пока есть Fe2+, основная реакция обрыва цепи – это реакция:
Fe2+ + L· + H+ → Fe3+ + LH (k9)
Скорость нескольких параллельных реакций в основном определяется самой быстрой из них
Слайд 23Упрощенная схема реакций перекисного окисления липидов из 3 реакций
L· + O2
Если считать, что образование радикалов идет , в основном, за счет реакции с ионами Fe2+, то можно удалить и реакцию (0). Тогда получим:
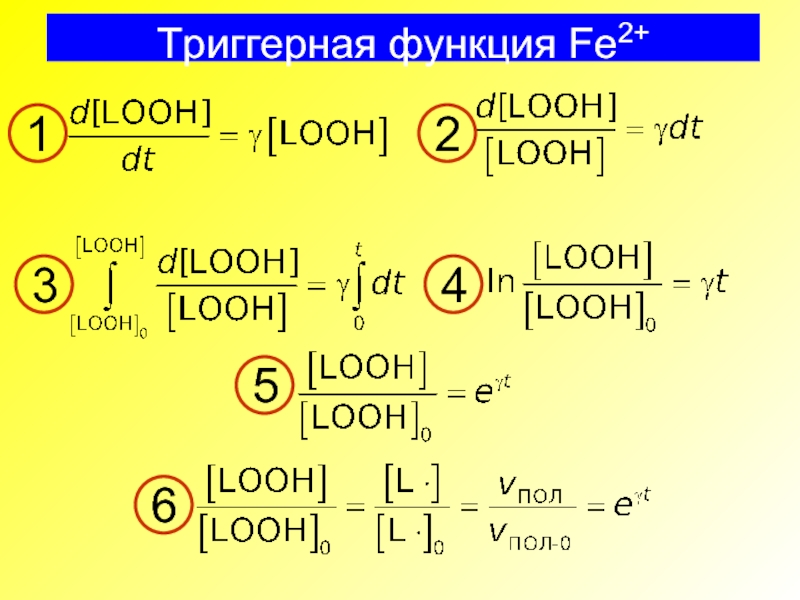
Слайд 27Триггерная функция Fe2+
При γ = 0
При [Fe2+] > [Fe2+] *, γ
γ = kp([Fe2+]* – [Fe2+])
При [Fe2+] < [Fe2+] *, γ > 0
1
2
3
4
5
6
Слайд 28Железо как про- и антиоксидант
[Fe2+] > [Fe2+] *
γ < 0
[Fe2+]
γ > 0
Скорость цепного окисления
Слайд 29Кинетика перекисного окисления липидов
БВ – быстрая вспышка;
МВ – медленная вспышка; СС – стационарное свечение
Владимиров, А., Т.Б. Суслова, В.И. Оленев, Хемилюминесценция, сопряженная с образованием липидных перекисей в биологических мембранах. П. Роль Fe(2+) в разитии цепного окисления липидов и сверхслабого свечения. Биофизика, 1969. 14: p. 836.
Fe2+
Слайд 35Кинетика перекисного окисления липидов
Владимиров, А., Т.Б. Суслова, and В.И. Оленев, Хемилюминесценция,
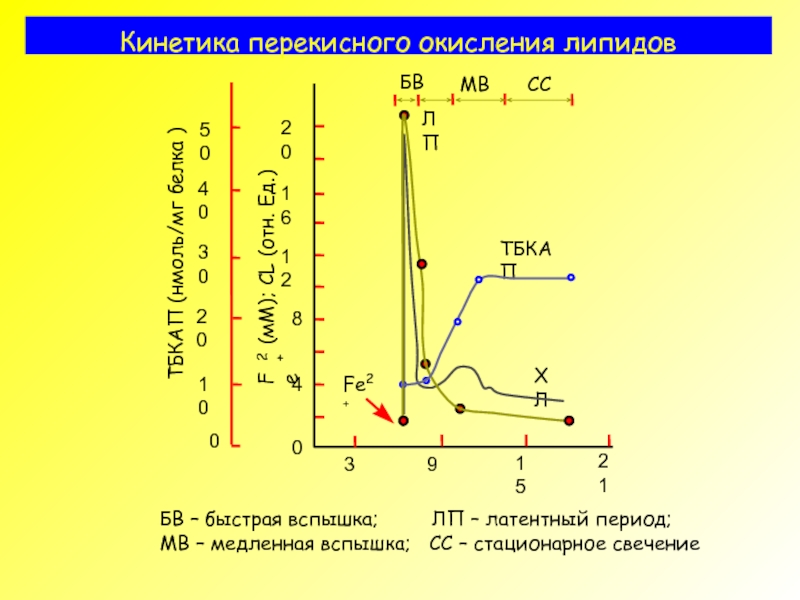
Слайд 36Кинетика перекисного окисления липидов
БВ – быстрая вспышка;
МВ – медленная вспышка; СС – стационарное свечение
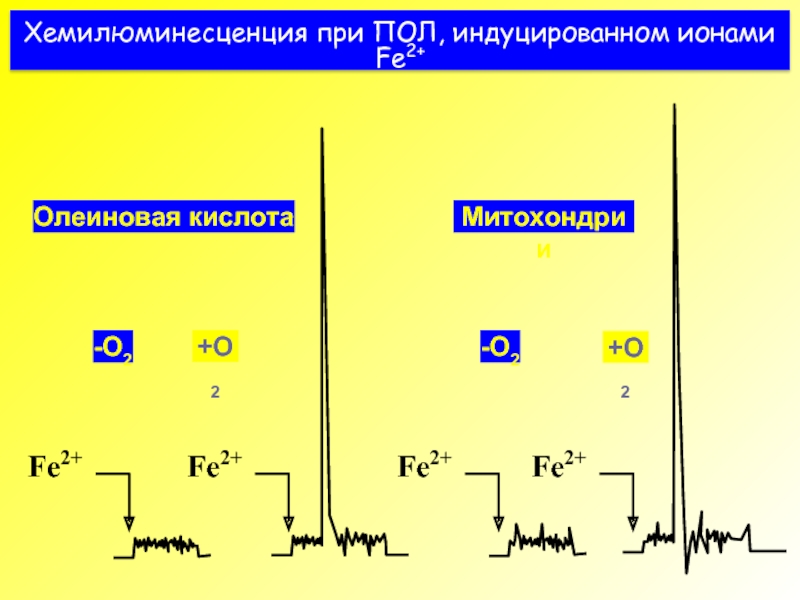
Слайд 38Хемилюминесценция при ПОЛ, индуцированном ионами Fe2+
Олеиновая кислота
-O2
+O2
Митохондрии
+O2
-O2
Слайд 39Реакции ПОЛ, протекающие в присутствии и в отсутствие О2
Без кислорода:
Fe2+ +
LO∙ + LH ⇒ LOH + L∙
L∙ + L∙ ⇒
LO∙ + LO∙ ⇒
L∙ + LO∙ ⇒
В присутствии кислорода:
Fe2+ + LOOH ⇒ Fe3+ + LO∙
LO∙ + LH ⇒ LOH + L∙
L∙ + O2 ⇒ LOO∙
L∙ + L∙ ⇒
LO∙ + LO∙ ⇒
LOO∙ + LOO∙ ⇒ L=O* ⇒ LO + hν
L∙ + LO∙ ⇒
LO∙ + LOO∙ ⇒
L∙ + LOO∙ ⇒
I = ηk6[LOO∙]2
η = 10-9 ÷ 10-15
Слайд 44Сравнение кинетики ХЛ (медленная вспышка) и ее модели при разных [Fe2+]
Измеренные кривые
Рассчитанные кривые
Слайд 47Вопросы к зачету:
Кинетика реакций цепного окисления липидов
Кривые кинетики цепного окисления липидов
Уравнения реакций цепного окисления липидов
Скорости парциальных реакций цепного окисления
Упрощение схемы химических реакций. Скорость системы параллельных реакций.
Упрощение схемы химических реакций. Скорость системы последовательных реакций.
Упрощение схемы химических реакций. Как из системы из 9 реакций мы приходим к системе из 5 реакций?
Алгоритм расчета кривых кинетики реакции на ЭВМ.
Аналитическое решение уравнений кинетики ПОЛ. Дальнейшее упрощение системы реакций (от 5 до 3).
Дифференциальные уравнения кинетики в системе трех реакций. Стационарное приближение Боденштейна – Семенова.
Зависимость скорости реакции пероксидации от концентрации ионов железа. Понятие "критической концентрации" железа.
Тригерная функция Fe2+. Железо как про- и антиоксидант.






















![Триггерная функция Fe2+При γ = 0При [Fe2+] > [Fe2+] *, γ < 0γ = kp([Fe2+]*](/img/tmb/1/77669/1f9f22b805e3405d56ed8a41ba5d4ce5-800x.jpg)
![Железо как про- и антиоксидант[Fe2+] > [Fe2+] *γ < 0[Fe2+] < [Fe2+] *γ > 0Скорость](/img/tmb/1/77669/fa4b1481f13f6e07d8141621714ec805-800x.jpg)





![Кинетика ХЛ (быстрая вспышка) при различных [Fe2+]](/img/tmb/1/77669/33325af34af7894ad9cc5583f122d210-800x.jpg)
![Сравнение кинетики ХЛ (медленная вспышка) и ее модели при разных [Fe2+] Измеренные кривыеРассчитанные кривые](/img/tmb/1/77669/f41329fa1b59996e576cc2f29512bd53-800x.jpg)