- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Биоэнергетика. Современное представление о биологическом окислении презентация
Содержание
- 1. Биоэнергетика. Современное представление о биологическом окислении
- 2. Детоксикация ксенобиотиков Регуляция обмена веществ
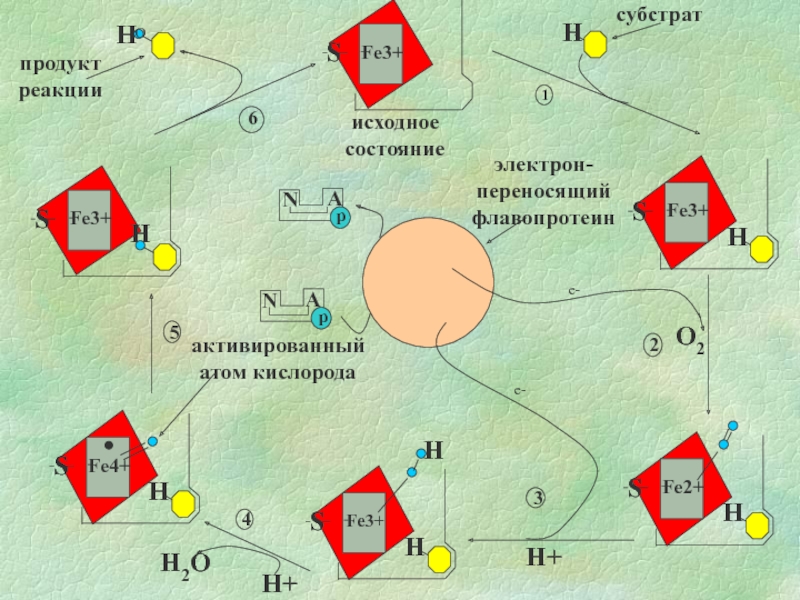
- 3. Способы передачи электронов 1. Прямой перенос электронов
- 4. I. Оксидазный: в митохондриях II. Пероксидазный :
- 5. III Оксигеназный : в ЭПР а)
- 6. ПОЛ мембран Окисление белков мембран Изменение функций клеток ОКИСЛИТЕЛЬНЫЕ ПУТИ
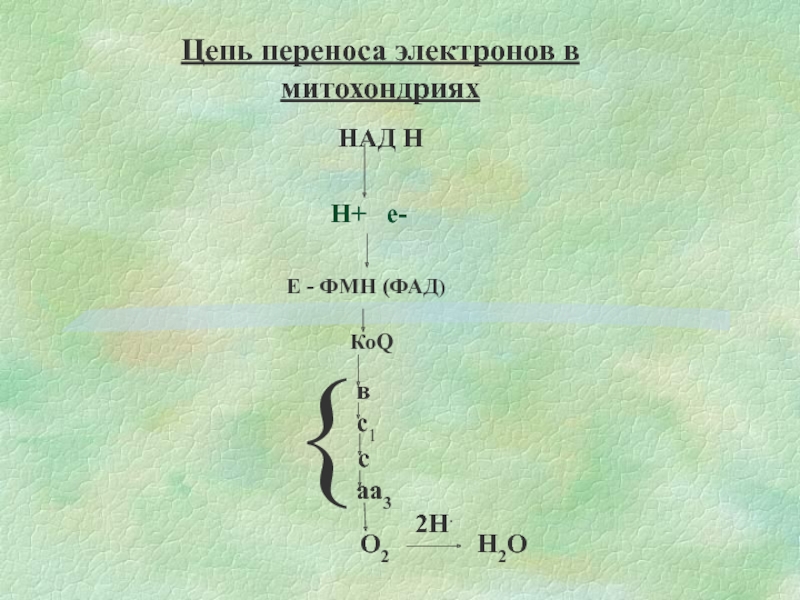
- 7. НАД Н Н+ е- Е
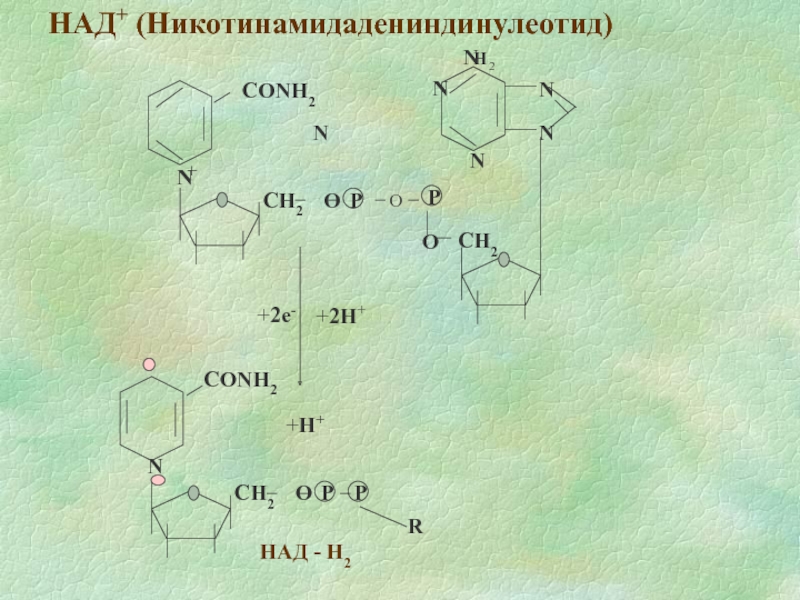
- 8. НАД+ (Никотинамидадениндинулеотид) +2e- +2H+
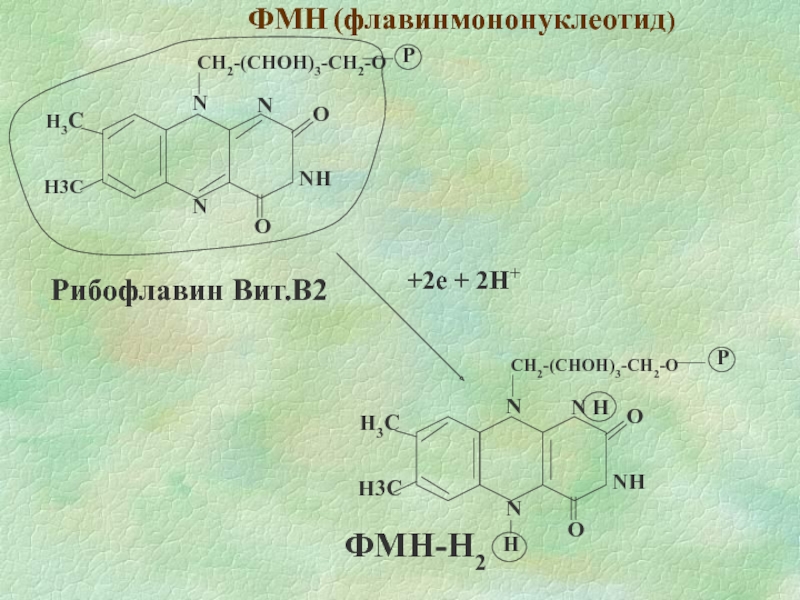
- 9. ФМН (флавинмононуклеотид) Рибофлавин Вит.B2 +2e + 2H+
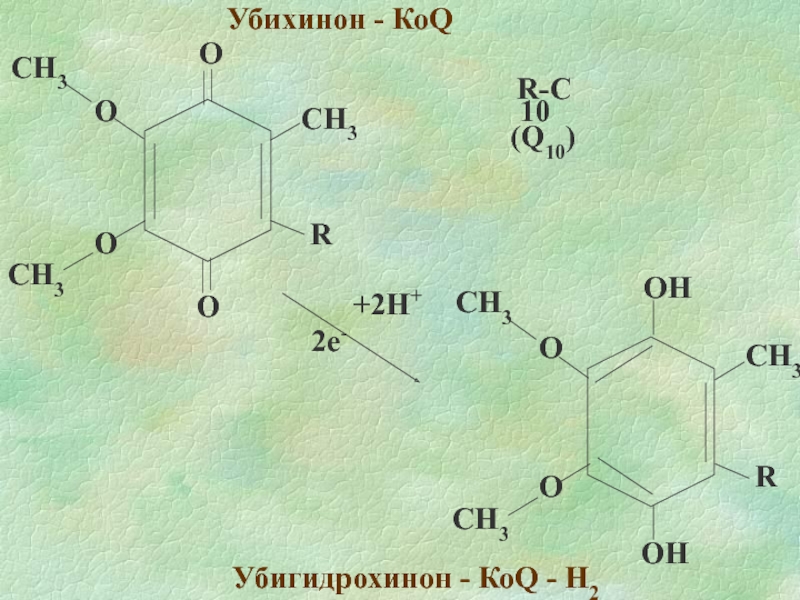
- 10. Убихинон - КоQ Убигидрохинон - КоQ - H2 2e- +2H+
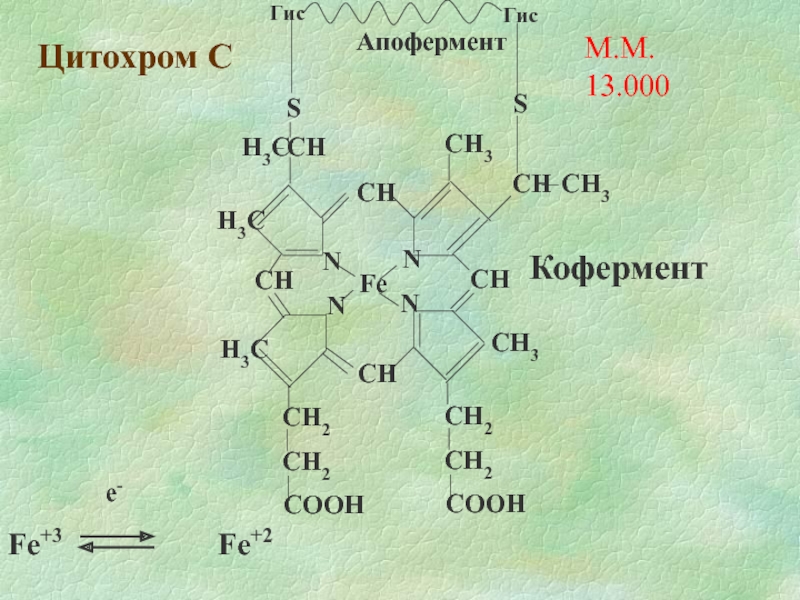
- 11. Цитохром С М.М. 13.000 е-
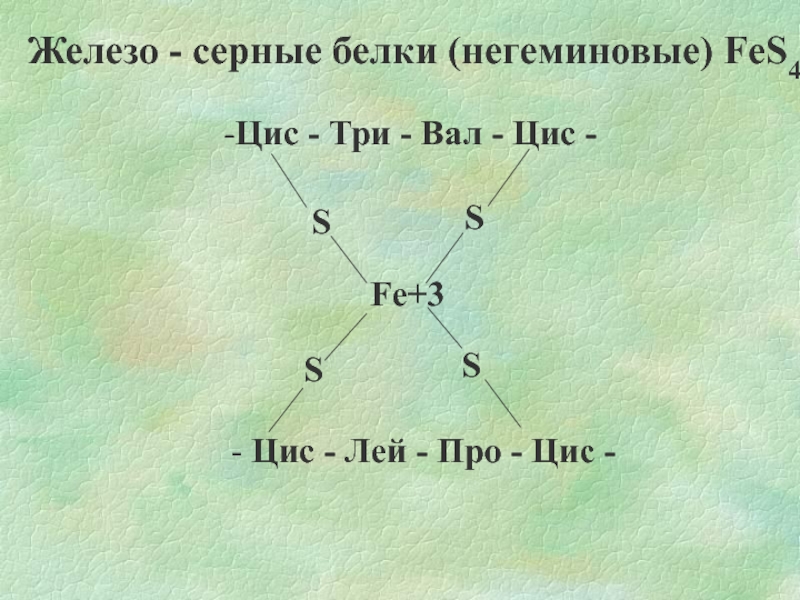
- 12. Железо - серные белки (негеминовые) FeS4
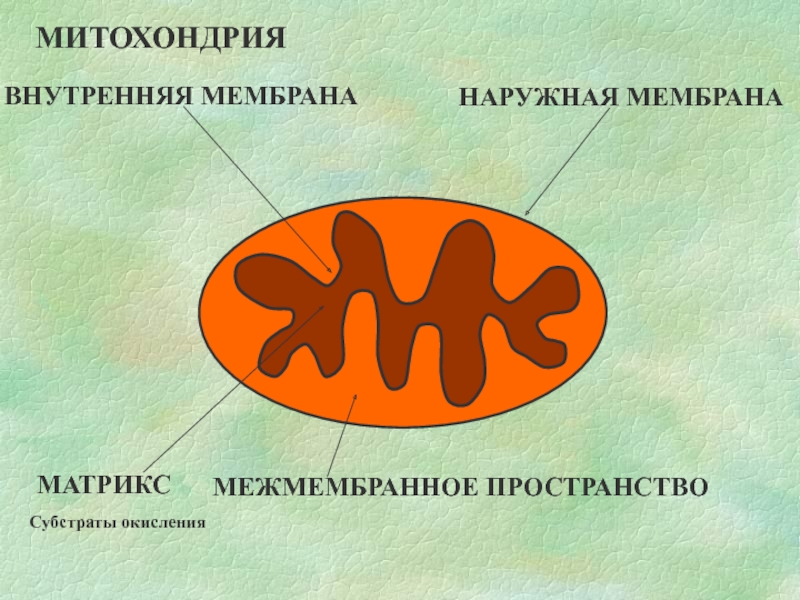
- 13. МАТРИКС МЕЖМЕМБРАННОЕ ПРОСТРАНСТВО ВНУТРЕННЯЯ МЕМБРАНА НАРУЖНАЯ МЕМБРАНА МИТОХОНДРИЯ Субстраты окисления
- 14. FMN е FeS
- 15. Разность Е0 стандартных потенциалов от НАДН2/НАД к
- 16. Оксидазный путь Дыхательная цепь переносчиков Н+ и
- 17. Коллекторная функция НАД и ФП (ФМН, ФАД)
- 18. СУБСТРАТНОЕ ФОСФОРИЛИРОВАНИЕ (образование АТФ из высокоэнергетических соединений)
- 19. W + АДФ + Фнеорг
- 20. Тканевое дыхание (ox - red цепи) Роль трансмембранного электрохимического потенциала (ΔμH) (Акад. Скулачев)
- 22. АТФ - синтаза (белки
- 23. Микросомальное окисление SН+НАДФH2 + O2
- 24. O2 H H+
- 25. Спасибо за внимание!
Слайд 1Военно-медицинская академия
доцент Шелепина Е.П.
Лекция
По Биохимии
Тема: Биоэнергетика.
Современное представление о биологическом
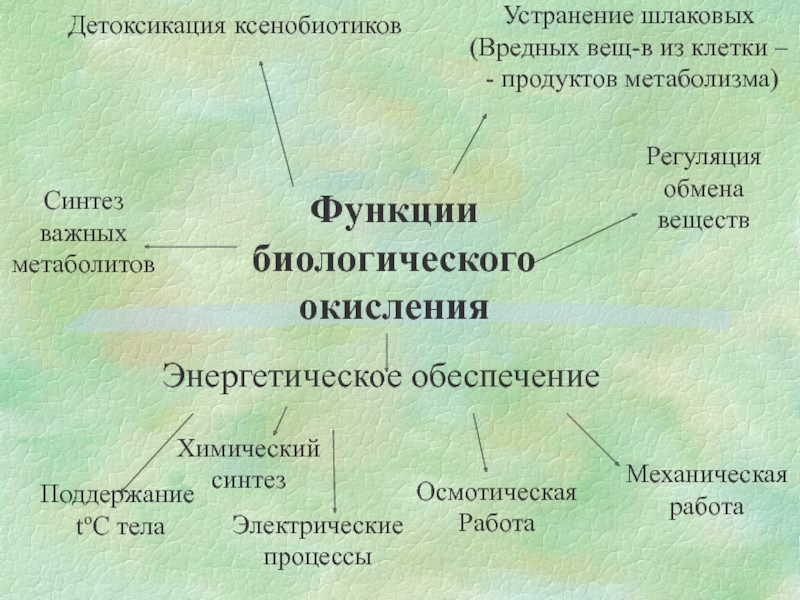
Слайд 2Детоксикация ксенобиотиков
Регуляция
обмена
веществ
Устранение шлаковых
(Вредных вещ-в из клетки –
- продуктов
Синтез
важных
метаболитов
Функции
биологического
окисления
Энергетическое обеспечение
Химический
синтез
Поддержание
toC тела
Электрические
процессы
Осмотическая
Работа
Механическая
работа
Слайд 3Способы передачи электронов
1. Прямой перенос электронов
Fe2+ + Cu2+
2. Перенос в составе атомов водорода (H+ + е )
AH2 ---- A + 2e + 2H+
AH2 + B A + BH2
3. Перенос в форме гидрид – иона.(:H- ).
4.Прямое взаимодействие органического восстановителя с кислородом.
R-CH3 + ½ O2 ----- R-CH2-OH
Под окислением понимают отщепление электронов,
а под восстановлением – присоединение электронов.
Слайд 4I. Оксидазный: в митохондриях
II. Пероксидазный : в макрофагах, фагоцитах, лейкоцитах,
гистиоцитах
перекись водорода
*МПО - миелопероксидаза
S + ФМН SOX + ФМН-Н2
ФМН-Н2 +О2 ФМН + Н2О2
Н2О2 + CI - Н2О
МПО
ОКИСЛИТЕЛЬНЫЕ ПУТИ
HOCI +
H2O2 + AH2 2H2O + A
ПО
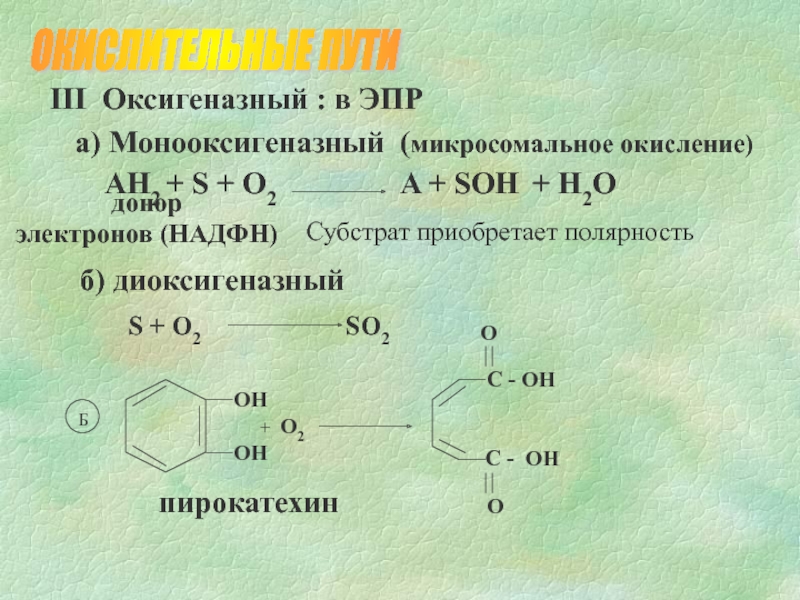
Слайд 5III Оксигеназный : в ЭПР
а) Монооксигеназный (микросомальное окисление)
б) диоксигеназный
S +
Субстрат приобретает полярность
ОКИСЛИТЕЛЬНЫЕ ПУТИ
АН2 + S + O2 A + SOH + H2O
донор
электронов (НАДФН)
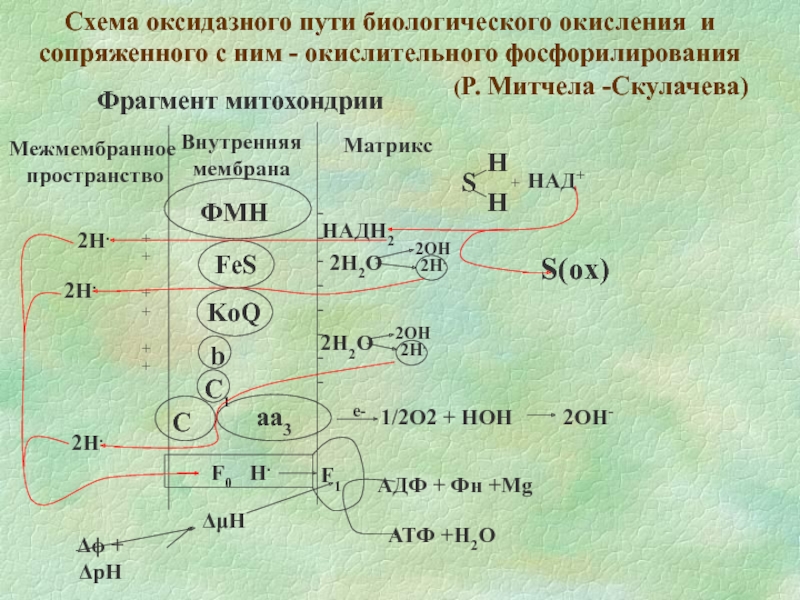
Слайд 13МАТРИКС
МЕЖМЕМБРАННОЕ ПРОСТРАНСТВО
ВНУТРЕННЯЯ МЕМБРАНА
НАРУЖНАЯ МЕМБРАНА
МИТОХОНДРИЯ
Субстраты окисления
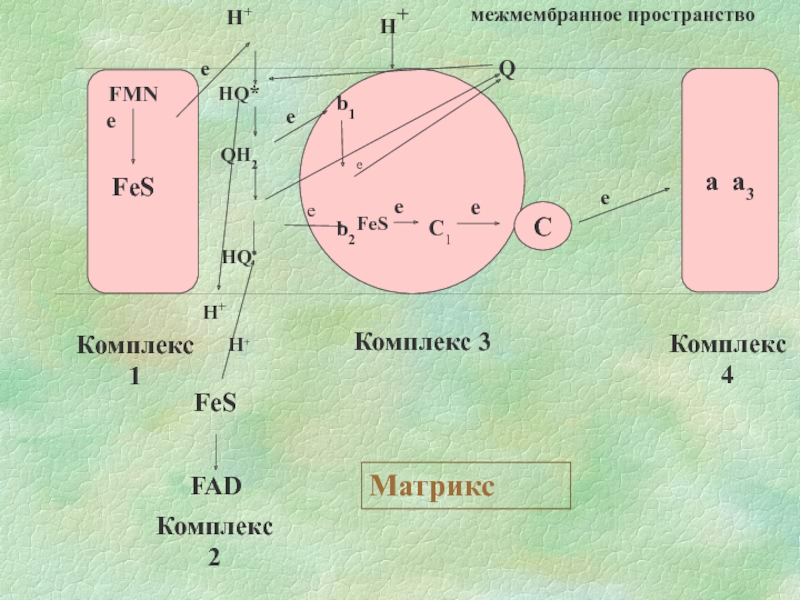
Слайд 14
FMN
е
FeS
H+
HQ*
QH2
HQ*
H+
b1
e
b2
FeS
C1
Q
C
a
е
е
е
е
H+
е
H+ межмембранное пространство
е
Комплекс 1
Комплекс 3
Комплекс 4
_____________________________________________________________________________________________________________________________________________
__________________________________________________________________________________________________________________________________________
FeS
FAD
Комплекс 2
Матрикс
Слайд 15Разность Е0 стандартных потенциалов от НАДН2/НАД
к паре Н2О/1/2О2 равна [0,82 V
Величина ΔΥ = 52,6 ккал или 220кДж
Изменение стандартной свободной энергии (ΔΥ0) , обусловленное
перемещением пары электронов по дыхательной цепи к кислороду. На 3х участках выделя-
ется достаточная энергия, необходимая для 3АДФ + W 3АТФ
~ 10 ккал
АДФ + Фн АТФ + Н2О
W - 7,3 ккал
ΔΥο =−n*F*ΔEo
n - число е
F - число Фарадея (ккал/v*m)
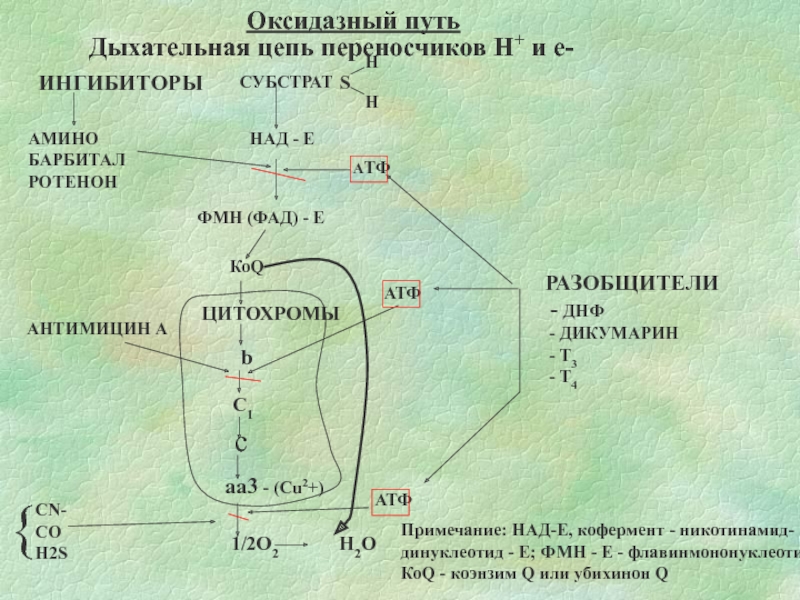
Слайд 16Оксидазный путь
Дыхательная цепь переносчиков Н+ и е-
ИНГИБИТОРЫ
АМИНО
БАРБИТАЛ
РОТЕНОН
НАД - Е
АТФ
ФМН (ФАД) -
РАЗОБЩИТЕЛИ
- ДНФ
- ДИКУМАРИН
- Т3
- Т4
АТФ
КоQ
ЦИТОХРОМЫ
b
C1
c
aa3 - (Cu2+)
1/2O2 H2O
CN-
CO
H2S
{
АТФ
АНТИМИЦИН А
Примечание: НАД-Е, кофермент - никотинамид-
динуклеотид - Е; ФМН - Е - флавинмононуклеотид - Е;
КоQ - коэнзим Q или убихинон Q
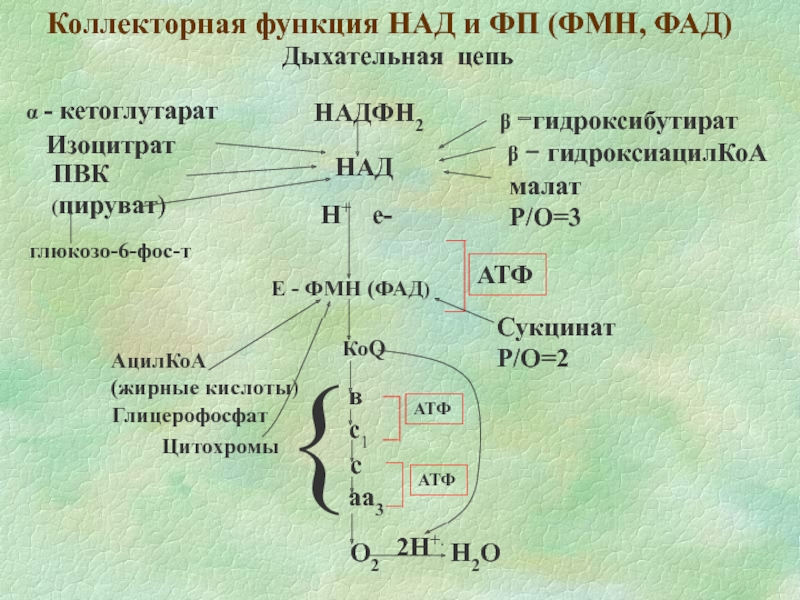
Слайд 17Коллекторная функция НАД и ФП (ФМН, ФАД)
О2
Н2О
Дыхательная цепь
НАДФН2
НАД
Н+ е-
Е -
2Н+.
Слайд 18СУБСТРАТНОЕ ФОСФОРИЛИРОВАНИЕ
(образование АТФ из высокоэнергетических соединений)
СН2
С O ~
СООН
ФЕП
(ФОСФОЕНОЛ-
ПИРУВАТ)
ПВК-КИНАЗА
АДФ
АТФ
(ПИРУВАТ)
СН3
С O
СООН
Слайд 19
W + АДФ + Фнеорг
1936 г. проф. Энгельгардт В.Н.
ФОСФОРИЛИРОВАНИЕ АДФ СОПРЯЖЕНО С АЭРОБНЫМ ДЫХАНИЕМ
Р/О = 3
Число молекул неорганического фосфата, перешедших в органическую форму (АТФ), в расчете на каждый поглощенный атом кислорода близко к 3
1940 - 41 г. проф. Белицер В.А.
АТФ АДФ + 7,6 ккал + Фн
Энергия
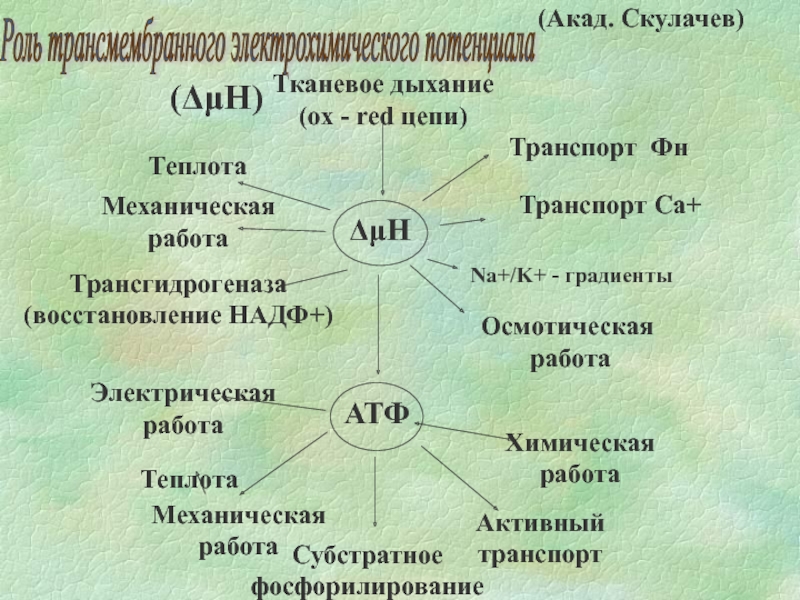
Слайд 20Тканевое дыхание
(ox - red цепи)
Роль трансмембранного электрохимического потенциала
(ΔμH)
(Акад. Скулачев)
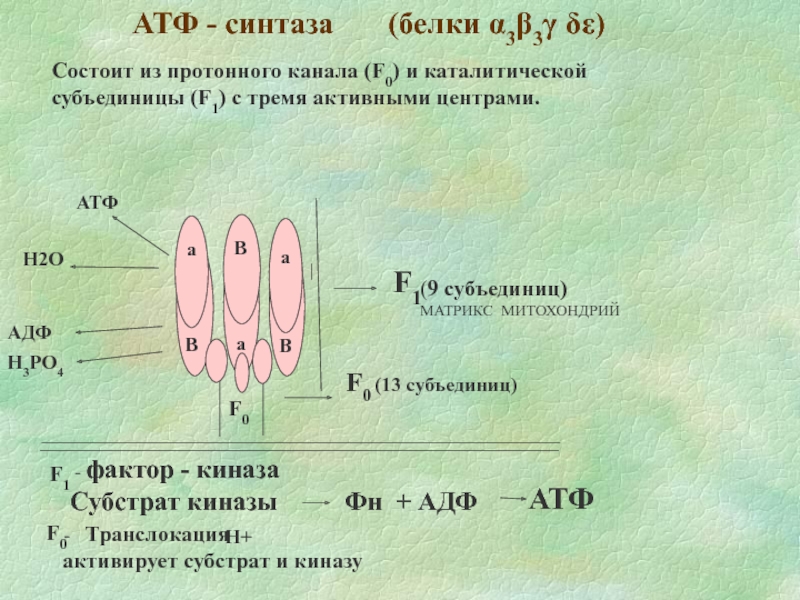
Слайд 22АТФ - синтаза (белки α3β3γ δε)
а
B
B
B
a
a
АТФ
H2O
АДФ
H3PO4
F0 (13 субъединиц)
F0
F1
Состоит
(9 субъединиц)
МАТРИКС МИТОХОНДРИЙ
АТФ
Слайд 23Микросомальное окисление
SН+НАДФH2 + O2 SOH + H2O +
1. НАДФH2 ФАД ФМН Fe3+ (P450) O2
. НАДH ФАД Fe3+ (в5) Fe3+ (P450 ) O2
В результате микросомального окисления происходит модификация субстрата с образованием функциональных групп, повышающих растворимость гидрофобного соединения.
2 цепи переноса электронов на комплекс (P450-SН-O2):




![Разность Е0 стандартных потенциалов от НАДН2/НАДк паре Н2О/1/2О2 равна [0,82 V - ( - 0,32V)]](/img/tmb/5/429560/2874633470de4fbb337331dd527512f8-800x.jpg)