- Главная
- Разное
- Дизайн
- Бизнес и предпринимательство
- Аналитика
- Образование
- Развлечения
- Красота и здоровье
- Финансы
- Государство
- Путешествия
- Спорт
- Недвижимость
- Армия
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Белки и нуклеиновые кислоты презентация
Содержание
- 1. Белки и нуклеиновые кислоты
- 2. Белки в природе Белки входят в состав
- 3. Состав и строение белков При рассмотрении строения
- 4. Первичная структура белков: Вторичная структура белков: Третичная структура белков: Четвертичная структура белков:
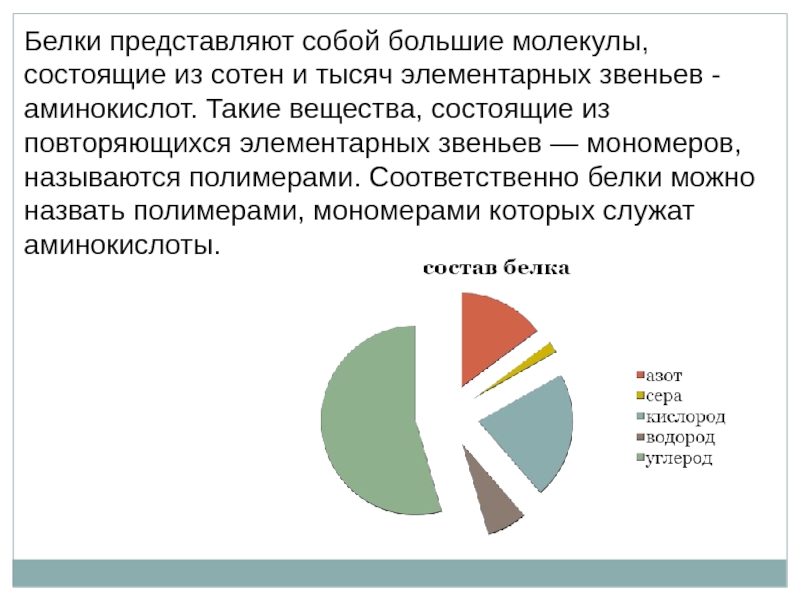
- 5. Белки представляют собой большие молекулы, состоящие из
- 6. Свойства белков Размер РАЗМЕР БЕЛКА МОЖЕТ
- 7. Амфотерность Физико-химические свойства: Растворимость Денатурация В зависимости
- 8. Превращения белков в организме. Белки — это основа
- 9. Проблема синтеза белков Белки представляют собой не
- 10. Причины невозможности получения белков синтетическим путем.
- 11. Нуклеиновые кислоты Нуклеиновая кислота — высокомолекулярное органическое
- 12. Мономерные формы также встречаются в клетках и
Слайд 2Белки в природе
Белки входят в состав клеток, тканей всех живых организмов,
Слайд 3Состав и строение белков
При рассмотрении строения белков выделяют четыре вида структур:
Вторичная структура — белковая цепь укладывается в спираль, состоящую из равномерных витков. Соседние витки соединены между собой слабыми водородными связями, которые при многократном повторении придают устойчивость молекулам белков с этой структурой. Третичная структура — спираль вторичной структуры укладывается в клубок. Форма клубка у каждого вида белков строго специфична и полностью зависит от первичной структуры, т. е. от порядка расположения аминокислот в цепи. Третичная структура удерживается благодаря множеству слабых электростатических связей: положительно и отрицательно заряженные группы аминокислот притягиваются и сближают даже далеко отстоящие друг от друга участки белковой цепи. Четвертичная структура — некоторые белки, например гемоглобин, состоят из нескольких цепей, различающихся по первичной структуре. Объединяясь вместе, они создают сложный белок.
Слайд 4Первичная структура белков:
Вторичная структура белков:
Третичная структура белков:
Четвертичная структура белков:
Слайд 5Белки представляют собой большие молекулы, состоящие из сотен и тысяч элементарных
Слайд 6Свойства белков
Размер
РАЗМЕР БЕЛКА МОЖЕТ ИЗМЕРЯТЬСЯ В ЧИСЛЕ АМИНОКИСЛОТНЫХ ОСТАТКОВ ИЛИ
Слайд 7Амфотерность
Физико-химические свойства:
Растворимость
Денатурация
В зависимости от условий проявляют кислотные и основные свойства.
В белках присутствуют несколько
Белки различаются по степени растворимости в воде. Водорастворимые белки называются альбуминами, к ним относятся белки крови и молока. К нерастворимым (склеропротеинам) относятся, например, кератин (волосы, шерсть млекопитающих, перья птиц и т. п.) и фиброин, который входит в состав шёлка и паутины.
Белки также делятся на гидрофильные и гидрофобные (водооталкивающие). К гидрофильным относится большинство белков цитоплазмы, ядра и межклеточного вещества, в том числе нерастворимые кератин и фиброин. К гидрофобным относится большинство белков, входящих в состав биологических мембран.
Денатурация белка – это любое изменение в его биологической
активности или физико-химических свойствах, связанные с потерей четвертичной,
третичной или вторичной структуры.
Денатурация белка может быть полной или частичной, обратимой или необратимой.
Слайд 8Превращения белков в организме.
Белки — это основа жизни. Из них построена цитоплазма,
Животные и растительные белки в пищеварительном тракте человека расщепляются на аминокислоты. Всасываясь, аминокислоты кровью доставляются в клетки тканей. Здесь из аминокислот под действием ферментов синтезируются белки, свойственные тканям человеческого тела.
Для синтезирования белков необходимо наличие определенных аминокислот. Но в одних белках, поступающих с пищей, имеются все необходимые человеку аминокислоты, а в других не все. Организм человека может сам синтезировать некоторые аминокислоты или заменять их другими. Но 10 аминокислот он образовать не в состоянии. Их должен непременно получать с пищей. Эти кислоты называются незаменимыми.
Белки, содержащие все необходимые аминокислоты, называют полноценными. Остальные белки - неполноценные. Полноценными являются белки молока, сыра, мяса, рыбы, яиц, картофеля, бобовых.
Синтезом белков в клетках управляет ДНК. Он осуществляется на поверхности рибосом с помощью РНК. В организме человека белки почти не откладываются в запас. Излишки аминокислот в клетках печени превращаются в углеводы — глюкозу и гликоген или в резервный жир. Поэтому артистам балета слишком больших количеств белков в пище нужно избегать. Но и намеренное голодание, когда вследствие больших энерготрат организм, израсходовав запасы углеводов и жира, начинает тратить резервы белка, очень вредно. Это тратятся белки цитоплазмы клеток.
Слайд 9Проблема синтеза белков
Белки представляют собой не просто определенную последовательность остатков аминокислот.
Слайд 10Причины невозможности получения белков синтетическим путем. 1. Причина – в чрезвычайной сложности
Слайд 11Нуклеиновые кислоты
Нуклеиновая кислота — высокомолекулярное органическое соединение, биополимер (полинуклеотид), образованный остатками
Физические свойства:
Нуклеиновые кислоты хорошо растворимы в воде, практически нерастворимы в органических растворителях. Очень чувствительны к действию температуры и критическим значениям уровня pH. Молекулы ДНК с высокой молекулярной массой, выделенные из природных источников, способны фрагментироваться под действием механических сил, например, при перемешивании раствора. Нуклеиновые кислоты фрагментируются ферментами — нуклеазами.
Состав:
Полимерные формы нуклеиновых кислот называют полинуклеотидами. Цепочки из нуклеотидов соединяются через остаток фосфорной кислоты (фосфодиэфирная связь). Поскольку в нуклеотидах существует только два типа гетероциклических молекул, рибоза и дезоксирибоза, то и имеется лишь два вида нуклеиновых кислот — дезоксирибонуклеиновая (ДНК) и рибонуклеиновая (РНК).
Слайд 12Мономерные формы также встречаются в клетках и играют важную роль в
ДНК (дезоксирибонуклеиновая кислота). Сахар — дезоксирибоза, азотистые основания: пуриновые — гуанин (G), аденин (A), пиримидиновые — тимин (T) и цитозин (C). ДНК часто состоит из двух полинуклеотидных цепей, направленных антипараллельно.
РНК (рибонуклеиновая кислота). Сахар — рибоза, азотистые основания: пуриновые — гуанин (G), аденин (A), пиримидиновые урацил (U) и цитозин (C). Структура полинуклеотидной цепочки аналогична таковой в ДНК. Из-за особенностей рибозы молекулы РНК часто имеют различные вторичные и третичные структуры, образуя комплементарные участки между разными цепями. ДНК (дезоксирибонуклеиновая кислота). Сахар — дезоксирибоза, азотистые основания: пуриновые — гуанин (G), аденин (A), пиримидиновые — тимин (T) и цитозин (C). ДНК часто состоит из двух полинуклеотидных цепей, направленных антипараллельно.
РНК (рибонуклеиновая кислота). Сахар — рибоза, азотистые основания: пуриновые — гуанин (G), аденин (A), пиримидиновые урацил (U) и цитозин (C). Структура полинуклеотидной цепочки аналогична таковой в ДНК. Из-за особенностей рибозы молекулы РНК часто имеют различные вторичные и третичные структуры, образуя комплементарные участки между разными цепями.